Cianeto
| Cianeto | |
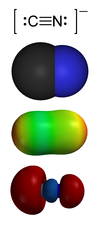
| |
| Identificação | |
|---|---|
| N o CAS | |
| PubChem | 5975 |
| ChEBI | 17514 |
| SORRISOS |
[C -] # N , |
| InChI |
InChI: InChI = 1 / CN / c1-2 / q-1 InChIKey: XFXPMWWXUTWYJX-UHFFFAOYAF Padrão. InChI: InChI = 1S / CN / c1-2 / q-1 Std. InChIKey: XFXPMWWXUTWYJX-UHFFFAOYSA-N |
| Propriedades quimicas | |
| Fórmula bruta |
C N - |
| Massa molar | 26,0174 ± 0,001 g / mol C 46,16%, N 53,84%, |
| Propriedades eletrônicas | |
| 1 energia de re ionização | 13,5984 eV (gás) |
| Considerações Terapêuticas | |
| Antídoto | Tiossulfato de sódio |
| Unidades de SI e STP, salvo indicação em contrário. | |
Em química, o termo cianeto - da palavra grega κυανός ( kyanos ) que significa azul - designa:
- o cianeto de iões de C = N - , um anião que consiste em um carbono átomo ligado por uma ligação tripla a um azoto átomo e transportando um negativo carga elementar ; base conjugada de cianeto de hidrogênio HC≡N, cuja solução aquosa é chamada de ácido cianídrico;
- os sais deste íon, tais como cianeto de potássio (KCN), de sódio (NaCN) ou prata (AgCN);
- as moléculas orgânicas tendo o grupo ciano -C≡N, formalmente chamadas de nitrilas .
Na linguagem cotidiana, o termo cianeto geralmente designa uma das formas envolvidas no envenenamento por cianeto : cianeto de hidrogênio gasoso, cianeto de potássio ou cianeto de sódio.
Fonte e uso
Na natureza
Os cianetos podem ser produzidos por bactérias , fungos e algas e são encontrados em muitos alimentos e plantas. Nas plantas, os cianetos são normalmente ligados às moléculas de açúcar na forma de glicosídeos cianogênicos e servem nas plantas como defesa contra os herbívoros . Raízes de mandioca ou sementes de linho contêm glicosídeos cianogênicos e muitas vezes precisam ser tratados antes do consumo (geralmente por fervura prolongada).
Os caroços das drupas , como os das cerejas ou dos damascos , geralmente contêm cianetos ou glicosídeos cianogênicos . As sementes de maçã também o contêm. As amêndoas amargas que são transformadas em óleo de amêndoa também contêm um glicosídeo cianogênico, a amigdalina .
A ingestão de 50 amêndoas amargas pode causar a morte de um ser humano por envenenamento por cianeto . Muitas enzimas hidrogenase contêm ligantes de cianeto em seus locais ativos .
Os lepidópteros da família Zygaenidae emitem um cianeto líquido quando atacados.
De acordo com a Agência Canadense de Inspeção de Alimentos, o glicosídeo cianogênico das amêndoas das frutas de caroço torna-se tóxico quando se transforma em ácido cianídrico no corpo. A dose letal de cianeto está entre 0,5 e 3 mg por quilograma de massa corporal.
Produção industrial
De amônia e metano , outros hidrocarbonetos ou monóxido de carbono , veja cianeto de hidrogênio .
O cianeto de sódio também foi produzido pela reação entre a amida de sódio e o carbono .
Os nitrilos são freqüentemente produzidos pela oxidação de hidrocarbonetos com a amônia ( por exemplo, acrilonitrila ) ou por desidratação de amidas .
Química
Química de coordenaçãoO cianeto é um ligante muito nucleofílico que forma complexos com muitos metais de transição . A alta afinidade dos metais pelo cianeto pode ser atribuída à sua carga negativa e à sua capacidade de entrar em uma ligação pi.
Estrutura de cianetos complexos- Octocianetos [M (CN) 8 ] 4- (M = Mo, W) que têm uma forma dodecaédrica;
- Hexacianidas [M (CN) 6 ] 3- (M = Ti, V, Cr, Mn, Fe, Co), que têm uma forma octaédrica ;
- Tetracianetos [M (CN) 4 ] 2- (M = Ni, Pd, Pt), que têm uma forma quadrada plana ;
- Dicianetos [M (CN) 2 ] - (M = Cu, Ag, Au), que têm uma forma linear .
Os ferrocianetos (ou hexacianoferrato II ) Fe (CN) 6 4 - são praticamente inofensivos. O ferrocianeto de sódio , de potássio e cálcio são aditivos alimentares ( anti-aglomeração ), respectivamente referenciados em E 535, E 536 e E 538. O ferrocianeto de potássio também é permitido em enologia para a ligação de vinho branco ou rosé com excesso de ferro ou cobre.
Os ferricianetos (ou hexacianoferrato III ) Fe (CN) 6 3- também tem baixa toxicidade, eles são usados em fotografia , como um agente de enfraquecimento para impressões de prata a preto e branco e, como ingrediente activo para o cianotipo e cyanographie .
O azul da Prússia é um pigmento azul escuro usado como corante, um complexo de cianeto é o ferro. É ele quem está ativo no cyanotype emulsão e cyanography . O azul da Prússia pode produzir cianeto de hidrogênio pela ação de ácidos .
Propriedades redoxO íon cianeto é um agente redutor e é oxidado por oxidantes fortes, como cloro molecular (Cl 2 ), hipoclorito (ClO - ) e peróxido de hidrogênio (H 2 O 2 ). Esses oxidantes são usados para destruir o cianeto em efluentes de minas de ouro . Os íons cúpricos (Cu 2+ ) catalisam a oxidação dos cianetos formando um intermediário complexo . O cianeto de ânions (CN - ) é primeiro oxidado a cianato ([OCN] - ) que pode então ser decomposto em amônia (NH 3 ) e, finalmente, em gás nitrogênio (N 2 ).
Cianetos orgânicosAs moléculas orgânicas com ciano -C≡N são chamadas de nitrilos .
Em síntese orgânica , os nitrilos são intermediários sintéticos para reações de homologação , ou seja, para aumentar o comprimento da cadeia de carbono em uma unidade .
Metalurgia
O cianeto é usado na mineração e na indústria para extrair o ouro e a prata . O cianeto também é usado para realizar a eletrodeposição (por eletrólise ) de certos metais (prata, ouro, cádmio, cobre, mercúrio, etc.).
segurança
Toxicidade
Os sais de cianeto são extremamente tóxicos , assim como o cianeto de hidrogênio e sua solução, o ácido cianídrico.
Os ferricianetos e ferrocianetos não são tóxicos, pois os ligantes estão fortemente ligados ao íon central, mas podem se decompor sob o efeito do ácido ou do calor e liberar cianeto de hidrogênio.
O íon cianeto se liga aos átomos de ferro contidos na hemoglobina e na citocromo oxidase ( íon Fe 2+ / Fe 3+ ). Este último é responsável pelo transporte e uso de oxigênio na cadeia respiratória mitocondrial. Deve-se notar que, se a ligação do cianeto à hemoglobina deslocar a curva de saturação da hemoglobina para a esquerda e, assim, diminuir a extração de oxigênio pelos tecidos, esse mecanismo é modesto na morte por intoxicação.
É particularmente formidável na forma de cianeto de hidrogênio , um composto volátil e muito tóxico. Este gás é formado principalmente quando os cianetos são acidificados (em solução ou pelo suco gástrico após a ingestão). Pode ser usado por suas propriedades anóxicas como arma química .
A intoxicação por cianeto pode ocorrer simplesmente durante a ingestão de certas plantas ( mandioca , mandioca, etc.) e do caroço de certas frutas . Eles contêm uma molécula de cianogênio , a amigdalina , que é decomposta no intestino em glicose , aldeído e cianeto, sob o efeito de beta-glicosidases . A própria amêndoa amarga, possuindo uma beta-glucosidase ativada pelo ar, libera aromas de cianeto de hidrogênio e benzaldeído , sendo este último que exala o odor de amêndoas amargas comumente atribuídas ao cianeto.
A amigdalina e o laetrile são erroneamente apresentados como fármacos anticâncer naturais, sem nunca terem comprovado sua eficácia in vivo , e apresentam alto risco de intoxicação por cianeto.
A combustão de certos polímeros ( poliuretanos , vinis , lã) libera cianeto de hidrogênio e pode causar envenenamento, principalmente em casos de "incêndios na cama" (pessoas fumando na cama, adormecendo, cigarros causando combustão lenta. Cobertores) onde as vítimas morrem de envenenamento antes sendo queimado. O uso de sais de cianeto na metalurgia também aumentou o risco de envenenamento.
Os cianetos, principalmente cianetos de potássio e sódio, são usados como pesticidas por essas propriedades tóxicas e podem ser desviados para usos ilegais, como a pesca com cianeto. O Zyklon B , usado pelos nazistas durante a Segunda Guerra Mundial como veneno nas câmaras de gás , contém ácido cianídrico.
Reatividade
Os íons cianeto já ligados aos íons ferrosos ( ferrocianeto ) ou férricos ( ferricianeto ) normalmente não se ligam ao ferro na hemoglobina e nos citocromos . Da mesma forma, aqueles ligados ao cobalto, por exemplo, na vitamina B12 .
Os íons de cianeto podem ser oxidados pelo oxigênio em cianatos muito menos tóxicos, que podem então se hidrolisar em dióxido de carbono e amônia . O óxido de enxofre em tiocianatos de cianetos é menos tóxico.
O grupo cianeto liga-se a um grupo alquil ou aril . No caso de nitrilos , como acetonitrila ou poliacrilonitrila , o grupo cianeto está ligado o suficiente para não atacar mais o ferro porque não há grupos que forneceriam elétrons para compensar a saída do cianeto.
No entanto, nas cianoidrinas, o oxigênio da função álcool perde facilmente seu próton ácido e o par de elétrons assim liberado pode se tornar a ligação pi do grupo carbonila (CO). O ânion cianeto sai com o par de elétrons que o ligava ao carbono carbonílico.
Antídotos
Existem os seguintes antídotos:
- nitrito de amila combinado com nitrito de sódio e tiossulfato de sódio ,
- a hidroxocobalamina , que captura o cianeto para produzir a vitamina B 12 e não é tóxica excretada na urina,
- sais de cobalto .
- EDTA dicobáltico
É necessário reagir rapidamente e, em caso de parada respiratória, respirar oxigênio e em nenhum caso praticar boca a boca, pois há risco de intoxicação ao expirar.
A ação dos antídotos de cianeto é baseada nos seguintes mecanismos:
- O nitrito de amila e o nitrito de sódio induzem a formação de metahemoglobina que se liga aos íons cianeto, ao contrário da hemoglobina nativa. Isso permite que parte do cianeto seja removido de seu alvo. Esse mecanismo de ação torna o uso desse antídoto perigoso quando há intoxicação por monóxido de carbono associada, que já diminui a proporção de hemoglobina ativa. No entanto, esta intoxicação associada é frequente (co-intoxicação por fumaça de fogo).
- O tiossulfato permite o metabolismo do cianeto em tiocianato não tóxico. Esta é uma ação mais lenta, portanto, este antídoto não é usado sozinho em um ambiente de emergência.
- A hidroxocobalamina e os sais de cobalto capturam o íon cianeto para permitir sua eliminação urinária.
Nomenclatura
- Número CAS: 151-50-8
- Folha toxicológica INRS: FT111
- Número CAS: 143-33-9
- Folha toxicológica INRS: FT111
História
- No final da Segunda Guerra Mundial, vários nazistas cometeram suicídio ingerindo uma cápsula de cianeto, em particular Richard Glücks (1889-1945), Heinrich Himmler (1900-1945), Eva Braun (1912-1945), Hermann Göring (1893-1946 ); Magda Goebbels (1901-1945) e Joseph Goebbels envenenaram seus seis filhos com cianeto e posteriormente cometeram suicídio, mas atirando na própria cabeça.
- A tentativa de envenenar Rasputin com cianeto não teve sucesso, mas não se sabe se ele recorreu à mitridatização ou se o cianeto reagiu ao assar com o açúcar do bolo em que foi colocado.
- 914 seguidores da seita Templo do Povo morreram por absorção de cianeto em um suicídio em massa em 1978.
- O 30 de janeiro de 2000Um dos piores desastres ecológicos na Europa aconteceu: o vazamento de cianeto em Baia Mare , na Romênia .
- O 12 de agosto de 2015, em Tianjin , no leste da China , duas poderosas explosões destroem um armazém contendo 700 toneladas de cianeto de sódio .
- O 29 de novembro de 2017, enquanto Slobodan Praljak , um ex-oficial croata estava sendo julgado no Tribunal Criminal Internacional para a Ex-Iugoslávia (TPIJ), acusado de crimes de guerra, ele repentinamente tirou um pequeno frasco de seu bolso após o veredicto ser proferido e engoliu seu conteúdo. Ele foi atendido rapidamente pelos serviços de emergência, mas não sobreviveu. Ele morreu algumas horas depois. A autópsia realizada em seu corpo constatou que o líquido ingerido pelo general Praljak continha cianeto.
Em romances policiais
- No romance " Le Grand Sommeil " de Raymond Chandler , um dos personagens é envenenado por cianeto misturado com uísque.
- Na série Henderson's Boys of Robert Muchamore , é usado na forma de pílula em casos de extrema emergência.
Agatha Christie
- Cianeto de potássio em pó dissolvido em champanhe é usado para cometer dois assassinatos no assassinato de Champagne .
- O primeiro e o quinto assassinato de Dez Negros são cometidos com cianeto (em champanhe para um, em uma seringa para o outro).
- O segundo assassinato em Death in the Clouds é realizado com cianeto, apenas para ser disfarçado de suicídio.
- Em The Poisonous Feather a Sra. Symmington termina sua vida engolindo cianeto destinado à jardinagem.
- Em Yellow Iris, a vítima é morta por cianeto de potássio misturado com champanhe.
Notas e referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (em) David R. Lide, Handbook of Chemistry and Physics , Boca Raton, CRC,2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205.
- Guia prático de toxicologia, F.-X. Reichl, R. Perraud, Ed. Krahé, 2004, p. 134 .
- Agência Canadense de Inspeção de Alimentos - Toxinas Naturais em Frutas e Vegetais Frescos .
- Young, CA e Jordan, TS (1995, maio). Remediação de cianeto: tecnologias atuais e passadas. In: Proceedings of the 10th Annual Conference on Hazardous Waste Research (pp. 104-129). Universidade Estadual do Kansas: Manhattan, KS. https://engg.ksu.edu/HSRC/95Proceed/young.pdf
- (in) Dmitry Yermakov, " Destruição de cianeto | SRK Consulting ” , em srk.com (acessado em 2 de março de 2021 )
- Botz Michael M. Visão geral dos métodos de tratamento com cianeto. Elbow Creek Engineering, Inc. http://www.botz.com/MEMCyanideTreatment.pdf
- Cianetação e ouro: Dissolução pela água? : um artigo explicativo publicado pela Culturesciences-Chimie École Normale Supérieure - DGESCO.
- (em) Judith E Tintinalli David Cline et al. , Medicina de Emergência do Tintinalli Manual: 7 ª edição , New York, McGraw-Hill Professional,2012, 7 th ed. , 969 p. ( ISBN 978-0-07-178184-8 , OCLC 755056524 ).
- (em) " Cianeto: uma maneira fácil e mortal de pegar peixes " no WWF ,29 de janeiro de 2003(acessado em 31 de março de 2019 )
- (em) "Death of a River" , BBC ,15 de fevereiro de 2000.
- " Tianjin: autoridades chinesas confirmam a presença de centenas de toneladas de cianeto ", Le Monde.fr ,16 de agosto de 2015( ISSN 1950-6244 , ler online , acessado em 16 de agosto de 2015 ).
- " Explosão na China: presença de cianeto de sódio altamente tóxico ", Le Point ,15 de agosto de 2015( leia online ).
Veja também
Artigos relacionados
links externos
- Folha toxicológica INRS para cianetos de sódio e potássio [PDF]
- Comunicado de imprensa da Euromines que expõe a posição do Comissário Europeu para o Ambiente, Sr. Potočnik, na sequência de uma resolução do Parlamento Europeu que preconiza uma proibição geral da utilização de tecnologias à base de cianeto na União Europeia [PDF] ; Bruxelas,1 st julho 2010,
- Código Internacional de Gerenciamento de Cianeto [PDF] (versão de 11 de janeiro de 2011, escrito e apoiado por um "grupo de empresas de mineração de ouro e produtores de cianeto em todo o mundo", e que se promove como uma "iniciativa de adesão voluntária para a indústria de mineração de ouro, produtores e transportadores de cianeto usados na mineração de ouro. Visa complementar os regulamentos existentes que são obrigatórios para qualquer empresa de mineração. O cumprimento das regras, regulamentos, regulamentos e leis das jurisdições competentes é obrigatório; este código não se destina a infringir essas leis ”; PDF, 12 p. , Consultado em 25/02/2014
Bibliografia
- Convenção sobre a Proibição do Desenvolvimento, Produção, Armazenamento e Uso de Armas Químicas e sobre Sua Destruição (consultada em 7/5/2010).
- Circular n o 700 / NWMO / PES / PPS, de 7 de Novembro de 2008 sobre a doutrina nacional de emprego dos equipamentos de emergência e cuidado face uma ação terrorista através da implementação de produtos químicos.
- Rauber C, Kupferschmidt H. (2008) Envenenamento por cianeto [PDF] Swiss Center for Toxicological Information; Janeiro de 2008 (consultado em 27/07/2010)
- INRS (2006) Cianeto de hidrogênio e soluções aquosas . Folha de dados toxicológicos FT 4, edição de 2006.
- INRS (2006) Cianeto de sódio e cianeto de potássio . Folha de dados toxicológicos FT 111, edição de 2006.
- INERIS (2006). Cianetos e derivados Folha de dados toxicológicos e ambientais de substâncias químicas. (v n o 1 de 27 de julho de 2006)
- Benaissa L, Hantson P, Laforge M, Borron S, Baud F. (1999) Cyanide and cyanogenic toxicants . na Encyclopédie Médico-Chirurgicale patologias ocupacionais e ambientais. Paris: Elsevier Masson SAS, 16-048-C-20 ,: 7 p.
- Cavallo JD, Fuilla C, Dorandeu F, Laroche P, Vidal D. (2010) CBRN-E arrisca saber para agir . Paris: edição de Xavier Montauban; 336 p.
- INRS (2004) Acetonitrila . Folha de dados toxicológicos FT 104, edição de 2004.
- INRS (2004) Acrilonitrila . Folha de dados toxicológicos FT 105, edição de 2004.
- Lgifrance Decreto n o 88-448 alterado pelo Decreto n o 95-608 relativa à protecção dos trabalhadores expostos a gases de fumigação.
- Falcy M, Malard S. (2005) Comparação dos limiares olfativos de substâncias químicas com indicadores de segurança usados no local de trabalho (ND 2221) . INRS . Higiene e segurança industrial. Cadernos documentários; 1 st trimestre de 2005; 198: 7-21.
- Renard C, Dorandeu F, Borron S, Baud F, Rüttmann M, Vest P, et al. (2003) Notícias sobre envenenamento cianídrico . Medicine and the Armies; 31 (3): 218-26.
- [Rivièrea, F., Bohanda, S., Fuillab, C., Petitc, JL, Lapostolled, F., Lamberte, Y .... & Larochea, P. (2010). Envenenamento cianídrico: pense nisso! [PDF] . medicina e exércitos, 38 (5), 387-396.