Borane
Este artigo é sobre um composto específico. Para a classe de compostos, consulte boranos .
| Borane | ||
| ||
 | ||
| Identificação | ||
|---|---|---|
| Nome IUPAC | borano | |
| Sinônimos |
boro, tri-hidreto de boro, tri-hidridoboro |
|
| N o CAS | ||
| PubChem | 6331 | |
| ChEBI | 30149 | |
| SORRISOS |
B , |
|
| InChI |
InChI: InChI = 1 / BH3 / h1H3 InChIKey: UORVGPXVDQYIDP-UHFFFAOYSA-N |
|
| Propriedades quimicas | ||
| Fórmula bruta | B H 3 | |
| Massa molar | 13,835 ± 0,007 g / mol H 21,86%, B 78,14%, |
|
| Momento dipolar | 0 D | |
| Termoquímica | ||
| S 0 gás, 1 bar | 187,88 kJ mol −1 K −1 | |
| Δ f H 0 gás | 106,69 kJ / mol | |
| Propriedades eletrônicas | ||
| 1 energia de re ionização | 12,026 ± 0,024 eV (gás) | |
| Unidades de SI e STP, salvo indicação em contrário. | ||
O borano ( nomenclatura sistemática trihydridobore ) é uma molécula instável e altamente reativa possuindo a fórmula química BH 3 .
A espécie molecular BH 3 é um ácido de Lewis muito forte. Portanto, é altamente reativo e só pode ser observado diretamente como um produto contínuo e transiente, em um sistema de fluxo ou durante a reação de boro atômico ablacionado a laser com hidrogênio.
É um gás incolor impossível de concentrar em sua forma pura. O borano é o elemento mais simples da família do borano , bem como o protótipo dos monoboranos.
Estrutura e propriedades
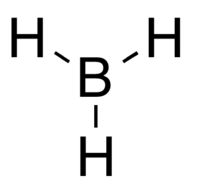
BH 3 é uma molécula trigonal planar (AX 3 E 0 ) que exibe simetria D 3h . O comprimento da ligação B - H determinado experimentalmente é 119 μm .
Na ausência de outras espécies químicas, ele reage consigo mesmo para formar diborano. É, portanto, um produto intermediário na preparação de diborano dependendo da reação:
BX 3 + BH 4 - → HBX 3 - + (BH 3 ) (X = F, Cl, Br, I) 2 BH 3 → B 2 H 6A entalpia padrão de dimerização de BH 3 é estimada em -170 kJ mol -1 . O átomo de boro em BH 3 tem seis elétrons de valência . Portanto, é um ácido de Lewis forte que reage com qualquer base de Lewis , L, para formar um aduto no qual a base doa seu único par, formando uma ligação covalente dativa .
BH 3 + L → L - BH 3Esses compostos são termodinamicamente estáveis, mas podem ser facilmente oxidados ao ar livre. Soluções contendo sulfureto de dimetilo de borano e tetra-hidrofurano de borano estão disponíveis comercialmente; no tetrahidrofurano , um agente estabilizador é adicionado para evitar que o THF oxide o borano.
O borano também é usado na prática para reduzir os ácidos carboxílicos a álcoois primários.
Notas e referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (em) David R. Lide, Handbook of Chemistry and Physics , Boca Raton, CRC,2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205.