Tetraóxido de xenônio
| Tetraóxido de xenônio | |
 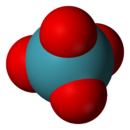 Estrutura do tetraóxido de xenônio |
|
| Identificação | |
|---|---|
| N o CAS | |
| Propriedades quimicas | |
| Fórmula bruta | XeO 4 |
| Massa molar | 195,291 ± 0,007 g / mol O 32,77%, Xe 67,23%, |
| Propriedades físicas | |
| Fusão T ° | −35,9 ° C ( explosão ) |
| Unidades de SI e STP, salvo indicação em contrário. | |
O tetróxido de xenônio é um sólido cristalino amarelo de fórmula Xeo 4que só é estável abaixo de −35,9 ° C ; acima dessa temperatura, ele se decompõe explodindo para liberar xenônio e oxigênio . Na molécula XeO 4, o xenônio está no estado de oxidação +8, enquanto o oxigênio está no estado de oxidação -2. O oxigênio é o único elemento conhecido por levar o xenônio ao seu estado de oxidação mais alto; o flúor para no estado 6 com o hexafluoreto de xenônio XeF 6, provavelmente por razões de impedimento estérico .
Propriedades químicas e síntese
O tetraóxido de xenônio explode acima de −35,9 ° C , com ΔH = -643 kJ / mol:
XeO 4 → Xe+ 2 O 2Dois outros compostos de xenônio com um estado de oxidação +8 são obtidos pela reação de tetraóxido de xenônio com hexafluoreto de xenônio XeF 6 : Xénon trioxydifluoride Xeo 3 F 2e xénon dioxytetrafluoride Xeo 2 F 4, que pode ser detectado por espectrometria de massa .
Todos os métodos de preparação começam com perxenatos , que são obtidos dos xenatos por dois métodos possíveis. O primeiro é a desproporção de dois xenatos em um perxenato e xenônio :
2 XeO 4 2−→ XeO 6 4−+ Xe+ O 2.O segundo é a oxidação de dois xenatos com ozônio :
2 XeO 4 2-+ 4 e - + 2 O 3→ 2 XeO 6 4-+ O 2.O Perxenato de bário Ba 2 Xeo 6reage com ácido sulfúrico H 2 SO 4para formar sulfato de bário BaSO 4com ácido perxênico H 4 XeO 6, que dá tetraóxido de xenônio na desidratação:
Ba 2 XeO 6+ 2 H 2 SO 4→ 2 BaSO 4+ H 4 XeO 6 H 4 XeO 6→ 2 H 2 O+ XeO 4Caso contrário, o ácido perxênico lentamente se desproporcionará em oxigênio e ácido xênico :
2 H 4 XeO 6→ O 2+ 2 H 2 XeO 4+ 2 H 2 O.Notas e referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (em) H. Selig JG Malm, HH Claassen CL Chernick, JL Huston, " Xenon tetroxide -Preparation + Some Properties " , Science , vol. 143,1964, p. 1322 ( PMID 17799234 , DOI 10.1126 / science.143.3612.1322 , ler online )
- (em) JL Huston, MH Studier, IN Sloth, " Xenon tetroxide - Mass Spectrum " , Science , vol. 143,1964, p. 1162 ( PMID 17833897 , DOI 10.1126 / science.143.3611.1161-a , leia online )