Doença de Lyme
Doença de Lyme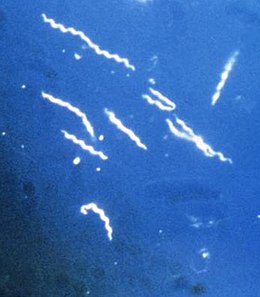 Borrelia burgdorferi , uma das três variantes conhecidas da bactéria parasita que causa a doença de Lyme. Borrelia tem uma forma característica de serpentina e espiral, daí o seu nome espiroquetas .
Borrelia burgdorferi , uma das três variantes conhecidas da bactéria parasita que causa a doença de Lyme. Borrelia tem uma forma característica de serpentina e espiral, daí o seu nome espiroquetas .
| Especialidade | Doenças infecciosas , dermatologia , neurologia e cardiologia |
|---|
| ICD - 10 | A69.2 |
|---|---|
| CIM - 9 | 088,81 |
| DiseasesDB | 1531 |
| MedlinePlus | 001319 |
| eMedicine | 330178, 965922 e 786767 |
| eMedicine | med / 1346 ped / 1331 neuro / 521 emerg / 588 |
| Malha | D008193 |
| Incubação mín. | 1 dia |
| Incubação máxima | 44 d |
| Sintomas | Eritema migratório crônico , fadiga , dor de cabeça , artralgia , mialgia , fasciculação , parestesia , vertigem , arritmia cardíaca , dor neuropática crônica ( d ) , febre , neurite , meningite , meningoencefalite ( en ) , miocardite , artrite , encefalomielite ( en ) e cardiomiopatia hipertrófica |
| Doença transmitida | Transmissão por carrapatos ( d ) , Ixodes pacificus e Ixodes scapularis |
| Causas | Borrelia burgdorferi |
| Medicamento | Ceftriaxona , cefuroxima , amoxicilina , doxiciclina e azitromicina |
| Paciente do Reino Unido | Doença de Lyme-pro |
A doença de Lyme é uma doença transmitida por um vetor e uma zoonose (doença infecciosa que afeta humanos e muitos animais). A doença de Lyme deve o seu nome às cidades de Lyme e Old Lyme , duas cidades dos Estados Unidos , no estado de Connecticut, onde foi relatada pela primeira vez em 1975 e identificada em 1977. Transmitida por picadas de agulha, carrapatos duros Ixodes é uma doença bacteriana causada por borrelia ( Borrelia burgdorferi , estritamente definida, predominante na América do Norte).
A expressão borreliose de Lyme designa frequentemente “doença de Lyme europeia”, devido a uma maior diversidade de borrelia (principalmente Borrelia garinii , B. afzelii … ou B. burgdorferi no sentido lato). A doença de Lyme e a borreliose de Lyme são freqüentemente sinônimos, devido à Borrelia burgdorferi no sentido amplo. As outras borrelioses são chamadas de febres recorrentes (cosmopolita transmitida por piolhos e regional por carrapatos moles ).
A doença é caracterizada por grande diversidade (genética, epidemiológica, clínica e diagnóstica) por ser multiorgânica (podendo acometer diversos órgãos) e multissistêmica , podendo acometer diversos sistemas com, portanto, manifestações clínicas polimórficas (cutâneas, reumatológicas e neurológicas ) Está se expandindo, tornando-se a doença transmitida por vetores mais comum transmitida aos humanos no hemisfério norte.
Em quase 90% dos casos, é efetivamente tratada com antibióticos por 2 a 4 semanas. Não tratada, pode evoluir ao longo de vários anos, passando classicamente por três estágios mais ou menos diferenciados, às vezes intercalados com períodos de latência e que podem se sobrepor para determinados sintomas. Após uma possível fase de dormência, a doença pode, de forma aguda ou crônica, assumir formas mais cutâneas, articulares ou neurológicas.
A existência e o significado de formas não curadas pelo tratamento padrão, ou a atribuição de patologias crônicas à doença de Lyme, colocam o problema da "doença de Lyme crônica", a complexidade do diagnóstico clínico, interpretação problemática de testes sorológicos, diretrizes contraditórias para o diagnóstico, tratamento e o manejo de antibióticos na doença de Lyme crônica alimenta uma controvérsia social conhecida como Guerra de Lyme nos Estados Unidos ou Escândalo de Lyme na França.
História da doença
A borreliose existe há muito tempo:
- de acordo com os restos de DNA bacteriano encontrados em seu cadáver, o primeiro humano conhecido a ter sido infectado com Borrelia burgdorferi é Ötzi , cerca de 5.300 anos atrás;
- a história evolutiva de B. burgdorferi na América do Norte foi reconstruída, sugerindo sua presença por pelo menos 60.000 anos, muito antes de os humanos chegarem às Américas;
- várias linhas muito antigas e amplamente distribuídas (incluindo na América do Norte) encontraram recentemente as condições para o desenvolvimento de epidemia (Walter et al. , 2017); sua diversidade e ampla distribuição refuta a hipótese de uma emergência ligada a modificações genéticas recentes (até mesmo à manipulação genética (em 2019, discussões estão em andamento nos Estados Unidos para saber se a doença de Lyme foi usada como arma biológica).); a emergência da doença de Lyme é, sem dúvida, o resultado de distúrbios antropogênicos dos ecossistemas e do clima que têm favorecido surtos de carrapatos e / ou bactérias e um número crescente de infecções humanas;
- a doença leva o nome da cidade de Lyme ( Connecticut ) onde foi relatado em 1975 ter sido identificada como resultado de uma picada de carrapato em 1977. Mas a maioria de suas manifestações já havia sido descrita na Europa, no final do século XIX th século, mas pouco.
Primeiras descrições na Europa
- Em 1883 , um médico alemão, Alfred Buchwald, descreveu (em Breslau ) uma anormalidade da pele que parece ser o que hoje é chamado de acrodermatite atrófica crônica , mas Buchwald não a vinculou a uma picada de carrapato, e este sintoma não estará presente em Lyme (onde a borrelia dominante é diferente das encontradas na Eurásia);
- Em 1909 , Arvid Afzelius (dermatologista sueco) notou o aparecimento de outra lesão cutânea em forma de anel, às vezes após uma picada de carrapato Ixodes , e que ele chamou de eritema migrans . Em 1913, Bruce Lipschutz (dermatologista austríaco) chamou de eritema migrante crônico.
- Em 1922 , os médicos franceses Garin e Bujadoux associavam esta lesão dermatológica a um ataque mais geral de paralisia "mais ou menos grave, às vezes fatal, após picada de carrapato" ( Ixodes hexagonus ). Os dois franceses atribuem essa meningoradiculite linfocítica (às vezes associando meningite e polineurite ) a um "vírus" que deve ser procurado não no sangue, mas no tecido nervoso.
- Em 1934 , na Alemanha, o eritema migrans foi descrito em associação com lesão articular.
- Em 1941 , o alemão Alfred Bannwarth (des) associou o dano articular à meningo-radiculite do tipo linfocítico ( síndrome de Bannwarth então às vezes rebatizada de síndrome de Garin-Boujadoux-Bannwarth ).
- Em 1951 , os efeitos benéficos da penicilina nessas condições sugerem uma origem bacteriana.
Redescoberto nos Estados Unidos
Em 1969 , foi publicado nos Estados Unidos o primeiro caso documentado de eritema crônico de migrante, ocorrido em um caçador na floresta.
Em 1975 , duas mães na cidade de Lyme com crianças diagnosticadas com artrite reumatóide juvenil observaram que muitas outras crianças na cidade tinham problemas semelhantes. Alertada, uma equipe de epidemiologistas da Universidade de Yale , liderada por Allen Steere, rapidamente destacou uma situação atípica:
- a prevalência de oligoartrite nessa comuna era cem vezes maior do que a da artrite reumatóide juvenil nos Estados Unidos;
- os novos casos eram mais numerosos no verão e claramente divididos em focos geográficos;
- 25% dos pacientes apresentaram associação com eritema crônico.
Allen Steere (em) chamou então a doença de "doença ou artrite de Lyme" o nome da cidade, atribuindo-a a uma transmissão por carrapato em um artigo publicado em 1977.
De carrapatos a bactérias
Em 1977 , a picada do carrapato Ixodes dammini (agora Ixodes scapularis ) foi relatada em um caso humano de eritema migrante crônico.
Em 1982 , Willy Burgdorfer isolou a bactéria espiroqueta responsável pela doença no trato digestivo de I. scapularis , conhecido como “carrapato de cervo” na América do Norte. Após a inoculação no coelho, mostra que esta espiroqueta pode causar eritema migrans. Ele também observou uma forte reação entre o soro dos pacientes e a bactéria. É em sua homenagem que esta bactéria receberá o nome de Borrelia burgdorferi em 1984 . Ao mesmo tempo, espiroquetas idênticas ou semelhantes foram detectadas na Europa (Suíça), em carrapatos Ixodes ricinus .
A responsabilidade desta espiroqueta será confirmada isolando-a do sangue, da pele e do líquido cefalorraquidiano de pacientes com doença de Lyme.
Em 1984, o dermatologista alemão Klaus Weber demonstrou aumento de anticorpos do tipo IgG no sangue de pacientes com acrodermatite atrófica crônica , estabelecendo assim uma primeira relação entre as manifestações precoces e tardias da doença.
Etiologia
Agentes
Ainda são bactérias do gênero Borrelia , classificadas entre os espiroquetas por seu caráter serpentiforme e espiral.
Borrelia burgdorferi sl ( sensu lato) designa um “complexo” de cerca de 30 espécies, várias das quais são patogênicas para o homem. Os três principais são: Borrelia burgdorferi ss ( sensu stricto ), B. garinii , B. afzelii . No início do XXI th métodos de século genética molecular (tipagem molecular de bactérias) foram usados para detectar novas espécies patogénicas para os humanos: como B. spielmanii ou B. bavariensis Eurásia, ou B. bissettii Eurásia, América, Austrália .
Também foi demonstrado (em 2016) que certas cepas da mesma espécie de Borrelia são mais patogênicas para humanos do que outras.
Qualquer que seja a espécie de Borrelia envolvida, o ataque inicial pode se manifestar (às vezes) por eritema migrans; caso contrário, as evoluções diferem. As associações não são absolutas, mas preferenciais, explicando em parte a predominância geográfica de certas formas complicadas da doença.
- Na América do Norte , B. burgdorferi ss ( sensu stricto ) predomina quase exclusivamente, causando principalmente artrite de Lyme e dor reumática (mas sempre sem acrodermatite ).
- Na Eurásia , B. burgdorferi ss é mais rara, enquanto B. burgdorferi sl ( sensus lato ) predomina, visando também outros órgãos. Na Europa, os dois agentes mais comuns são Borrelia garinii que causa principalmente danos neurológicos ou "neuroborreliose" e Borrelia afzelii , que causa principalmente danos cutâneos, em particular acrodermatite atrófica crónica . O tipo de bactéria pode variar no espaço e no tempo, mas, por exemplo, uma análise de genospecia foi feita em 710 carrapatos retirados de janeiro a dezembro de 2009 da pele de soldados alemães treinando na área de Seedorf (noroeste da Alemanha): 84% de borrelia eram da espécie B. afzelii , 11% eram B. burgdorferi , 3% eram B. garinii e 3% eram B. spielmanii (nota: 99,2% dos carrapatos eram I. ricinus , 0,7% eram I. hexagonus e 0,1% H . concinna ).
Vetores
CarrapatosOs vetores são principalmente carrapatos do gênero Ixodes . Esses vetores principais têm em comum o fato de terem um ciclo de transmissão com três hospedeiros sucessivos, em floresta ou prados úmidos, de 2 a 7 anos dependendo da espécie e do clima. Na América do Norte, o principal vetor é Ixodes scapularis [ = I. dammini ], no Nordeste e no Centro-Oeste. Todos os estágios, especialmente ninfas e fêmeas adultas, podem morder humanos. Ixodes pacificus , a fonte de cerca de 5% dos casos relatados nos Estados Unidos, é encontrado no oeste. Sua eficácia patogênica em humanos é mais baixa (apenas o estágio adulto pica em humanos).
Na Eurásia e especialmente na Europa, o principal vetor é o Ixodes ricinus . É predominante em regiões arborizadas, picando humanos em todas as fases (larvas e ninfas na primavera, adultos no final do verão).
Na Eurásia temperada e fria, especialmente na Ásia e na maior parte da ex-URSS , o principal vetor é o Ixodes persulcatus .
Certos artrópodes sugadores de sangue , como mutucas , mosquitos, etc. , podem ser vetores potenciais de Lyme. Este possível papel do vetor acessório está em discussão.
Relações entre carrapatos e borreliaA proporção de carrapatos infectados varia muito dependendo do estágio de desenvolvimento, espécies, estações e regiões: menos de 2% de I. pacificus na Califórnia, até 30% dos carrapatos infectados na França, 60% na Áustria e 100% na Long Island .
Na França, um estudo realizado em 2021 pelo INRAE mostra que 15% dos carrapatos que picam humanos são portadores da bactéria Borrelia bugdorferi sensu lato .
A bactéria desenvolve-se em duas fases: multiplica-se primeiro no intestino médio da larva , nesta fase a bactéria é " imóvel ", ou seja, incapaz de se mover sozinha. Então, em uma segunda fase, sob o efeito do repasto sanguíneo (de um primeiro pequeno roedor hospedeiro), a bactéria torna-se móvel e capaz de penetrar na hemocele do carrapato e atingir as "glândulas salivares" do carrapato. Ninfa ou carrapato adulto.
De lá, ele passa para a saliva e é injetado nos seguintes hospedeiros (mamífero, ave, réptil ...). Isso explica por que geralmente é pela picada de uma ninfa do carrapato, e não pela picada de uma larva, que a bactéria é transmitida aos grandes mamíferos.
Excepcionalmente, a bactéria também pode se espalhar para os ovários do carrapato, o que dá origem à chamada transmissão transovariana “vertical”, em que o carrapato transmite a bactéria diretamente para sua prole. Isso explica porque, nesses casos, uma larva de carrapato pode ser infecciosa, antes mesmo de ter feito uma refeição de sangue.
Em 2017, o INRA lançou um projeto de ciência cidadã para melhor conhecimento dos vetores da doença de Lyme, no âmbito do plano nacional de controlo da doença de Lyme. Um aplicativo para smartphone permite que todos os cidadãos relatem picadas de carrapatos, e eles são convidados a enviar carrapatos a laboratórios para analisar e conhecer melhor a distribuição de espécies de vetores e Borrelia.
Reservatórios
O reservatório de borrelia consiste em pequenos roedores, principais carrapatos hospedeiros na fase de larvas ou pupas. Nesse estágio inicial, as larvas e pupas se alimentam primeiro da mesma espécie de pequeno roedor. No início do verão, as ninfas infectadas infectam seu hospedeiro e, no final do verão, o hospedeiro infectado infecta as larvas. A larva infectada muda , pupa e o ciclo começa novamente no ano seguinte. Este ciclo inicial é essencial para a manutenção da borrelia na natureza.
À medida que continuam a se desenvolver (da ninfa ao adulto), os carrapatos contaminados transmitem a bactéria a outros hospedeiros (roedores, grandes mamíferos, pássaros, às vezes répteis). Nesse ponto, os carrapatos se reproduzem e o ciclo começa novamente. Esta parte do ciclo é essencial para a manutenção dos carrapatos, mas não para a borrelia .
As espécies que desempenham um papel real de reservatório podem variar entre países e regiões. Na Europa, mais de 300 espécies foram identificadas desta forma: principalmente pequenos roedores, mas também mamíferos de médio porte (raposa, lebre, etc.) ou mamíferos de grande porte como veados ou mesmo pássaros. Estas espécies de reservatório são aquelas de animais selvagens que vivem em áreas arborizadas, vegetação rasteira, prados, úmidos e temperados ... em contato regular e permanente com o habitat habitual dos carrapatos. Os ciclos europeus parecem mais complexos e variados do que na América.
Na América do Norte, ao contrário da Europa, as espécies de reservatório predominantes se destacam com mais clareza. Por exemplo, no Nordeste e no Centro-Oeste: o camundongo-de-pés-brancos e o veado-de-cauda-branca . Aves migratórias podem desempenhar um papel importante na disseminação de carrapatos no Canadá.
Animais domésticos também podem ser infectados, em particular cães, ovelhas, bovinos e cavalos, que podem apresentar danos nas articulações (cavalos) ou nos rins (cães), ao contrário das espécies selvagens com infecções invisíveis.
O humano que entra neste ciclo, expondo-se aos carrapatos, é na verdade um hospedeiro terminal acidental de carrapatos.
Coinfecções
Um único carrapato pode injetar até cinco patógenos diferentes em seu hospedeiro, juntos ou de forma retardada, a coinfecção com várias espécies de Borrelia em carrapatos parecendo ser a regra, e não a exceção.
Assim, as possíveis coinfecções transmitidas por carrapatos aos humanos são:
- nos Estados Unidos , o carrapato Ixodes scapularis frequentemente também transmite Anaplasma phagocytophilum (agente da erliquiose humana ) e, menos frequentemente, Babesia microti (agente da babesiose ), Borrelia miyamotoi , Borrelia mayonii (agentes da febre recorrente transmitida por carrapatos).
- na Europa , o carrapato Ixodes Ricinus também pode transmitir Anaplasma phagocytophilum e Babesia microti, agente da babesiose, e também encefalite por carrapato (causada por um vírus);
- na Ásia , também são descritas coinfecções.
Agentes conhecidos diferentes de Borrelia causam geralmente sintomas inespecíficos (dor de cabeça, dores nas articulações e musculares, fadiga, etc.) e febre mais alta do que na doença de Lyme.
O impacto real na saúde de outros patógenos potenciais que constituiriam um “patobioma” do carrapato ainda é pouco compreendido. De acordo com Johnson et al. (2014), as coinfecções poderiam, pelo menos parcialmente, explicar a variabilidade da gravidade e das manifestações clínicas, por vezes crônicas, observadas na expressão da doença de Lyme;
Métodos de contaminação
Picadas de carrapato
Os humanos são contaminados quando encontram carrapatos vetores (contaminados), que são encontrados principalmente em áreas úmidas de floresta com vegetação rasteira; da primavera ao início do outono. Eles estão localizados no tapete vegetal a menos de um metro de altura.
Eles caçam "à espreita", detectando a presença de um hospedeiro próximo usando sensores sensíveis a CO 2 , calor e substâncias bioquímicas ( órgão de Haller ).
Uma vez no corpo do hospedeiro, o carrapato procura áreas quentes e úmidas como as dobras do corpo: nos humanos, dobra do cotovelo ou joelho, axila, virilha ... Pode passar por baixo da roupa e chegar à pele onde está fixado por sua tribuna para fazer sua refeição de sangue.
Essa refeição de sangue dura de 3 a 5 dias. A transmissão ocorre durante a refeição, pela passagem de bactérias do trato digestivo do carrapato para suas glândulas salivares. Saliva e bactérias são inoculadas na epiderme , não diretamente em um vaso sanguíneo. Essa progressão não começa até depois da picada do carrapato, leva várias horas para que se torne contaminante. Além disso, um carrapato que é removido rapidamente não transmite doenças.
O risco de desenvolver a doença de Lyme após uma picada de carrapato é da ordem de 1 a 5%. Apenas um terço dos pacientes com doença de Lyme conhece ou lembra de uma picada de carrapato.
Outras
A transmissão direta de mãe para filho no útero é possível quando a mãe é infectada durante a gravidez. A doença não tem efeito sobre o feto se a mãe for tratada com antibióticos apropriados.
Os outros modos de transmissão não foram demonstrados: de pessoa para pessoa (tocando, beijando ou fazendo sexo), por ar, água, comida, amamentação, transfusão de sangue, etc.
Não há risco de contaminação direta de um animal infectado.
O CDC dos EUA recomenda que os pacientes de Lyme com infecção ativa durante a antibioticoterapia não doem sangue, pois aqueles que concluíram o tratamento podem ser doadores. Na França, a atitude é semelhante (adiamento temporário).
Epidemiologia
Dados atuais
PrevalênciaA doença de Lyme existe em todos os continentes, mas é predominante na zona temperada do hemisfério norte, onde é o principal vetor da doença (incluindo na Europa). A doença afeta mais crianças pequenas e maiores de 45 anos, com um pico de frequência correspondente à atividade do carrapato (início da primavera ao final do outono). As áreas do norte e de grande altitude são cada vez mais afetadas, sem dúvida porque estão aquecendo .
Nos Estados Unidos , quase 30.000 casos são notificados ao CDC a cada ano , 95% dos quais em 14 estados do nordeste e centro - oeste , mas estudos estimam que o número de casos diagnosticados seja da ordem de 300.000, com a mesma distribuição geográfica . A prevalência da doença também está aumentando no Canadá , notavelmente demonstrada por monitoramento sorológico em cães; em 2019, estimou-se que cerca de um terço dos casos foram notificados em áreas de emergência da doença no Canadá.
Na Europa , sua incidência aumenta com um gradiente sul-norte e oeste-leste, geralmente entre uma latitude de 35 ° Norte e 60 ° Norte, e abaixo de uma altitude de 1300 m . Estima-se em 65.000 casos por ano, distribuídos de forma heterogênea, com máximo na Eslovênia e na Áustria com mais de 100 casos por 100.000 habitantes.
Na Bélgica , de 2000 a 2016, em média 200 a 300 pessoas foram hospitalizadas por ano por esta doença; quase 10.000 consultam um clínico geral para o eritema migratório .
Na Suíça , haveria 200 a 600 consultas por ano para novos casos da doença de Lyme (estimativa para 2008-2018).
Na França , em 2005 , foram estimados 43 casos por 100.000 habitantes. Essa taxa subiu para 84 [70-98] casos por 100.000 habitantes em 2016 , mas com incidência variando muito dependendo da região: a doença parece excepcional na orla do Mediterrâneo (clima muito seco para o vetor), mas chega a mais de 100 casos por 100.000 habitantes no Leste e Limousin e pode exceder 200 casos por 100.000 habitantes em certas regiões de acordo com a rede Sentinelles em 2018.
Atividades arriscadasCaminhadas na floresta, camping, jardinagem, atividades naturalizadas, caça, trabalhos agrícolas e principalmente florestais expõem as pessoas à doença:
- de 2.975 trabalhadores agrícolas e florestais testados no leste da França no início dos anos 2000, 14,1% já haviam tido pelo menos um contato com borreliose de Lyme e 3,4% com o vírus da encefalite . Idade, ocupação e local de residência influenciaram significativamente a sua condição de HIV: 17,5% dos madeireiros eram HIV positivos. A soroprevalência na Alsácia (26,9%) e Lorena (16,5%) foi significativamente maior do que nas outras regiões; Da mesma forma, a soroprevalência do vírus da encefalite transmitida por carrapatos foi maior na Alsácia (5,5%), mas as taxas de soroprevalência para essas duas infecções variaram de acordo com as áreas de floresta.
- De 310 engenheiros florestais belgas (estudo de 2018), 21,6% eram soropositivos para a doença de Lyme. Aqueles que estavam mais frequentemente nas florestas ou que relataram mais de 100 picadas foram os mais afetados. A intensidade das picadas e o uso de medidas de proteção reduziram a taxa de seroprevalência, enquanto a quantidade de sombra das árvores no solo a aumentou.
- Entre 181 guardas florestais italianos na região de Friuli-Venezia Giulia (extremo nordeste da Itália), no início dos anos 2000, a prevalência sorológica da borreliose de Lyme era de 23,2% (em comparação com 0,6% para o vírus da encefalopatia transmitida por carrapatos e 0,6% para erliquiose ). Trabalhos no sopé e jardinagem no nordeste da região e um histórico múltiplo de picadas de carrapatos aumentaram o risco da doença de Lyme. Esses dados defendem um fator de eco- paisagem ( ecoepidemiológico ).
Nota: Os fatores de risco foram semelhantes para borreliose de Lyme diagnosticada por teste de Western blot ou com base na história clínica.
Síntese epidemiológica
A epidemiologia da doença de Lyme é a de uma zoonose "com focos naturais", ou seja, cuja distribuição é irregular com zonas endêmicas localizadas, separadas por zonas mais ou menos livres (à escala nacional - diferenças regionais - como em escala regional - diferenças locais -, etc. ).
Este zoneamento varia no tempo e no espaço, dependendo das condições climáticas e ecológicas, da estação, do número e movimento dos hospedeiros (pássaros e grandes mamíferos em particular ...) portadores de carrapatos e / ou borrelia.
A progressão da doença desde a década de 1970 resulta principalmente do aumento da incidência e da extensão das áreas afetadas, e menos de uma melhoria na detecção e vigilância.
Fatores de emergência
O aumento da prevalência desta doença pode ser decorrente da evolução genética de agentes, vetores e hospedeiros, em relação às mudanças nos ecossistemas.
O aquecimento global resulta em temperaturas mínimas mais altas (noite e inverno) e primaveras mais cedo, o que provavelmente afeta a distribuição local dos carrapatos, sua densidade populacional e taxa de sobrevivência.
Além deste fenômeno global, existem silvicultura e desenvolvimento agrícola: drenagem , floresta e paisagem fragmentação , corte raso , reflorestamento , etc. Essas atividades humanas podem perturbar a dinâmica das populações faunísticas e os equilíbrios sylvocynégétique .
Esses processos reduzem a biodiversidade , considerada um elemento estabilizador. Eles se manifestam por um aumento na densidade de vertebrados domésticos e selvagens (hospedeiros reservatórios competentes) com um declínio em seus grandes predadores.
América do NortePor exemplo, na América, veados de pés brancos e ratos de pés brancos (hospedeiros primários para carrapatos do vetor Lyme) experimentaram rápido aumento na densidade.
No Nordeste, o XVII º século para o início do XIX ° século, os colonos apuradas vastas extensões de florestas para atividades agrícolas com um virtual desaparecimento de veados e seus predadores. No final do XIX th século, a região foi industrializados e agricultura declina; terras abandonadas são reflorestadas, habitat favorável à multiplicação do veado-de-cauda-branca. Durante o XX th século, esse reflorestamento é acompanhada por um desenvolvimento residencial suburbana na área arborizada. As condições estão então maduras para uma maior proximidade permanente camundongos-veados-carrapatos-humanos.
EuropaNa Europa, como na América do Norte, o aumento da presença humana na floresta ou na orla da floresta (habitat periurbano, caça ou atividades de lazer, etc.) aumenta a possibilidade de contato entre carrapatos, humanos e seus animais domésticos. (cachorro, cavalo ...).
O contexto de guerra e guerra civil também pode favorecer esse tipo de zoonose; assim, na Sérvia , logo após o início das guerras conhecidas como Guerras da Iugoslávia , notou-se um forte aumento nos casos de borreliose de Lyme.
A globalização , o comércio internacional e o turismo também desempenham um papel importante na distribuição geográfica de hospedeiros e parasitas. Por exemplo, na França, um novo animal de estimação , o esquilo coreano ou esquilo siberiano , lançado na natureza por seus proprietários, era suspeito de ser um novo hospedeiro reservatório porque se adaptou rapidamente: uma das maiores populações de esquilos (entre dez e vinte mil indivíduos) é, portanto, encontrada na floresta de Sénart .
Fisiopatologia
Reações imunológicas
Após a inoculação, exceto no caso de alergia à saliva do carrapato, há pouca reação inflamatória imediata, porque a borrelia pode modificar seus antígenos de superfície, proteínas da superfície externa ou Osp (AF), e escapar das primeiras defesas imunológicas. Se não forem tratados, eles se difundem localmente na pele a partir do local da inoculação ( eritema migrans ).
Eles então se difundem através do sangue para os tecidos articulares, neurológicos e cardíacos. No sujeito imunocompetente , após várias semanas ou meses, as respostas de anticorpos geralmente controlam a infecção disseminada, mesmo sem tratamento, e os sintomas diminuem.
Em espécies reservatório de borrelia, como camundongos, as infecções não parecem ser patogênicas, apesar da persistência da bactéria ao longo da vida, sugerindo que o sistema imunológico de alguns hospedeiros selvagens co-evoluiu com a bactéria para "tolerá-la".
Os humanos não são hospedeiros reservatórios naturais; seu sistema imunológico permanece ativado até que a bactéria seja eliminada (a bactéria pode persistir por muito tempo em locais localizados em vários tecidos). Essa persistência e seu significado médico em vários tecidos são discutidos. Não tratada, a bactéria foi demonstrada anos após a inoculação, especialmente em lesões cutâneas tardias ( acrodermatite atrófica crônica ou ACA).
Foi recentemente (2019) confirmado que em alguns casos, mesmo após um tratamento antibiótico intenso e de longo prazo, a bactéria pode persistir por muito tempo no corpo, em vários órgãos (por exemplo , cérebro , coração , rins e fígado ), no forma de agregados (do tipo biofilme ) protegidos do sistema imunológico por alginato .
Essa persistência também é observada no modelo animal ( in vivo , em camundongos imunocompetentes , cães e primatas não humanos nos quais foi encontrada uma forma de B. burgdorferi que sobreviveu ao tratamento com antibióticos).
Em macacos e rhesus e em camundongos infectados voluntariamente, recentemente demonstramos claramente essa persistência de Borrelia viva e metabolicamente ativa, após um tratamento com antibióticos que supostamente os erradicou.
Estudos em humanos também forneceram evidências clínicas da existência de uma forma crônica da doença de Lyme que pode ser explicada por infecção espiroqueta persistente, por exemplo, 3 meses após o tratamento para paralisia facial , em tendões., Em um caso de artrite de Lyme crônica ou em pacientes cujos sintomas persistiram após o tratamento com antibióticos.
Em humanos, a infecção não cria imunidade protetora, mesmo se os anticorpos ainda estiverem presentes.
História natural da doença
Classicamente, a doença evolui em três fases, não obrigatórias. Cada fase pode ser reveladora ou se enredar em outra, com surtos ou remissões em cada fase. Além das variações de acordo com as áreas geográficas (América e Eurásia), a doença também é variável de acordo com os pacientes (alguns apresentam apenas a fase primária, outros a fase terciária).
A fase primária, ou fase inicial localizada, que ocorre 3 a 30 dias após a inoculação, é uma fase cutânea, representada pelo eritema migrante. Em 20 a 30% dos casos, está ausente ou passa despercebido.
A fase secundária, ou disseminada precocemente, se manifesta nas semanas ou meses após a inoculação. Pode ser revelador (apareça primeiro). Dependendo do caso (germe causal relacionado à área geográfica), os distúrbios podem ser neurológicos, articulares, cardíacos ou cutâneos.
Essas duas primeiras fases às vezes são agrupadas em uma única fase chamada de precoce, especialmente na Europa, porque os distúrbios são diversos (maior variedade de borrelia). A doença de Lyme se apresenta como um todo polimórfico (doenças aparentemente diferentes). Já na América do Norte, a doença de Lyme se apresenta mais de forma articular, única ou predominante.
A fase terciária ocorre meses ou anos após a inoculação. É um sinal de infecção persistente ou ressurgente, mas também pode ser revelador. Essas formas tardias são reconhecidas quando formam conjuntos típicos e coerentes do ponto de vista clínico e biológico. Eles são discutidos ou controversos quando a clínica não é característica e a biologia não é validada.
Formas clínicas
A existência e a importância das formas assintomáticas estão em discussão. Sua frequência seria da ordem de 5% de soropositivos em áreas endêmicas e até 20% em populações de risco (trabalhadores florestais). Esses casos assintomáticos indicariam um contato antigo com a bactéria ou uma infecção antiga que foi curada.
Fase primária
É uma fase precoce e local, produzindo o eritema migrans característico, mas não sistemático. Corresponde a uma infecção cutânea inicial, localizada ao redor do ponto da picada.
Esta lesão aparece 3 a 30 dias depois. É mais freqüentemente encontrado nos membros inferiores ou na parte inferior do tronco; mais raramente na cabeça (crianças pequenas).
É um eritema anular com borda ativa que se estende de forma centrífuga, enquanto o centro se esclarece com uma pequena mancha vermelha central (sequela da picada do carrapato). O diâmetro inicial do anel é de alguns cm, depois chega a 15 cm em média, podendo ultrapassar 20 cm (foi publicado um caso de 70 cm).
Este eritema migrans pode ter algumas diferenças entre sua forma americana e europeia.
Forma europeiaA lesão é única, ligeiramente quente, mas indolor e sem coceira. Na Europa, onde a doença é mais frequentemente causada por B. afzelii ou B. garinii , a inflamação geralmente é menos intensa nesse estágio do que na América do Norte, e o crescimento (migração) do eritema costuma ser mais lento.
Esse eritema migrante costuma ser isolado, sem febre, sem síndrome inflamatória. Mais raramente, pode haver sinais de disseminação precoce com febre, dor e distúrbios neurológicos.
Forma americanaFreqüentemente, é feito de lesões múltiplas. A parte central permanece vermelha ou escura e torna-se mais endurecida . Sua borda externa também permanece vermelha, mas mais raramente, a porção da pele entre o centro e a borda retorna à cor normal. Às vezes, uma necrose central ou uma vesícula aparece no local da picada, possivelmente com coceira intensa e persistente, se a doença não tiver sido tratada precocemente.
Mais frequentemente do que na Europa, pode haver sinais de disseminação precoce com febre, dor e distúrbios neurológicos.
Quando os aspectos característicos dessas duas formas estão presentes, o eritema migrans é praticamente patognomônico , sendo suficiente por si só para o diagnóstico.
Esse eritema migrante se resolve espontaneamente em 4 a 6 semanas. Com o tratamento precoce, a evolução é mais rápida: a lesão desaparece em menos de uma semana e a doença não progride para formas mais complicadas.
Fase secundária
Na maioria das vezes ocorre algumas semanas a alguns meses após a inoculação, quando a lesão inicial permaneceu ausente ou passou despercebida, ou sem terapia antibiótica adequada.
Esta etapa corresponde à disseminação bacteriana, seguida pelo foco em tecidos específicos.
As manifestações são dominadas na Europa por distúrbios neurológicos ("neuroborreliose") e na América por distúrbios reumatológicos ("artrite de Lyme"). Mais raramente, doenças cardíacas, cutâneas e oculares são encontradas.
Se a fase primária estiver ausente (revelando a fase secundária), o diagnóstico pode ser confirmado pela combinação de argumentos clínicos, epidemiológicos e biológicos (nesta fase, a infecção ativa é geralmente detectável no líquido cefalorraquidiano e em testes sorológicos. Relevante, melhor do que em fase três).
NeuroborrelioseA incidência dessas neuroborreliose (formas neurológicas da doença de Lyme) varia de acordo com o país e a região. Na Europa, mais de 15% das neuroborrelioses são encontradas entre as doenças de Lyme, enquanto nos Estados Unidos essa proporção não ultrapassa 8%.
Na Europa, também varia por região, por 100.000 habitantes: Dinamarca 0,5 caso, Suécia 1 caso, Alemanha 3 casos, Alsácia 10 casos.
As formas mais frequentes (70 a 80% das neuroborrelioses) são a meningoradiculite ( polineurite com infecção do líquido cefalorraquidiano ). Eles aparecem após 3 semanas a mais de 3 meses após a picada do carrapato.
Em primeiro lugar, trata-se de distúrbios sensoriais, mais frequentemente do que motores, na área do eritema migratório. As dores são intensas (ardor, lacrimejamento), frequentemente recrudescimento noturno e causando insônia. Essas dores nem sempre têm um caminho de raiz estrito. Pode haver dano associado aos nervos cranianos , manifestado principalmente por paralisia facial periférica , bilateral em um terço dos casos.
A neuroborreliose é a causa mais comum de paralisia facial periférica em crianças.
Mais raramente, em 0,5 a 8% dos casos, podemos encontrar meningite aguda , mielite aguda , encefalite aguda .
Nessas manifestações neurológicas agudas ou subagudas, o diagnóstico é feito pelo estudo do líquido cefalorraquidiano ( LCR ). A punção lombar para confirmar meningite linfocítica . A sorologia LCS está associada à pesquisa de síntese intratecal de anticorpos específicos.
Em crianças com paralisia facial periférica, a sorologia sanguínea positiva é considerada suficiente para confirmar o diagnóstico e prescrever antibioticoterapia.
A radiculite hiperalgésica é resistente aos analgésicos usuais. Eles podem desaparecer espontaneamente em algumas semanas ou meses. Eles cederam mais rapidamente em poucos dias com antibioticoterapia apropriada.
Artrite de LymeAs manifestações articulares estiveram na origem da redescoberta da doença nos Estados Unidos, onde são mais frequentes (60% dos pacientes) do que na Europa (10 a 15%). Pode ser visto em qualquer idade, mas com mais freqüência em crianças.
Na Europa, eles são precoces (alguns dias a algumas semanas após a inoculação) e na maioria das vezes cicatrizam espontaneamente. Na América, eles são mais tardios (6 meses em média até 2 anos), para se tornarem mais frequentemente crônicos, carregando o quadro da artrite de Lyme. Na Europa, os distúrbios articulares são classificados como fase secundária, enquanto na América pertencem à fase terciária.
Em sua forma mais típica, a artrite de Lyme afeta uma única grande articulação (mono ou oligoartrite), com dor e derrame de líquido sinovial , especialmente no joelho (menos freqüentemente ombro, cotovelo, etc.). Este ataque é assimétrico, recorrente (com recidivas e remissões), às vezes permanente e provavelmente durará vários anos na ausência de tratamento.
A maioria dos pacientes se recupera com antibioticoterapia apropriada, mas alguns retêm sinovite pós-infecciosa, refratária aos antibióticos.
Outros eventosCom exceção da astenia acentuada, os distúrbios gerais são raros. Em particular, geralmente não há febre na doença de Lyme.
Em menos de 5% dos casos, pode haver distúrbios cardíacos decorrentes do bloqueio atrioventricular , manifestados por palpitações intermitentes ou desconforto. Esses últimos distúrbios são espontaneamente regressivos e muito raramente requerem a colocação de um marca- passo permanente. A pericardite prolongada é possível. A doença de Lyme deve ser testada sistematicamente em qualquer paciente jovem com bloqueio atrioventricular paroxístico inexplicado.
Na mesma proporção, podemos encontrar uma manifestação chamada linfocitoma borreliano. É um nódulo vermelho-arroxeado, de 1 a 2 cm , que se localiza mais freqüentemente na face, no lóbulo da orelha, na aréola mamária ou no escroto .
Em 1% dos casos, existem vários distúrbios oftalmológicos: conjuntivite , uveíte , ceratite, etc.
Fase terciária
A linha entre as formas secundária e terciária é difícil de estabelecer. Uma forma secundária continua a se tornar terciária, ou manifestações terciárias aparecem, aparentemente primitivas, anos após a infecção.
Fenômenos autoimunes poderiam explicar esses sintomas, mas a responsabilidade direta da bactéria durante essas manifestações tardias permanece debatida.
São as formas crônicas: cutâneas, articulares ou neurológicas. Do ponto de vista clínico, dificilmente são específicos (também podem ser encontrados à parte da doença de Lyme), com exceção da acrodermatite atrófica crônica.
Formas de peleA acrodermatite atrófica crônica , ou ACA, anteriormente também chamada de "doença de Pick-Herxheimer", está ligada de alguma forma à doença de Lyme: o germe foi isolado na biópsia da lesão. Este é o sintoma mais óbvio desta terceira fase, mas é visto principalmente apenas na Europa e não em todos os pacientes.
ACA começa com uma mudança na cor e textura da superfície da pele, geralmente em uma área exposta ao sol dos membros superiores ou inferiores. A atrofia resulta em superfícies da pele que se tornam muito finas e transparentes, assumindo uma aparência que lembra papel de cigarro amassado e uma cor vermelha a arroxeada, às vezes com a aparência de certos líquenes achatados . O ACA inicialmente localizado pode então se espalhar gradualmente e às vezes se tornar bilateral.
Formas reumatológicasÉ uma artrite de Lyme (ver seção fase secundária) que persiste e é prolongada por ser refratária à terapia com antibióticos.
Formas neurológicas"Neuroborreliose tardia" inclui várias entidades, incluindo encefalite (dano cerebral) e polineuropatias (dano aos nervos). Eles aparecem mais de 6 meses após a picada do carrapato.
A encefalite ou encefalomielite, crónica ou tardia, manifesta-se por vários distúrbios: distúrbios cognitivos, dificuldade de concentração por vezes associada a um estado de fadiga, dor, fraqueza muscular, distúrbios motores…. A ligação com a doença de Lyme é reconhecida quando a síntese de anticorpos específicos é encontrada no líquido cefalorraquidiano.
A polineuropatia aparece pela primeira vez com picos de dor, às vezes acompanhados de dormência e formigamento nas mãos ou pés. Está classicamente associada à acrodermatite atrófica. Também pode ser dor crônica na raiz isolada que se manifesta como ciática.
Formas discutidas ou controversasEles são mal compreendidos e difíceis de relacionar formalmente com a borreliose.
Manifestações dermatológicas (além de linfocitoma e acrodermatite ) foram descritas: morféia , esclerodermia , dermatomiosite ... mas a ligação com a doença de Lyme permanece hipotética e debatida.
Alguns pacientes, após um tratamento antibiótico bem conduzido, apresentam distúrbios subjetivos crônicos (cefaleia, fadiga e dores nas articulações), enquanto o objetivo clínico e biológico é a favor da cura. Em seguida, falamos de “síndrome de borreliose pós-Lyme” ou síndrome da doença pós-Lyme PLDS . A partir daí, e após uma continuidade confusa, surgiu o termo “doença crônica de Lyme”. Indefinido ou mal definido, reúne todo um conjunto de várias patologias crônicas, relacionadas à doença de Lyme. Essas são reivindicações, que apareceram nos Estados Unidos na década de 1990, e são feitas tanto por pacientes tratados e tratados, mas não curados, quanto por pacientes não previamente diagnosticados ou tratados para a doença de Lyme. Esse movimento associativo pretende defender esse diagnóstico e se beneficiar de terapias alternativas.
Diagnóstico
Diagnóstico positivo
O exame clínico continua sendo o elemento básico do processo diagnóstico de uma doença de Lyme. Pesquisamos a noção de picada de carrapato e eritema migrans, a origem geográfica e as atividades do paciente, avaliando as características mais ou menos características das lesões. Os vários exames são organizados e interpretados de acordo com esses dados clínicos. Em 2019, o diagnóstico de confirmação mais consensual com base na serologia em dois níveis para cada fase da infecção, excepto na presença de eritema migrans ( 1 r escalonados) que consideram a infecção como determinado.
SorologiaExistem dificuldades no diagnóstico serológico na Europa devido à diversidade das espécies patogénicas envolvidas, como a dos reagentes; daí a falta de padronização. Já nos Estados Unidos, a sorologia é mais fácil de interpretar (critérios padrão do CDC ), devido à presença de uma espécie patogênica muito predominante ( B. Burdorgferi em sentido estrito). No entanto, na década de 2010 , mesmo nos Estados Unidos, "a variabilidade interlaboratorial era considerável e continua sendo um problema nos testes da doença de Lyme" .
Durante a fase primária, o diagnóstico é exclusivamente clínico para eritema migrante. Nesta fase, a sorologia é desnecessária, pois a produção de anticorpos ainda é insuficiente. Da mesma forma, os dados biológicos, ainda nesta fase, costumam ser normais. A presença de uma síndrome inflamatória significativa deve sugerir outro diagnóstico.
Durante a fase secundária, exames sorológicos (ensaios de anticorpos) são discutidos dependendo do contexto. Existem dois métodos comumente usados na prática: ELISA e Western Blot . O teste ELISA é usado na primeira intenção, se for positivo ou duvidoso deve ser confirmado por Western-Blot. A administração de Stevia ou Serrapeptase antes do teste, por seu efeito anti-biofilme, permite que bactérias sejam liberadas no sistema sanguíneo o que melhora a sensibilidade de detecção.
Esta sorologia é realizada no sangue (linfocitoma, envolvimento cardíaco, artrite, etc.), no líquido articular (artrite) ou no líquido cefalorraquidiano (neuroborreliose).
Uma sorologia positiva tem valor patológico apenas em um contexto clínico evocativo. Por outro lado, uma sorologia negativa no mesmo contexto incentiva a repetição ou a continuação da investigação.
PCRO objetivo da PCR é detectar a presença de um fragmento do genoma de uma borrelia. É um exame opcional, em segunda intenção, nos casos duvidosos (contexto clínico e epidemiológico sugestivo, mas sorologia negativa). É feito em locais específicos (amostra de pele, líquido cefalorraquidiano, líquido articular) dependendo do contexto.
A PCR é muito específica, mas não prova uma infecção ativa, porque o DNA da borrelia pode persistir após sua morte (eliminação com antibióticos). Também nos Estados Unidos como na Europa, a sorologia continua sendo, na prática atual, o único método imediatamente disponível para o diagnóstico. Em 2019, “nenhum teste sorológico permite (...) diferenciar entre uma infecção passada e uma infecção ativa. O papel do internista é duplo: pensar na doença de Lyme diante dos sintomas focais e / ou gerais, mas também não atribuir erroneamente a uma doença de Lyme sintomas que deveriam abrir o campo dos diagnósticos diferenciais ” .
Um estudo mostrou que a infecção ativa pode ser detectada por análise de DNA circulante livre , com maior sensibilidade do que a sorologia.
Diagnóstico diferencial
Na fase primária, quando atípico, o eritema migrans pode ser confundido com eczema numular , eritema multiforme , dermatofitose , etc. e, no sudeste dos Estados Unidos, para um STARI (acrônimo para doença exantema associada ao carrapato do sul ).
Quando o eritema migrans está ausente ou passa despercebido, muitos diagnósticos podem ser elevados à fase secundária neurológica (encefalite viral ou mielite, Guillain-Barré , paralisia facial a frigore , esclerose múltipla ...), reumatológica ( artrite reumatóide , reação de artrite , artrite juvenil, etc.).
Na fase tardia, a acrodermatite crônica pode ser confundida com distúrbios relacionados à insuficiência venosa ou esclerodermia localizada. Os distúrbios gerais levam à discussão sobre fibromialgia ou fadiga crônica .
A diferença pode ser feita pela sorologia e pelo fato dos sintomas melhorarem com a antibioticoterapia.
A situação mais complexa surge quando um paciente é rotulado como “ Doença de Lyme crônica ” ou doença de Lyme crônica CLD . Essa entidade não é reconhecida pela comunidade científica devido à ausência de definição desses pacientes e à incapacidade de determinar a presença de germes ativos que persistem após o tratamento padrão.
Diagnóstico crônico de Lyme
Nos Estados Unidos, esses diagnósticos seriam realizados no âmbito de uma “contracultura” reunindo associações, laboratórios de exames diagnósticos não validados e médicos autoproclamados especialistas do afeto ou “médicos alfabetizados em Lyme” ( LLMD ), com atividades de lobby junto ao Congresso dos EUA e à Internet.
Esses diagnósticos de "doença de Lyme crônica" se enquadram em quatro categorias:
- A categoria 1 é um diagnóstico baseado apenas em sintomas não específicos (fadiga, dor crônica, distúrbios cognitivos ou de humor, etc.) sem qualquer distúrbio biológico detectável. Esses distúrbios inespecíficos estão presentes em pelo menos 10% da população geral, não relacionados a uma distribuição endêmica da doença de Lyme.
- A categoria 2 são pacientes com outra doença (quer já tenham ou não uma história de doença de Lyme não comprovada). Por exemplo, os pacientes têm dificuldade em aceitar o diagnóstico de esclerose múltipla e encontrar um médico disposto a tratá-los da doença de Lyme crônica.
- A categoria 3 não tem distúrbios clínicos objetivos sugestivos de doença de Lyme, mas eles têm anticorpos contra B. burgdoferi . Os médicos estão oferecendo um ensaio empírico de terapia antibiótica para tratar seus sintomas.
- A categoria 4 são pacientes (diagnosticados e tratados com Lyme) com manifestações crônicas que realizam “Síndrome de Borreliose Pós-Lyme” ou Síndrome Pós-Doença de Lyme PLDS . Esses são distúrbios subjetivos que podem persistir por um ano ou mais após o tratamento. Esses pacientes representam o problema mais geral de estados de fadiga e dor crônica.
Um estudo recente (2019) buscou estimar o número de casos da forma crônica da doença nos Estados Unidos em 2016 e 2020 . Seus resultados mostram uma prevalência "alta e crescente" de formas crônicas nos Estados Unidos: com base nos dados disponíveis, 69.011 a 1.523.869 pessoas foram afetadas em 2016, e em 2020 a prevalência pode chegar a 1.944.189.
Tratamento
Terapia antibiótica
Princípios básicosO objetivo do tratamento com antibióticos é curar as manifestações clínicas e evitar a progressão para as formas secundária e terciária, que se obtém com a erradicação completa da Borrelia. Não estamos tentando obter uma sorologia negativa.
Na prática, utiliza-se uma ciclina e, como segunda linha ou em casos especiais, uma β-lactama ( cefalosporina ).
Na fase primária (eritema migrans), amoxicilina ou doxiciclina devem ser prescritas por 14 a 21 dias , no mínimo: dentro de 72 horas se possível para melhores resultados.
Na fase secundária e terciária, para a neuroborreliose, são utilizadas principalmente as cefalosporinas , geralmente a ceftriaxona , por um período de 21 a 28 dias, no mínimo; por via venosa periférica em caso de meningoencefalite.
Para formas terciárias, durações mais longas podem ser oferecidas dependendo do caso.
Em Maio de 2019 um grupo de sociedades científicas francesas dá a seguinte opinião:
“Dado o continuum entre a forma inicial localizada e borreliose disseminada e a eficácia da doxiciclina para tratar a neuroborreliose, a doxiciclina é preferida como a primeira linha de tratamento para eritema migrans (duração 14 dias (d). Alternativa: amoxicilina) e neuroborreliose (duração 14 dias se o tratamento for precoce, 21 dias se atrasado. Alternativa: ceftriaxona). O tratamento das manifestações articulares da borreliose de Lyme é feito à base de doxiciclina, ceftriaxona ou amoxicilina por 28 dias . Pacientes com sintomas persistentes após tratamento apropriado não devem receber tratamento prolongado ou repetido. Alguns pacientes apresentam sintomas persistentes e pleomórficos após um diagnóstico documentado ou suspeito de borreliose. Outra patologia é diagnosticada em 80% deles. "
Em cerca de 15% dos pacientes, a antibioticoterapia pode causar uma reação de Jarisch-Herxheimer , relacionada à lise de bactérias, com exacerbação dos sintomas. Esta é uma reação leve e transitória que desaparece em algumas horas, ou um a dois dias.
EficiênciaAs infecções tratadas na fase primária são curadas com os antibióticos recomendados. Se a fase primária passar despercebida ou tratada de forma insuficiente, a doença continua a progredir.
Cerca de 10% dos pacientes tratados, e talvez mais naqueles com neuroborreliose, continuam a ter distúrbios subjetivos (fadiga, dores musculares, distúrbios cognitivos, etc.). Esses distúrbios persistem por mais de 6 meses após a antibioticoterapia recomendada e até mais de 10 anos, pelo menos de forma intermitente.
Embora a maioria dos pacientes melhore com o passar dos meses, essa condição tem um efeito duradouro na qualidade de vida. É a “síndrome de borreliose pós-Lyme”, ou síndrome pós-doença de Lyme PLDS . Nessa situação, os estudos controlados não mostram diferença entre a antibioticoterapia prolongada e um placebo, o que indica que a bactéria não pode ser responsável pelos sintomas.
Tratamentos alternativos
Mais ou menos reconhecidoSe a antibioticoterapia prolongada não for uma solução para essas condições crônicas, novas estratégias de manejo devem ser implementadas; sabendo que quase 40% dos pacientes crônicos com "borreliose pós-Lyme" melhoram com um placebo . O paciente "pós-Lyme" então se junta aos milhões de pessoas em todo o mundo que sofrem de fadiga e dores crônicas de origem indeterminada.
Assim, os transtornos depressivos devem ser tratados de acordo com os padrões usuais e a dor persistente de acordo com uma abordagem multidisciplinar semelhante ao tratamento da fibromialgia . Existem, portanto, combinações de medicamentos (analgésicos, antidepressivos, etc.), terapias comportamentais , fisioterapia e acupuntura .
Técnicas de origem neurocirúrgica , conhecidas como neuromodulação por estimulação espinhal, foram desenvolvidas para tratar síndromes complexas de dor crônica ou pós-operatória. Eles parecem ser capazes de reduzir a dor de pacientes com artrite de Lyme crônica que são resistentes aos tratamentos convencionais (medicamentos, fisioterapia).
Não reconhecido ou não recomendadoMuitos tratamentos alternativos são oferecidos na rede. O problema central é que afirmam curar os sintomas de uma doença quando sua existência não é comprovada (os estudos citados no parágrafo anterior chegam a concluir que ela não existe). Sem comprovação de eficácia - o que é lógico, visto que a própria existência da doença não foi validada - alguns apresentam certo risco de efeitos adversos.
- Terapia antibiótica não recomendada, por exemplo de duração muito longa; intermitente; repetido (para o mesmo episódio de Lyme); para co-infecções sem prova.
- Medicina hiperbárica .
- Terapias de "radiação ou energia" (que se enquadram no campo das pseudociências)
- Terapias "nutricionais".
- Quelação de metais pesados .
- Piroterapia .
- Vários medicamentos: imunoglobulinas, hormônios, veneno de abelha ...
As preparações fitoterápicas são oferecidas ou distribuídas por vários laboratórios.
Várias plantas, especialmente a quinina ganense ( Cryptolepis sanguinolenta ) e a knotweed japonesa (Polygonum cuspidatum), foram estudadas por pesquisadores americanos da Escola de Saúde Pública Johns Hopkins Bloomberg e testadas in vitro em culturas de Borrelia:
"Mesmo em baixas concentrações, os extratos dessas duas plantas destruíram as microcolônias de Borrelia e inibiram a divisão celular da forma livre da bactéria. Em 7 dias, uma solução de quinina ganense a 1% destruiu todas as bactérias, de modo que os antibióticos ou outras plantas não puderam erradicar todas as células. "
Um estudo mostra a atividade de certos óleos essenciais in vitro contra o biofilme formado pela bactéria. A Stevia também apresentou redução de biofilmes in vitro .
Na França, um deles, o Tic Tox , é uma mistura de óleos essenciais e própolis desenvolvida por Bernard Christophe (1949-2016), farmacêutico alsaciano especializado em fito-aromaterapia . Este produto foi suspenso em 2012, enquanto se aguarda a sua conformidade com os regulamentos, pela Agência Nacional para a Segurança de Medicamentos e Produtos de Saúde (AFSSAPS), que argumentou em particular que contém sálvia oficinal (potencialmente tóxica dependendo das doses ingeridas) e um terpeno , tujona , além de uma "falta de autorização de introdução no mercado " (AMM).
No entanto, segundo o professor Christian Perronne , especialista em doença de Lyme, essa decisão seria questionável.
Prevenção
Evite a exposição a carrapatos
A prevenção primária (atuar diretamente no caso: hospedeiros e vetores) é difícil devido à diversidade do reservatório animal. Sempre se discute atuar sobre um dos fatores de emergência (ver seção epidemiologia), pois se se identifica mais ou menos esses fatores, não se conhece bem a forma como reagem entre si. Por exemplo, nos Estados Unidos, onde a diversidade de reservatórios parece ser menor, a redução da população de veados ( especialmente veados-de-cauda-branca ), como forma de reduzir doenças humanas, é debatida.
As medidas recomendadas são evitar a exposição aos carrapatos.
Florestas- Use roupas de proteção na floresta (sapatos fechados, calças compridas enfiadas nas meias, camisa com gola fechada e mangas compridas abotoadas nos punhos; usar polainas para trabalhadores florestais e catadores de cogumelos). Roupas de cores claras permitem que você veja melhor os carrapatos. Proibir chinelos e sandálias, shorts e camisetas;
- evite áreas de risco muito alto (matagais, vegetação rasteira, etc. especialmente úmidas), permanecendo no meio dos caminhos, se possível;
- limitar o manejo da caça para os caçadores;
- o uso de repelentes em áreas de risco é possível. Por razões toxicológicas, a impregnação de roupas com inseticidas raramente era usada (incômodo e risco de efeitos colaterais);
nota: foram desenvolvidos trajes profissionais e uniformes de combate revestidos com polímero impregnado com permetrina (algodão, sintéticos e materiais mistos); eles reduzem o risco de mordidas em mais de 95% se a roupa for usada corretamente, de acordo com um estudo alemão. Essa proteção dura pelo menos um ano. Outro estudo (2020) só conseguiu comprovar essa proteção de 65% no primeiro ano e de 50% no segundo ano, sem efeitos imediatos detectados na saúde dos usuários da vestimenta. Algumas espécies de carrapatos (ou estágios de desenvolvimento) são mais sensíveis à permetrina do que outras. Um estudo de laboratório (2019) mostrou que após 16 dias de uso e 16 ciclos de lavagem / secagem na máquina 50-90% da permetrina que embebida em camisas, calças e meias tratadas em fábrica foi removida dos tecidos (agora fonte de poluição da água, e tornando a vestimenta significativamente menos protetora; após 1 hora de contato com o tecido, 31 a 67% dos carrapatos ainda apresentavam movimento normal, ao invés de fugir do tecido ou permanecer imobilizado nele). Por outro lado, os sapatos tratados, usados mas não lavados, permaneceram tão tóxicos para os carrapatos quanto eram originalmente. - inspecione-se cuidadosamente após caminhadas ou trabalho na floresta; em particular as axilas, o umbigo, os genitais, as dobras dos joelhos, sem esquecer nas crianças a cabeça e o couro cabeludo.
Um estudo científico participativo lançado no verão de 2017 na França pelo INRA , com base em um aplicativo ("Sinalização de carrapatos") que permite o mapeamento dos locais onde ocorreram picadas de carrapatos acaba de mostrar que - contra todas as expectativas - se 53% de os casos dizem respeito à floresta, 1/3 (exatamente 27%) das picadas declaradas voluntariamente ocorreram em jardins de residências particulares, e "apenas 10% em prados". Os inscritos são convidados a tirar uma fotografia do carrapato e enviá-la por correio aos pesquisadores (54 inscrições por dia em média emMaio de 2018) Um provável viés joga a favor de afirmações sobre humanos e o público dos entrevistados, sem dúvida, não é representativo de toda a população. Para 1.254 relatos de mordidas em animais, 4.198 foram em humanos. As picadas afetam primeiramente pessoas de 20 a 40 anos (30% dos casos) e de 40 a 60 anos (26%). Essa taxa cai para 17% na faixa etária de 5 a 20 anos. Seguem-se pessoas com mais de 60 anos (15% dos casos) e crianças com menos de 5 anos (12% dos casos). Para os animais, as declarações referem-se principalmente a cães (45% dos casos) e gatos (44%) e, em menor medida, a cavalos e gado (6 e 5% dos casos).
Entre as medidas às vezes recomendadas:
- manter seus jardins, em particular cortando grama alta em áreas freqüentadas e destruindo ou removendo folhas mortas;
- a abundância de carrapatos pode ser reduzida em algumas áreas (parques florestais suburbanos e jardins ...) por uma zona tampão livre de lixo de folhas mortas (por exemplo, coberta com cobertura morta ou cascalho entre a borda da floresta e áreas de jogo (criança, piquenique, etc. . ) e por medidas que proíbem a intrusão de animais como javalis ou veados), ao mesmo tempo que promovem os predadores naturais dos carrapatos: nas áreas rurais, as galinhas , que deles se alimentam, parecem limitar as suas populações.
- Equipe os animais de estimação com coleiras contra carrapatos, inspecione-os regularmente, especialmente depois de retornar de uma caminhada na floresta, e livre-os dos carrapatos. Inseticidas adequados podem ser pulverizados em cães;
- Os gatos são extremamente sensíveis a produtos químicos. Não aplique inseticida ou repelente a eles sem o conselho de um veterinário;
- Um modelo preditivo de risco foi criado para cães combinando fatores climáticos, geográficos e sociais, com resultados de testes sorológicos. Este modelo pode ser útil para ajudar os veterinários a avaliar o risco para os cães e talvez indiretamente para os humanos.
Esses cuidados nem sempre são suficientes e nem 100% eficazes, pois as ninfas do carrapato estão no limite de visibilidade (1 a 2 mm ) e sua picada é indolor. Além disso, animais de estimação podem trazer carrapatos para casa, resultando em contaminação cruzada com humanos.
Cuidado com picadas de carrapato
A contaminação requer um longo tempo de presença do carrapato na pele. Se o risco começa na primeira hora, é proporcional ao tempo de contato, no máximo entre 48 e 72 horas (a refeição de sangue do carrapato dura de 2 a 5 dias).
Se o carrapato for removido da pele nas primeiras 36 horas após sua fixação, o risco de contaminação é considerado baixo; menos de 1%, porque os borrelia ainda não estão nas glândulas salivares do carrapato, mas no trato digestivo. Para infectar o hospedeiro, eles ainda precisam migrar do trato digestivo para as glândulas salivares, o que pode levar de 2 a 3 dias , período que pode ser encurtado na Europa.
Remoção de carrapatosOs métodos populares, que usam uma gota de vários produtos para acalmar, sufocar ou separar o carrapato, são muito lentos ou podem regurgitar o carrapato: éter, benzina, gasolina, diesel, óleo comestível, esmalte de unha, calor por cigarro aceso ... É não é uma questão de esperar, portanto, o carrapato deve ser removido o mais rápido possível, sem manuseá-lo.
Vários modelos de pinças especiais ou tipos de pequenos pés de galinha que permitem a extração de carrapatos girando-os suavemente são vendidos nas farmácias (com um modelo menor para larvas e ninfas). Você não deve puxar, mas girar suavemente como se fosse desenroscar, você pode facilmente extrair o carrapato, pelo menos se não estiver ancorado por muito tempo. Essa ação evita o risco de deixar o rostro ou a cabeça e seu cimento grudado na pele, podendo causar infecção ou até mesmo abcesso.
Na ausência de um puxador de carrapato, você pode usar uma pinça fina para puxar o carrapato sem torcer ou esmagá-lo.
Tratamento de feridasDepois que o carrapato foi removido (e não antes, nenhum produto em um carrapato preso), a ferida deve ser cuidadosamente desinfetada e monitorada. Nesta fase, a antibioticoterapia profilática não é recomendada para picada simples de carrapato, devido à baixa probabilidade de contaminação. Isso pode ser discutido em certos casos específicos (gestantes, imunocomprometidos, etc.) ou mesmo em uma área hiperendêmica, quando o carrapato é removido tardiamente e ingurgitado de sangue.
O mesmo é verdade nos Estados Unidos, onde, após a picada do carrapato, a profilaxia antibiótica geralmente não é recomendada pelo CDC . As exceções estão em áreas hiperendêmicas, onde qualquer pessoa mordida com mais de 8 anos de idade pode receber uma dose única de 200 mg de doxiciclina em 72 horas após a remoção do carrapato. Para isso, todas as seguintes condições devem ser atendidas: nenhuma contra-indicação para doxiciclina, I. carrapato scapularis identificado, carrapato ingurgitado de sangue com um tempo estimado de fixação de mais de 36 h .
Após uma picada de carrapato, o monitoramento da ferida é necessário e suficiente. Nos dias ou semanas seguintes, é imperativo consultar um médico para terapia antibiótica apropriada, se uma mancha aparecer e crescer gradualmente (eritema migrans). Acontece o mesmo no caso de aparecimento de um estado febril ou de gripe (mais frequentemente na América do que na Europa).
Vacina
A partir de 2020, não há mais uma vacina humana disponível contra a doença de Lyme.
Existem vacinas veterinárias, inclusive para cães, com base na bactéria inteira morta ou em subunidades ( proteínas de superfície OspA ou OspC ).
Primeira vacinaUma vacina (recombinante), Lymerix de Smith-Kline-Beecham , foi comercializada nos Estados Unidos a partir dedezembro de 1998 (após a aprovação do FDA) em Fevereiro de 2002. Ele teve como alvo uma das proteínas de superfície mais comuns de B. Burgorferi , OspA . Tem sido recomendado para pessoas em risco em áreas endêmicas, e 1,4 milhão de doses foram distribuídas. Estudos demonstraram que sua eficácia está na faixa de 70 a 80%, sem efeitos colaterais significativos, mas as incertezas sobre seu efeito protetor de longo prazo implicam que reforços anuais podem ser necessários.
Em 1999 , rumores associaram a vacina à artrite autoimune e geraram processos judiciais, o que levou a uma ação coletiva de 121 demandantes. Estudos do CDC e do FDA não confirmam uma relação causal, acreditando que os benefícios da vacina superam os riscos. A vacina, portanto, permanece disponível ao público, mas as vendas entram em colapso devido à cobertura da mídia de testes em andamento e controvérsias sobre o risco teórico de autoimunidade.
Em 2002 , o fabricante retira por conta própria sua vacina do mercado, por questões econômicas. Em 2003 , um acordo foi alcançado com os demandantes: eles suspenderam todos os processos judiciais em troca de um milhão de dólares usados para reembolsar as custas de advogados e tribunais.
Pesquisa em andamentoA pesquisa de vacinas visa atingir as proteínas de superfície mais constantes da bactéria. Uma vacina desse tipo para a Europa e os Estados Unidos está em preparação.
Segundo Stanley Plotkin , a vacina ideal contra a doença de Lyme deve ter pelo menos 80% de eficácia em dois anos, nos dois lados do Atlântico, ser bem tolerada, não conter determinante antigênico de risco teórico e ser utilizável em crianças. Também deve ser aceito pelo público; para evitar os erros de comunicação cometidos durante o caso Lymerix , uma nova vacina terá que atender a uma demanda concertada dos atores da saúde pública e do público para que haja um mercado para esta vacina.
O laboratório Valneva está trabalhando atualmente Em uma vacina para 2025 e começará os testes em 15.000 indivíduos a partir de 2022.
Outra estratégia é quebrar o ciclo de vida da bactéria com uma vacina (ou vacinas) visando reservatórios animais e / ou vetores (carrapatos):
- a vacinação oral de um reservatório animal como o camundongo Peromyscus leucopus está sendo considerada na América do Norte, no modelo de vacinação oral de raposas contra a raiva , que se mostrou muito eficaz;
- outras pesquisas têm como alvo o vetor e, mais especificamente, os componentes da saliva do carrapato. Isso, teoricamente, teria a vantagem de proteger contra todas as doenças transmitidas por carrapatos.
Custos econômicos
As doenças transmitidas por carrapatos (doença de Lyme em particular) têm um custo anual que ascende a várias dezenas de milhões de euros por ano para muitos países (por exemplo, custo estimado de 20 milhões de euros / ano para países -Baixo e 80 milhões de euros / ano para a Alemanha para meados da década de 2010.
Controvérsia social
São teses e argumentos desenvolvidos por uma corrente alternada, que se contrapõe às recomendações oficiais das sociedades científicas que, por sua vez, alcançam consenso em nível internacional e que são acatadas por todas as autoridades sanitárias da América do Norte e da Europa.
Essa corrente alternada apareceu nos Estados Unidos na década de 1990, onde os médicos se reuniram em uma Sociedade Internacional de Doenças de Lyme e Associadas (ILADS), com o apoio de associações de pacientes. Essa corrente argumenta que as recomendações oficiais são muito restritivas, que a doença é subdiagnosticada e subtratada. Pretende-se assim promover novas atitudes terapêuticas junto das autoridades públicas, nomeadamente pelo reconhecimento de uma “doença de Lyme crónica”, e de uma antibioticoterapia de longa duração, por vezes associada a terapias não convencionais.
Em 2019, uma revisão das recomendações europeias e americanas sobre o diagnóstico da doença de Lyme mostra que nas diretrizes de 16 sociedades científicas de 7 países, apenas uma é diferente das outras (uma sociedade alemã, a Deutsche Borreliose-Gesellschaft, não reconhecida como uma sociedade acadêmica pelas autoridades alemãs). A conclusão é “Ao contrário do acalorado debate que ocorre na Internet e na mídia europeia e americana, nossa análise mostra que a maioria das recomendações científicas médicas associadas a um alto escore qualitativo concordam com os métodos de diagnóstico clínico para a doença de Lyme.” .
Suposições em discussão
O termo Lyme crônica (ou síndrome pós-tratamento ) pode se referir a recaídas, sintomas que persistem com a interrupção do tratamento com antibióticos ou complicações crônicas reconhecidas atribuídas à doença de Lyme. Também pode se referir a formas crônicas contestadas pela maioria da comunidade médica; ou ambos, o que é confuso. A forma crônica da doença tem sido objeto de definições, por exemplo na Suíça em 2005 “(evidência clínica e laboratorial documentada de uma infecção anterior com B. burgdorferi , curso completo de terapia antibiótica apropriada, sintomas incluindo fadiga, artralgia, mialgia, disfunção cognitiva ou dor radicular persistindo por mais de 6 meses, associação oportuna plausível entre infecção documentada por B. burgdorferi e início dos sintomas (ou seja, sintomas persistentes ou recorrentes que começaram dentro de 6 meses após a conclusão da terapia antibiótica recomendada para borreliose de Lyme precoce ou tardia ) e exclusão de outras causas somáticas ou psiquiátricas de sintomas) ” ou nos Estados Unidos em 2019.
O caráter crônico, inicialmente silencioso, logo a resistência aos antibióticos da doença pode ter várias explicações (compatíveis entre si):
- formas "císticas" persistentes da bactéria ( pleomorfismo ); já em 1995 , foi detectado que em reação à penicilina e doxiciclina (mas não à ceftriaxona), a bactéria pode assumir formas particulares que podem permitir sua sobrevivência nos tecidos de certos pacientes "apesar da terapia aparentemente adequada" ; essas formas persistentes poderiam, segundo os autores, ser a fonte de um “estímulo antigênico contínuo levando a queixas de borreliose de Lyme crônica” .
- uma forma L (reversível) da bactéria (suspeita em 1996 e confirmada em 2008);
- persistência em um biofilme , demonstrada em 2008.
Em 2014, os autores consideraram que não havia sido demonstrado o envolvimento dessas 3 variantes morfológicas em uma forma crônica da doença de Lyme; outros, em 2019, acreditam que a probabilidade de a doença de Lyme crônica ocorrer como resultado de infecções persistentes é real.
Em 2015, um autor (Paul M. Lantos) questiona o conceito de “criptoinfecções” (ligadas a coinfecções, quando o carrapato transmite várias doenças), principalmente quando bactérias não reconhecidamente transmissíveis por carrapatos, até patógenos fantasiosos são mencionado.
Para ILADS, a doença é onipresente e disseminada em formas ou transmissões não reconhecidas (por exemplo, sexual). ILADS em 2019 definiu a forma crônica da doença de Lyme como "doença multissistêmica com uma ampla gama de sintomas e / ou sinais que estão presentes de forma contínua ou intermitente por pelo menos seis meses" . Os sintomas persistentes são fadiga, dor, distúrbios do sono, cognitivos e neurológicos, a serem tratados com antibioticoterapia prolongada. A forma crônica resulta de “uma infecção ativa e contínua com um dos muitos membros patogênicos do complexo Borrelia burgdorferi sensu lato (Bbsl). A infecção tem períodos de latência variáveis e os sinais e sintomas podem aumentar, diminuir e migrar ” . ILADS distingue entre a forma crônica não tratada e tratada anteriormente (no último caso, com manifestações da forma crônica que persistem ou reaparecem após o tratamento e se apresentam continuamente ou de acordo com um padrão de recidiva / remissão durante um período de seis meses ou mais). Essas definições foram desenvolvidas com base em uma “revisão sistemática de mais de 250 artigos revisados por pares na literatura internacional” . De acordo com um estudo recente (2015), os sintomas podem persistir por mais de 10 anos, sem estar associados a um comprometimento funcional do paciente, nem a uma cepa particular de B. burgdorferi.
De acordo com um estudo prospectivo que acompanhou 174 homens e 109 mulheres com diagnóstico claro inicial (eritema migrans e confirmação por cultura) em seis meses, 12 meses e subsequentemente até 20 anos, não há diferença nos sintomas entre homens e mulheres para os sintomas basais , Taxa de sororreatividade de B burgdorferi ou frequência de sintomas pós-tratamento, incluindo 71 homens e 57 mulheres que puderam ser acompanhados por 20 anos, mas "as mulheres eram muito mais propensas do que os homens a retornar para consultas de acompanhamento" .
Para a maioria da comunidade médica, a corrente de “Lyme crônica” seria um conjunto de “alternativas” de microbiologia, imunologia e farmacologia, difundido na Internet e outras mídias, mesclado com depoimentos de pacientes. Essa corrente representaria 2% dos médicos em Connecticut, uma das regiões onde a endemia de Lyme é mais forte; essas seriam atitudes baseadas em suposições ou crenças subjetivas, e não em evidências científicas validadas. A forma crônica da doença é mais frequentemente expressa por sintomas subjetivos, os vários testes (testes de urina, contagem de linfócitos CD 57, imunofluorescência para mostrar formas L de Borrelia , etc.) foram desenvolvidos por "laboratórios especializados de Lyme", e seriam não ser clinicamente validado ou não aprovado pelo FDA .
Os argumentos dos proponentes da forma crônica também se baseiam no modelo animal ( cães , pôneis, etc.), mostrando que as borrelias podem persistir apesar do tratamento antibiótico adequado. Mas, segundo seus detratores, essa presença é frequente em animais infectados, sem apresentar doenças.
Esses argumentos científicos vêm acompanhados de apelos ao poder público, ou mesmo de processos judiciais contra sociedades médicas eruditas, acusadas de terem vínculos ocultos com seguradoras para limitar a duração e, portanto, o reembolso da antibioticoterapia. Em Connecticut , uma investigação sem precedentes foi realizada na Infectious Diseases Society of America (IDSA ), uma sociedade culta acusada de violar a lei antitruste , sob o argumento de que suas recomendações eram as únicas a serem seguidas pelas autoridades de saúde.
Aparentemente, encontra-se um compromisso temporário com a publicação, em 2011 (revista em 2014), das recomendações do ILADS num site oficial, mas na verdade é um site que apenas enumera recomendações sem as validar. As recomendações oficiais americanas, portanto, permanecem as publicadas nos sites do CDC ou NIH .
De acordo com o professor Lantos, membro do painel de recomendações do IDSA, tais controvérsias persistirão "enquanto os pacientes continuarem a sofrer de sintomas inexplicáveis que afetam sua qualidade de vida" .
Situação francesa
A definição, os limites e o valor dos meios diagnósticos para a "doença de Lyme crônica" permanecem em debate. Essa questão tornou-se um problema da sociedade, devido às polêmicas que provoca. Na França, isso levaria a uma dupla perda de confiança "para os pacientes que perdem a confiança em seu médico, para os médicos que perdem a confiança em si mesmos" em um clima de desconfiança recíproca.
Associações de pacientesAs principais associações são Lyme sans frontières fundada em 2012, 700 membros na França e na Bélgica em 2013, 90% dos quais estão doentes; e a França Lyme criada em 2008, reivindicando 400 membros em 2014 e 2.700 membros do31 de março de 2019. Existem outras associações menores com vocação local. Um relatório de 2014 da Alta Autoridade para a Saúde (HAS) afirma que a maioria dos gestores são mulheres e pertencem à categoria de executivos e profissões intelectuais superiores.
De acordo com o relatório do HAS de 2014, que cita um sociólogo, há um “cara a cara amargo” entre a legitimidade das associações e a autoridade da ciência. Os primeiros defendem seus conhecimentos pela experiência pessoal e íntima, os segundos são baseados na observação e na dedução científica ( medicina baseada em fatos ). Ainda de acordo com o relatório, estas associações estão mais próximas da atitude dos antivacinas do que das associações de luta contra o VIH, porque “na maioria das vezes permanecem tensas pelo ressentimento contra a classe médica e os especialistas. E, portanto, o sistema de ação em torno da questão da borreliose de Lyme oferece hoje o espetáculo da legitimidade social sem autoridade ” .
Se essas associações compartilham certos traços com os militantes contra a contaminação pelo HIV - orientação “ comunitária ” (recorremos a uma patologia específica), ambivalência das relações com o poder público entre colaboração e confronto, legitimidade da “expertise” dos pacientes (a “ Legitimidade incorporada do paciente ”) versus a experiência de cientistas e da profissão médica, e assim por diante. - distinguem-se pela ausência de universalismo (ao serviço da saúde pública em um determinado campo de risco), pela ausência de profissionalização dos militantes tendendo a se tornarem especialistas reconhecidos consultados pelo poder público, pela ausência de capital social (densidade das redes de relações com cientistas, mídia e política).
O relatório observa: "Longe de qualquer 'delírio', o protesto das associações é, pelo contrário, perfeitamente racional, o que não impede que alguns de seus argumentos sejam muito fracos" e "Também os ativistas defendem uma noção essencialista da ciência - de base arcana numa experiência íntima - para reclamar o monopólio de ser vítima da doença e, pelo menos, querer acreditar, os únicos a não esconder a verdade (porque livres de tudo conflito de interesses) ” .
Debates em cursoAté junho de 2018, o atendimento na França foi baseado em uma conferência de consenso de 2006, estabelecendo protocolos oficiais.
- Em 2014 , a Alta Autoridade para a Saúde (HAS) lembrou que “Tal como os outros jogadores, as associações devem ter a liberdade de se expressar. Eles também devem ser ouvidos. Embora não caiba a eles falar sobre ciência ou liderar políticas, cabe a eles, por outro lado, fazer com que a voz dos pacientes seja ouvida ”. Para salvar o diálogo e a confiança necessários, o HAS faz da borreliose de Lyme um fato não apenas biomédico, mas também social . Oferece uma escuta mais aberta às histórias e discursos dos pacientes por meio da pesquisa em ciências sociais .
- Em 2015 , a oposição apresentou um projeto de lei sobre esta doença em fevereiro, que foi rejeitado, mas seguido de várias perguntas sobre o reconhecimento da doença.
- Em 2016 , Matthias Lacoste iniciou uma greve de fome em junho para alertar as autoridades sanitárias e pelo “ direito à cura ”. Em julho, mais de cem médicos franceses, incluindo Christian Perronne (chefe do departamento de doenças infecciosas do hospital Garches ) e associações de pacientes ( França Lyme , Lyme sans frontières , Lymp'act ... agruparam-se na Federação Francesa contra o vetor doenças. carrapatos) queixam-se de uma situação que não leva em consideração a sua experiência e a sua vivência.
Um plano nacional de controle da doença de Lyme foi apresentado por Marisol Touraine , então Ministro dos Assuntos Sociais e Saúde, emsetembro de 2016. - Em 2018, as críticas incidiram sobre o teste sorológico considerado pouco confiável e sobre a existência de uma forma crônica às vezes não curada por 3 semanas de antibioticoterapia ”; com, portanto, uma subestimação do número de casos crônicos. O reconhecimento não oficial da forma crônica induziria modalidades de tratamento às vezes inadequadas.
Estas críticas são rejeitadas pela SPILF (Sociedade Francesa de Patologia Infecciosa ), que considera as recomendações de 2006 válidas face ao conhecimento atual; o mesmo para a Academia de Medicina .
a20 de junho de 2018, o HAS publica novas recomendações de gestão para a borreliose de Lyme. Eles confirmam (especificando-os) os protocolos de diagnóstico e tratamento já adotados, mas como nos Estados Unidos, distingue uma "síndrome pós-borreliose de Lyme" ou PLDS Pós-doença de Lyme, o HAS distingue "a / a sintomatologia / persistente síndrome polimórfica após possível picada de carrapato ”ou SPPT. Essa denominação de compromisso (falta de consenso) deve melhorar o atendimento ao paciente. a2 de julho de 2018, a Academia de Medicina "expressa claramente sua profunda decepção" com esse texto. Então o19 de julho de 2018, um grupo de sociedades eruditas e profissionais se recusam a endossar este nome de SPPT e a seguir suas recomendações.
EmSetembro de 2018(três meses após a publicação das recomendações do HAS), Jérôme Salomon ( Diretor Geral de Saúde ), ainda em busca de um consenso, pediu a Pierre Tattevin, presidente do SPILF "que desenvolvesse novas práticas de recomendações para a prevenção, diagnóstico e tratamento de borreliose de Lyme e outras doenças transmitidas por carrapatos ... ”. Por sua vez, o HAS explicou que, antes de publicar suas recomendações, tentou em vão chegar a um consenso com o SPILF. Assim, publicou essas recomendações sem a assinatura do SPILF, por estar convencido de que refletiam o estado da arte, mas prevendo duas reuniões por ano para atualizar as recomendações à luz do progresso científico, na esperança de resultar em recomendações comuns. com o SPILF que em 2019 “ainda considera que os testes de rastreamento são eficazes” e que não existe forma crônica da doença. - Em 2019 , o10 de abril, o Senado deve ouvir Jérôme Salomon e Dominique Le Guludec (presidente do HAS).
- a 7 de maio de 2019, o Boletim Epidemiológico Semanal publica um estudo mostrando que em uma série de casos com suspeita de diagnóstico de Lyme, o diagnóstico foi confirmado em menos de 10% dos casos, com a presunção de antibióticos falhando em 80% dos casos, 80% dos pacientes apresentando outra doença. De acordo com o colunista do boletim informativo, há um significativo sobrediagnóstico e tratamento excessivo da doença de Lyme, uma tendência observada no exterior. Isso representa um problema ético de saúde pública: na construção de recomendações de tratamento, modelos alternativos podem ser levados em consideração na ausência de fatos convincentes?
Instalações de pesquisa
Nos Estados Unidos, onde se estima que apesar das ações de informação e prevenção, o número de casos da doença de Lyme praticamente triplicou de 1990 a 2019 (mais de 300.000 casos / ano), as ações preventivas e de manejo da doença são travadas por inadequadas diagnósticos (com uma subestimação do número de casos: 30.000 casos declarados oficialmente de doenças transmitidas por carrapatos nos Estados Unidos por ano, em comparação com provavelmente 300.000 na realidade), observou o New England Journal of Medicine . O fabricante da única vacina contra a doença de Lyme disponível a retirou em meio à queda nas vendas e questões de responsabilidade.
Em 2018 , o NIH gastou US $ 23 milhões apenas na doença de Lyme em 2018, para um total de US $ 56 milhões alocados para todas as doenças transmitidas por carrapatos. Em 2019 , após parecer de um grupo consultivo mandatado pelo governo dos Estados Unidos (opinião alarmante e concluindo sobre a necessidade de aumentar ações e recursos financeiros para pesquisas sobre doenças transmitidas por carrapatos em nível federal), o NIH elaborou um novo plano estratégico para combater essas doenças, e emAbril de 2019, lançaram uma convocatória de propostas para a prevenção de doenças transmitidas por carrapatos, dotada de 6 milhões de dólares até 2020. Por sua vez, segundo a revista Science , os cientistas esperam obter ainda mais dinheiro para melhorar o diagnóstico da doença e os meios de tratá-la.
Uma arma biológica
Já em 1949 , trazido para os Estados Unidos como parte do programa Operation Paperclip , um cientista nazista desertor dos Estados Unidos chamado Erich Traub colaborou em Fort Detrick, onde supostamente infectou gado, cavalos e porcos com a febre aftosa vírus. Em 2004, um advogado de Long Island , Michael Carroll, lançou um livro chamado "Lab 257", no qual afirmava que Erich Traub também teria manipulado carrapatos aumentando suas quantidades de " Borrelia " para torná-los mais contagiosos no Plum. Island Animal Disease Center, um centro militar biológico a poucos quilômetros da costa da cidade de Lyme . Carrapatos escaparam da ilha, especialmente em aves migratórias.
Na década de 1970, uma estranha epidemia de dores nas articulações estourou no condado de Lyme, nos Estados Unidos. A rapidez da epidemia e sua relativa proximidade geográfica com o Centro de Doenças dos Animais de Plum Island deram origem a uma espécie de suspeita.
O Representante Republicano de Nova Jersey, Chris Smith , aprovou uma emenda que visa lançar uma investigação sobre as acusações de que um laboratório militar é a fonte da doença de Lyme. "Vários livros e artigos sugerem que uma extensa pesquisa foi conduzida em instalações militares dos EUA, incluindo Fort Detrick, Maryland , e Plum Island , Nova York, a fim de usar carrapatos e outros. Insetos como armas biológicas".
Mas a acusação de experimentos baseados na contaminação de moscas, mosquitos e carrapatos, foi reavivada por um livro publicado em maio de 2019: "Bitten, a história secreta da doença de Lyme e armas biológicas" por Kris Newby, uma cientista da Universidade de Stanford fazendo-se contraiu a doença de Lyme. Em seu livro, Kris Newby cita em particular Willy Burgdorfer , entomologista e bacteriologista suíço-americano que em 1981 identificou o germe responsável pela doença de Lyme: Borrelia Burgdoferi , cujo nome é derivado dele.
Willy Burgdofer diz que trabalhou em armas biológicas para os militares dos EUA durante a Guerra Fria . Suas responsabilidades incluíam, diz ele, criar pulgas, carrapatos, mosquitos e outros insetos sugadores de sangue e infectá-los com patógenos capazes de transmitir doenças aos humanos. E seria, de acordo com Willy Burgdofer, uma daquelas experiências que teria dado errado e causado a epidemia de Lyme nos Estados Unidos.
O professor Christian Perronne , apresentado na mídia como especialista em doença de Lyme, disse em 2016 que a explosão da doença de Lyme, escondida "pelos militares americanos e cientistas sob seu controle" , se deve a uma proliferação de carrapatos mal controlados traficados pelos nazistas Pesquisador de virologia - Erich Traub - transferido para os Estados Unidos como parte da Operação Paperclip no final da Segunda Guerra Mundial.
Personalidades alcançadas
- Avril Lavigne
- Shania Twain
- Elena Delle Donne
- Bella tinha feito
- Ashley Olsen
- Alec Baldwin
- Fabien Canal
- George W. Bush
- Pierrick Fédrigo
- Justin Bieber
- Richard Gere
Notas e referências
- Gwenaël Vourc'h et al. , Zoonoses: Essas doenças que nos ligam aos animais , Éditions Quæ , coll. "EnjeuxScience",2021( ISBN 978-2-7592-3270-3 , ler online ) , Alguns exemplos de doenças zoonóticas, "Lyme borreliosis", p. 79-81, acesso livre.
- (em) Wynne Parry, " Iceman Mummy May Hold Earliest Evidence of Lyme Disease " on Live Science (acessado em 13 de março de 2020 ) .
- Cosson JF (2019) Ecology da doença de Lyme ; Public Health, 1 (HS), 73-87.
- " Nos Estados Unidos, as autoridades eleitas querem saber se os militares usaram carrapatos como armas biológicas "
- (em) Owen Dyer , " US Pentágono para Investigar reivindicações é dito que a doença de Lyme é uma arma biológica que escapou da guerra fria " , BMJ , vol. 366,19 de julho de 2019, l4784 ( ISSN 0959-8138 e 1756-1833 , PMID 31324616 , DOI 10.1136 / bmj.l4784 , ler online , acessado em 20 de julho de 2019 )
- (en) Robert D. Leff, Lyme Borreliosis , Cambridge, Cambridge University Press ,1993, 1176 p. ( ISBN 0-521-33286-9 ) , p. 852-854em The Cambridge World History of Human Disease, KF Kiple (eds).
- (em) Allen C. Steere , Stephen E. Malawista , David R. Snydman e Robert E. Shope , " Uma epidemia de artrite oligoarticular em crianças e adultos em três comunidades de Connecticut " , Arthritis & Rheumatism , Vol. 20, n o 1,1977, p. 7–17 ( ISSN 1529-0131 , DOI 10.1002 / art.1780200102 , lido online , acessado em 4 de julho de 2021 )
- (em) Johnson RC, FW Hyde GP Schmid e DJ Brenner " Borrelia burgdorferi sp. nov .: agente etiológico da doença de Lyme » Int J Syst Bacteriol . 1984; 34: 496-497.
- Barbour, AG, W. Burgdorfer, SF Hayes, O. Péter e A. Aeschlimann. "Isolation of a cultivable spirochete from Ixodes ricinus ticks of Switzerland" Current Microbiology 1983; 8: 123-126.
- (em) Ryan KJ, Ray CG; Sherris Medical Microbiology ; 4 ª edição (página 434-437) Ed: McGraw Hill, 2004; ( ISBN 978-0-8385-8542-9 )
- E. Pilly, Doenças infecciosas e tropicais: todos os itens de doenças infecciosas , Paris, Alinea Plus,2018, 720 p. ( ISBN 978-2-916641-66-9 ) , p. 377-378.
- (em) E. Claudia Coipan , Setareh Jahfari Manoj Fonville e G. Anneke Oei , " Presença desequilibrada de Borrelia burgdorferi sl tipo de sequência multilocus em manifestações clínicas da borreliose de Lyme " , Infection, Genetics and Evolution , vol. 42,agosto de 2016, p. 66-76 ( DOI 10.1016 / j.meegid.2016.04.019 , lido online , acessado em 24 de setembro de 2020 )
- Sylvie De Martino, " La Borreliose de Lyme ", La Revue du praticien , vol. 55,2005, p. 471-477.
- Steere AC & al. (2016) Borreliose de Lyme . Nature Reviews Disease Primers, 2, 16090. doi: 10.1038 / nrdp.2016.90
- (en) Michael K. Faulde e Martin Rutenfranz , " Padrão de infestação de carrapatos humanos, taxa de picadas de carrapatos e risco de infecção de Borrelia burgdorferi sl associado durante exposição ocupacional a carrapatos na área de treinamento militar de Seedorf, noroeste da Alemanha " , em Carrapatos e doenças transmitidas por carrapatos ,setembro de 2014( DOI 10.1016 / j.ttbdis.2014.04.009 , acessado em 24 de setembro de 2020 ) ,p. 594-599
- Evison J, Aebi C, Francioli P, Péter O, Bassetti S, Gervaix A, Zimmerli S, Weber R, “ Diagnóstico e tratamento da borreliose de Lyme em adultos e crianças: recomendações da Sociedade Suíça de doenças infecciosas: borreliose de Lyme 1 st parte: epidemiologia e diagnóstico [ doença de Lyme parte I : epidemiologia e diagnóstico ] " Rev Med Suisse , vol. 2, n o 60,2006, p. 919-24. ( PMID 16673723 , leia online [html] )
- F. Rodhain, “ Lyme disease: epidemiology ”, La Revue du Praticien , vol. 39, n o 15,18 de maio de 1989, p. 1291-1293.
- Por Le Parisien com AFP Em 27 de abril de 2021 às 19h46 , " doença de Lyme: 30% de carrapatos carregando um agente infeccioso, picadas em jardins em ascensão " , em leparisien.fr ,27 de abril de 2021(acessado em 28 de abril de 2021 )
- (en) SM Dunham-Ems, MJ Caimano, U. Pal, CW Wolgemuth, Eggers CH, A. Balic e JD Radolf, " Imagens ao vivo revelam uma forma bifásica de disseminação de Borrelia burgdorferi dentro de carrapatos " , J Clin Invest , vol . 119, n o 12,2009, p. 3652-3665 ( DOI 10.1172 / JCI39401 , leia online )
- (em) Tilly K, Rosa PA, Stewart PE. “ Biologia da infecção com Borrelia burgdorferi ” Infect Dis Clin North Am . 2008; 22: 217-234.
- INRA , “ Reservatório de pesquisa, vetor de soluções: o papel fundamental do INRA nas doenças transmitidas por carrapatos ” , em www.inra.fr ,9 de maio de 2017(acessado em 17 de dezembro de 2017 )
- “ Marisol Touraine lança Plano Nacional de Luta contra a Doença de Lyme e Doenças Transmitidas por Carrapatos ”, Ministério da Solidariedade e Saúde ,29 de setembro de 2016( leia online , consultado em 17 de dezembro de 2017 )
- Allen C. Steere , Frank Strle , Gary P. Wormser e Linden T. Hu , “ Lyme borreliosis ”, Nature reviews. Disease primers , vol. 2,15 de dezembro de 2016, p. 3. ( ISSN 2056-676X , PMID 27976670 , PMCID PMC5539539 , DOI 10.1038 / nrdp.2016.90 , ler online , acessado em 30 de abril de 2018 )
- (en) Dennis DT, Piesman, JF. “Visão geral das infecções transmitidas por carrapatos em humanos” In: Goodman JL, Dennis DT, Sonenshine DE, eds. Infecções humanas transmitidas por carrapatos . Washington, DC: ASM Press , 2005.
- (em) Allen C. Steere, " O aparecimento da Doença de Lyme " , J Clin Invest , Vol. 113, n o 8,2004, p. 1093-1101 ( ler online )
- Trap D (1996) Aspectos clínicos, epidemiológicos, diagnósticos e de controle da doença de Lyme em animais domésticos . Touro. de GTV., 2, 55-59
- Lamouraux, Cécile (2005), Borreliose de Lyme no cavalo , tese de doutorado em veterinária defendida na Faculdade de Medicina de Créteil; Alfort National Veterinary School
- Meryl P. Littman , Richard E. Goldstein , Mary A. Labato e Michael R. Lappin , “ Declaração de Consenso de Pequenos Animais ACVIM sobre Doença de Lyme em Cães: Diagnóstico, Tratamento e Prevenção ”, Journal of Veterinary Internal Medicine , vol. 20, n o 2Março de 2006, p. 422-434 ( ISSN 0891-6640 e 1939-1676 , DOI 10.1111 / j.1939-1676.2006.tb02880.x , leia online )
- Moutailler S. et al. (2015) Principais doenças transmitidas por carrapatos: epidemiologia, clínica e diagnóstico . In: McCoy KD, Boulanger N., eds. Carrapatos e doenças transmitidas por carrapatos: Biologia, ecologia evolutiva, epidemiologia. IRD Éditions. doi: 10.4000 / books.irdeditions.9047.
- Sara Moutailler , Claire Valiente Moro , Elise Vaumourin e Lorraine Michelet , “ Co-infecção de carrapatos: A regra em vez da exceção ”, PLoS Neglected Tropical Diseases , vol. 10, n o 3,17 de março de 2016( ISSN 1935-2727 , PMID 26986203 , PMCID 4795628 , DOI 10.1371 / journal.pntd.0004539 , lido online , acessado em 18 de maio de 2020 )
- Steere 2016, op. cit., p. 13 (em formato pdf).
- Djuk-Wasser MA & al. (2016) Coinfection by Ixodes Tick-Borne Pathogens: Ecological, Epidemiological, and Clinical Consequences . Trends in Ecology and Evolution, 32, 1, pp. 30-42. doi: 10.1016 / j.pt.2015.09.008
- Muriel Vayssier-Taussat , Maria Kazimirova , Zdenek Hubalek e Sándor Hornok , “ Horizontes emergentes para patógenos transmitidos por carrapatos: da visão de 'um patógeno - uma doença' ao paradigma do patobiologia ”, Future Microbiology , vol. 10, n o 12,dezembro de 2015, p. 2033–2043 ( ISSN 1746-0913 , PMID 26610021 , PMCID 4944395 , DOI 10.2217 / fmb.15.114 , ler online , acessado em 18 de maio de 2020 )
- Johnson et al. (2014) Gravidade da doença de Lyme crônica em comparação com outras condições crônicas: uma pesquisa de qualidade de vida . PeerJ, 2, e322. doi: 10.7717 / peerj.322
- M. Alcalay, " Lyme disease ", La Revue du Praticien , vol. 44, n o 12,1944, p. 1611-1618.
- (en-US) “ transmissão da doença de Lyme ” , em www.cdc.gov (acessado em 30 de abril de 2018 )
- (en-US) “ Perguntas frequentes sobre a doença de Lyme (FAQ) | Doença de Lyme | CDC ” , em www.cdc.gov (acessado em 14 de agosto de 2017 )
- " Doença de Lyme e doação de sangue | Etablissement francais du sang ” , em dondesang.efs.sante.fr (acessado em 30 de abril de 2018 )
- Vayssier-Taussat M & al. (2015) Como uma abordagem multidisciplinar “One Health” pode combater a ameaça do patógeno transmitido por carrapatos na Europa. Future Microbiology, vol. 10, pp. 809-818. doi: 10.2217 / fmb.15.15, veja também One Health
- (en-US) “ Quantas pessoas contraem a doença de Lyme? | Doença de Lyme | CDC ” , em www.cdc.gov (acessado em 28 de abril de 2018 )
- (em) Sarah E. St. Pierre , Odette N. Gould e Vett Lloyd , " Conhecimento e necessidades de conhecimento sobre a doença de Lyme entre usuários ocupacionais e recreativos do ar livre " , Jornal Internacional de Pesquisa Ambiental e Saúde Pública , vol. 17, n o 1,5 de janeiro de 2020, p. 355 ( ISSN 1660-4601 , PMID 31948017 , PMCID PMC6981950 , DOI 10.3390 / ijerph17010355 , ler online , acessado em 24 de setembro de 2020 )
- (em) NH Ogden , C. Bouchard , J. Badcock e MA Drebot , " Qual é o número real de casos de doença de Lyme no Canadá? ” , BMC Public Health , vol. 19, n o 1,dezembro de 2019, p. 849 ( ISSN 1471-2458 , PMID 31253135 , PMCID PMC6599318 , DOI 10.1186 / s12889-019-7219-x , ler online , acessado em 26 de setembro de 2020 )
- (en) A Rizzoli , HC Hauffe , G Carpi e GI Vourc'h , “ Lyme borreliosis in Europe ” , Eurosurveillance , vol. 16, n o 27,7 de julho de 2011( ISSN 1560-7917 , DOI 10.2807 / ese.16.27.19906-en , ler online , acessado em 28 de abril de 2018 )
- (en-US) “ LYME ” , em epidemio.wiv-isp.be (acessado em 29 de abril de 2018 )
- Escritório Federal de Saúde Pública BDPA , “ Doenças transmitidas por carrapatos - Situação na Suíça ” , em www.bag.admin.ch (acessado em 29 de abril de 2018 )
- Rede Sentinels (2018) | URL = https://websenti.u707.jussieu.fr/sentiweb/
- C. Thorin , E. Rigaud , I. Capek e G. André-Fontaine , " Seroprevalence of Lyme borreliosis and tick-borne encephalitis in profissionais expostos no Grand Est da França ", Medicine and Infectious Diseases , vol . 38, n o 10,Outubro de 2008, p. 533-542 ( DOI 10.1016 / j.medmal.2008.06.008 , lido online , acessado em 24 de setembro de 2020 )
- (em) Mathilde De Keukeleire , Annie Robert , Victor Luyasu e Benedict Kabamba , " Seroprevalence of Borrelia burgdorferi in Belgian forestry workers and associated risk fators " , Parasites & Vectors , vol. 11, n o 1,dezembro de 2018, p. 277 ( ISSN 1756-3305 , PMID 29716647 , PMCID PMC5930862 , DOI 10.1186 / s13071-018-2860-2 , ler online , acessado em 24 de setembro de 2020 )
- (en) M. Cinco , F. Barbone , M. Grazia Ciufolini e M. Mascioli , “ seroprevalência de infecções transmitidas por carraças em guardas florestais do nordeste da Itália ” , Clinical Microbiology and Infection , vol. 10, n o 12,dezembro de 2004, p. 1056-1061 ( DOI 10.1111 / j.1469-0691.2004.01026.x , ler online , acessado em 24 de setembro de 2020 )
- Ogden NH, Lindsay LR, Morshed M, Sockett PN, Artsob H. (2009) The emergence of Lyme disease in Canada . CMAJ; 180: 1221-4
- Jacques Exbalin , aquecimento global e seus impactos , t. II: O caso da França , Paris, edições L'Harmattan ,2014, 296 p. , com os testemunhos de Jean Jouzel , Nicolas Hulot , Yann Arthus-Bertrand , Yves Cochet e Brice Lalonde ( ISBN 978-2-336-34951-0 e 2-336-34951-5 , OCLC 887816626 , aviso BnF n o FRBNF43832179 , ler online ) , p. 230
- Stone, BL, Tourand, Y., & Brissette, CA (2017). Admiráveis mundos novos: o universo em expansão da doença de Lyme . Doenças transmitidas por vetores e zoonóticas | resumo .
- Tougeron K, Perez G, Gillard M, Seimandi-Corda G, Balbi M, et al .. (2015) Biodiversidade sob prescrição? Os efeitos da perda de biodiversidade na saúde, o exemplo da doença de Lyme em Quebec . Prêmio de ciência popular da Universidade de Montreal, Canadá. (hal-01162524)
- (in) Joshua Lederberg, Emerging Infections , National Academy Press ,1992( ISBN 0-309-04741-2 ) , p. 27-28
- (em) Z. Popović, S. Popović. “Forest Transition and Zoonoses Risk” Enciclopédia de Saúde Ambiental , p. 803-811 ( Resumo )
- Jean-Louis Chapuis, " Lyme borreliosis: introdução de um novo hospedeiro, o esquilo siberiano ", Boletim epidemiológico semanal ,14 de setembro de 2010, p. 6-8
- Sapi E & al. (2019) Antibiotics: The Long-Term Persistence of Borrelia burgdorferi Antigens and DNA in the Tissues of a Patient with Lyme Disease ; Antibiotics 2019, 8 (4), 183; https://doi.org/10.3390/antibiotics8040183
- Eppes SC & Childs JA (2002) Estudo comparativo de cefuroxima axetil versus amoxicilina em crianças com doença de Lyme inicial . Pediatrics, 109, 1173-1177.
- Preac-Mursic V, Weber K., Pfister HW, Wilske B, Gross B, Baumann A e Prokop J (1989) Survival of Borrelia burgdorferi in antibiotically tratados pacientes com Lyme borreliosis . Infection, 17, 355-359.
- Liegner KB, Rosenkilde CE, Campbell GL, Quan TJ, Dennis DT (1992) Falha no tratamento confirmado por cultura de cefotaxima e minociclina em um caso de meningoencefalomielite de Lyme nos Estados Unidos . Em Proceedings of the Program and Abstracts of the Fifth International Conference on Lyme Borreliosis, Arlington, VA, USA, 30 de maio - 2 de junho de 1992; Federação das Sociedades Americanas para Biologia Experimental: Bethesda, MD, EUA, 1992; Volume A11.
- Liegner KB, Shapiro JR, Ramsay D, Halperin AJ, Hogrefe W & Kong L (1993) Eritema migrans recorrente apesar do tratamento antibiótico prolongado com minociclina em um paciente com infecção persistente por Borrelia burgdorferi . J. Am. Acad. Dermatol, 28, 312-314.
- Steere, AC; Angelis, SM (2006) Terapia para artrite de Lyme: Estratégias para o tratamento da artrite refratária a antibióticos . Arthritis Rheum, 54, 3079–3086.
- Klempner, MS, Baker PJ, Shapiro ED, Marques A, Dattwyler RJ, Halperin JJ e Wormser GP (2013) Testes de tratamento para sintomas de doença pós-lima revisitados . Am. J. Med., 126, 665-669
- Hodzic, E.; Feng, S.; Holden, K.; Freet, KJ; Barthold, SW (2008) Persistence of Borrelia burgdorferi após tratamento com antibióticos em ratos . Antimicrob. Agentes Químicos. | 52, 1728-1736.
- Hodzic, E.; Imai, D.; Feng, S.; Barthold, SW (2014) Ressurgência de Borrelia burgdorferi não cultivável persistente após tratamento com antibióticos em camundongos . PLoS ONE 2014, 9, e86907.
- Straubinger, RK; Summers, BA; Chang, YF; Appel, MJ (1997) Persistence of Borrelia burgdorferi em cães infectados experimentalmente após tratamento com antibióticos . J. Clin. Microbiol, 35, 111-116.
- Berndtson, K. (2013) Revisão das evidências de evasão imune e infecção persistente na doença de Lyme . Int. J. Gen. Med, 6, 291-306.
- Brasas, ME; Barthold, SW; Borda, JT; Bowers, L.; Doyle, L.; Hodžić, E.; Jacobs, MB; Hasenkampf, NR; Martin, DS; Narasimhan, S.; et al. (2012) Persistência de Borrelia burgdorferi em Rhesus Macaques após tratamento com antibióticos de infecção disseminada . PLoS ONE 2012, 7, e29914.
- Brasas, ME; Barthold, SW; Borda, JT; Bowers, L.; Doyle, L.; Hodžić, E.; Jacobs, MB; Hasenkampf, NR; Martin, DS; Narasimhan, S.; et al. (2012) Persistência de Borrelia burgdorferi em Rhesus Macaques após tratamento com antibióticos de infecção disseminada . PLoS ONE, 7, e29914.
- Brasas, ME; Hasenkampf, NR; Jacobs, MB; Tardo, AC; Doyle-Meyers, LA; Philipp, MT; Hodzic, E. (2017) Manifestações variáveis, sororreatividade diversa e persistência pós-tratamento em primatas não humanos expostos a Borrelia burgdorferi pela alimentação de carrapatos . PLoS ONE, 12, e0189071.
- Crossland, NA; Alvarez, X.; Embers, ME. Doença de Lyme disseminada tardia: Patologia associada e persistência de espiroquetas pós-tratamento em Rhesus Macaques. Am. J. Pathol. 2018, 188, 672–682.
- Hodzic, E.; Imai, DM; Escobar, E. (2019) A generalidade da persistência pós-tratamento antimicrobiano de Borrelia burgdorferi cepas N40 e B31 em cepas de camundongos geneticamente suscetíveis e resistentes . Infectar. Immun., IAI.00442-19.
- Feng, J.; Cama.; Yuan, Y.; Sim, R.; Zhang, Y. (2019) Bactérias em biofilme / persistente / em fase estacionária causam doença mais grave do que bactérias em fase log - Biofilme Borrelia burgdorferi não apenas exibe mais tolerância aos antibióticos de Lyme, mas também causa patologia mais grave em um modelo de artrite em camundongo: implicações para compreender a persistência , PTLDS e falha do tratamento . Discov. Med., 148, 125-138.
- Schmidli, J.; Hunziker, T.; Moesli, P.; Schaad, UB (1988) Cultivation of Borrelia burgdorferi from joint fluid três meses após o tratamento de paralisia facial devido a borreliose de Lyme . J. Infect. Dizer. 1988, 158, 905–906.
- Häupl, T.; Hahn, G.; Rittig, M.; Krause, A.; Schoerner, C.; Schönherr, U.; Kalden, JR; Burmester, GR (1993) Persistence of Borrelia burgdorferi em tecido ligamentar de um paciente com borreliose de Lyme crônica . Artrite. Rheum., 36, 1621-1626.
- Battafarano, DF; Combs, JA; Enzenauer, RJ; Fitzpatrick, JE (1993) Artrite séptica crônica causada por Borrelia burgdorferi . Clin. Orthop. Relat. Res., 297, 238–241.
- Middelveen, MJ; Sapi, E.; Burke, J.; Filush, KR; Franco, A.; Fesler, MC; Stricker, RB (2018) Infecção persistente por Borrelia em pacientes com sintomas contínuos da doença de Lyme . Cuidados de saúde, 6, 33.
- Sylvie de Martino, " European Borreliosis and Lyme Disease ", Le Concours Médical , vol. 126, n o 33,10 de novembro de 2004, p. 1919-1924
- (in) Carrie D. Tibbles, " Será que este paciente tem Eritema migrans? ” , Journal of the American Medical Association , vol. 297, n o 23,20 de junho de 2007, p. 2617-2626
- Speere 2016, op. cit., p. 9-10.
- Frédéric Blanc, “ Neuroborreliose: quando pensar nisso? », La Revue du Praticien - medicina geral , vol. 21, nos . 782-783,2 de outubro de 2007, p. 843-846.
- Christine Tranchant, “ Neurolyme: como fazer o diagnóstico? », La Revue du Praticien - medicina geral , vol. 33, n o 1022,Maio de 2019, p. 428-429.
- Steere 2016, op. cit., p. 10-11.
- (en) Yeung C, Baranchuk A, “Diagnóstico e tratamento da cardite de Lyme” J Am Coll Cardiol . 2019; 73: 717-26. . DOI : 10.1016 / j.jacc.2018.11.035 .
- Pilly 2017, op. cit., pp. 379-380.
- Nicholas A. Crossland , Xavier Alvarez e Monica E. Embers , “ Late Disseminated Lyme Disease: Associated Pathology and Spirochete Persistence Posttreatment in Rhesus Macaques ”, The American Journal of Pathology , vol. 188, n o 3,março de 2018, p. 672-682 ( ISSN 1525-2191 , PMID 29242055 , PMCID 5840488 , DOI 10.1016 / j.ajpath.2017.11.005 , ler online , acessado em 9 de maio de 2020 )
- (in) Johannes Nemeth, " Atualização das diretrizes suíças sobre a síndrome da doença de Lyme pós-tratamento " , Swiss Medical Weekly ,2016( leia online [PDF] )
- (en) Feder HM, Johnson BJ, O'Connell S. et al. " Uma avaliação crítica da" doença de Lyme crônica " " N Engl J Med . 2007; 357 (14): 1422-30. DOI : 10.1056 / NEJMra072023 .
- Paul M. Lantos , “ Chronic Lyme Disease ”, Infectious disease clinics of North America , vol. 29, n o 2junho de 2015, p. 325–40 ( ISSN 0891-5520 , PMID 25999227 , PMCID PMC4477530 , DOI 10.1016 / j.idc.2015.02.006 , ler online , acessado em 3 de maio de 2018 ).
- François Bicaire , " a doença de Lyme ", La Revue du praticien - Médecine générale , vol. 29, n o 934,janeiro de 2015, p. 55-57
- HAS 2012 , p. 26
- Steere 2016, op. cit., p. 12 e 32.
- (in) BA Fallon , Sr. Pavlicová , SW Coffino e C. Brenner , " Uma Comparação dos Resultados do Teste Sorológico da Doença de Lyme de 4 Laboratórios em Pacientes com Sintomas Persistentes Após Tratamento com Antibióticos " , Clinical Infectious Diseases , vol. 59, n o 12,15 de dezembro de 2014, p. 1705–1710 ( ISSN 1058-4838 e 1537-6591 , DOI 10.1093 / cid / ciu703 , lido online , acessado em 26 de setembro de 2020 )
- "2018: Biofilms busters para melhorar a detecção de Borrelia usando PCR"
- Steere 2016, op. cit., p. 11-12.
- Feyeux D & Fantin B (2019) Notícias sobre o manejo da doença de Lyme . The Journal of Internal Medicine, 40 (4), 226-231 | resumo .
- "The lancet, December 2019: Detection of Borrelia burgdorferi Cell-Free DNA in Human Plasma Samples for Improved Diagnostic of Early Lyme Borreliosis"
- (em) Eugene D. Shapiro, " doença de Lyme " , The New England Journal of Medicine , vol. 370, n o 18,1 r maio 2014, p. 1724-1731.
- Paul G Auwaerter , Johan S Bakken , Raymond J Dattwyler e J Stephen Dumler , “ Antiscience and Ethics associated with advocacy of Lyme disease ”, The Lancet. Doenças infecciosas , vol. 11, n o 9,setembro de 2011, p. 713-719 ( ISSN 1473-3099 , PMID 21867956 , PMCID PMC4489928 , DOI 10.1016 / S1473-3099 (11) 70034-2 , ler online , acessado em 3 de maio de 2018 )
- Joanna Ścieszka , Józefa Dąbek e Paweł Cieślik , “ Post-Lyme disease syndrome ”, Reumatologia , vol. 53, n o 1,2015, p. 46-48 ( ISSN 0034-6233 , PMID 27407225 , PMCID 4847307 , DOI 10.5114 / reum.2015.50557 , ler online , acessado em 4 de junho de 2020 )
- (in) Michael T. Melia, " Tempo para uma abordagem diferente para a doença de Lyme e sintomas de Longo Prazo " , The New England Journal of Medicine , vol. 374, n o 13,31 de março de 2016, p. 1277-1278.
- (em) Allison DeLong e Mayla Hsu , " Estimativa do número cumulativo de casos de doença de Lyme pós-tratamento nos EUA, 2016 e 2020 " no BMC Public Health ,dezembro de 2019( ISSN 1471-2458 , PMID 31014314 , PMCID PMC6480773 , DOI 10.1186 / s12889-019-6681-9 , acessado em 24 de setembro de 2020 ) ,p. 352
- " Conferência de consenso de Lyme borreliosis 2006 " , em infectiologie.com (acessado em 4 de maio de 2018 )
- (en) B. Jaulhac, A. Saunier, E. Caumes, K. Bouiller, Gehanno JF et al. , “ Borreliose de Lyme e outras doenças transmitidas por carrapatos. Diretrizes das Sociedades Científicas Francesas (II). Biológico, tratamento, sintomas persistentes após borreliose de Lyme documentada ou suspeita ” , Medicina e Doenças Infecciosas ,31 de maio de 2019( DOI 10.1016 / j.medmal.2019.05.001 )
- Thomas Butler , " The Jarisch - Herxheimer Reaction After Antibiotic Treatment of Spirochetal Infections: A Review of Recent Cases and Our Understanding of Pathogenesis " , The American Journal of Tropical Medicine and Hygiene , vol. 96, n o 1,11 de janeiro de 2017, p. 46-52 ( ISSN 0002-9637 , PMID 28077740 , PMCID PMC5239707 , DOI 10.4269 / ajtmh.16-0434 , ler online , acessado em 4 de maio de 2018 )
- Steere 2016, op. cit., p. 16
- Steere 2016, op. cit., p. 17
- Simpson EL, Duenas A, Holmes MW, Papaioannou D, Chilcott “Estimulação da medula espinhal para dor crônica de origem neuropática ou isquêmica: revisão sistemática e avaliação econômica”; J. Health Technol Assess. Março de 2009; 13 (17): iii, ix-x, 1-154. ( resumo )
- Shui Y, Tao W, Huang D, Li Y, Fan B. “Estimulação da medula espinhal para dor crônica originada da doença de Lyme” ; Pain Physician. Novembro de 2012; 15 (6): 511-4. ( resumo )
- Paul M. Lantos , Eugene D. Shapiro , Paul G. Auwaerter e Phillip J. Baker , “ Unorthodox Alternative Therapies Marketed to Treat Lyme Disease, ” Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America , vol. 60, n o 12,15 de junho de 2015, p. 1776–1782 ( ISSN 1058-4838 , PMID 25852124 , PMCID PMC4490322 , DOI 10.1093 / cid / civ186 , ler online , acessado em 4 de maio de 2018 )
- Steere 2016, op. cit., p. 17 e 33.
- (en-US) Natalie S. Marzec , Christina Nelson , Paul Ravi Waldron e Brian G. Blackburn , “ Serious Bacterial Infections Adquiridas Durante Tratamento de Pacientes Dado um Diagnóstico de Doença de Lyme Crônica - Estados Unidos ” , MMWR. Morbidity and Mortality Weekly Report , vol. 66, n o 23,16 de junho de 2017, p. 607–609 ( ISSN 0149-2195 e 1545-861X , DOI 10.15585 / mmwr.mm6623a3 , ler online , acessado em 8 de maio de 2018 )
- (em) Matthew Wood, The Book of Herbal Wisdom , North Atlantic Books , Berkeley, Califórnia, 1997 ( ISBN 978-1-55643-232-3 ) .
- Wolf-Dieter Storl ( traduzido do alemão por Christophe Bernard), Curar a doença de Lyme naturalmente: tratamento holístico e usos práticos , Paris, Guy Trédaniel ,2013( 1 st ed. 2011 c alemão / o Weltbild sob o título " Borreliose natürlich heilen: ganzheitliche Behandlung und Anwendungen praktische " e depois em 2012 em holandês, sob o título " A partir van ziekte Lyme " ), 274 p. ( ISBN 978-2-8132-0618-3 e 2-8132-0618-0 , aviso BnF n o FRBNF43668365 , apresentação online )
- (de) Petra Gutmann , “ Borreliose: Natürliche Therapie ” , boletim informativo A. Vogel , Teufen “9. Heilpflanzen, die helfen” ,2014( leia online [Zecken, Borreliose, FSME: Informationen über Begriffe und Behandlung von Lyme Borreliose und FSME]) Veja carda selvagem ( dipsacus silvestris ), unha de gato ( uncaria tomentosa ).
- (en) Brorson O, Brorson SH, " extrato de semente de toranja é um poderoso agente in vitro contre motile e formas císticas de Borrelia burgdorferi sensu lato " , Infection , vol. 35, n o 3,2007, p. 206-8. ( PMID 17565468 ) [ ler online ] : clique na guia Look inside para ler as duas primeiras páginas do texto.
- https://www.frontiersin.org/articles/10.3389/fmed.2020.00006/full
- https://www.lanutrition.fr/lyme-deux-plantes-qui-tuent-la-bacterie-borrelia
- "Cronometrado: alguns óleos essenciais têm forte atividade contra a fase estacionária e o biofilme de Borrelia burgdorferi"
- "Fronteiras na medicina: Óleos essenciais seletivos de especiarias ou ervas culinárias têm alta atividade contra a fase estacionária e o biofilme Borrelia burgdorferi"
- "2015, Ncbi: Effectiveness of Stevia Rebaudiana Whole Leaf Extract Against the Various Morphological Forms of Borrelia Burgdorferi in Vitro"
- Guilhem Denis , " Carrapatos: o proibido remédio Tic Tox ", Europe 1 ,27 de janeiro de 2012( leia online ) “A comercialização de um produto, apresentado como remédio preventivo ou curativo para picadas de carrapato (doença de Lyme, borreliose, etc.) pela empresa Nutrivital, acaba de ser proibida pela Agência de Produtos de Saúde (Afssaps). As notas Afssaps que este produto é o tema da promoção divulgando seus efeitos terapêuticos enquanto ele não tem um marketing de autorização (AMM) para medicamento e que ela também apresenta riscos de neurotoxicidade , mesmo quando tomado por um curto período de tempo por via oral. "
- Decisão Afssaps [PDF] , 2012.
- Pryska Ducoeurjoly , " Arquivo: a proibição do Tic Tox surge em um contexto polêmico ", Aberturas: o tempo do cidadão "doença de Lyme",2 de março de 2013( leia online ) Entrevista com o professor Christian Perronne , especialista em doença de Lyme, chefe do Departamento de Doenças Infecciosas do Hospital Raymond-Poincaré em Garches (92), presidente da Comissão Especializada para Doenças Transmissíveis do Conselho Superior de Saúde Pública (HCSP).
- Rand PW & al. (2004) Abundância de Ixodes scapularis (Acari: Ixodidae) após a remoção completa de cervos de uma ilha isolada ao largo da costa, endêmica para a doença de Lyme . J. Med. Entomol. 41, 779-784
- Gilbert, L. et al. (2012) O efeito do manejo de veados na abundância de Ixodes ricinus na Escócia . Escola. Appl. 22, 658-667
- Levi, T. et al. (2012) Cervos, predadores e o surgimento da doença de Lyme. Proc. Natl. Acad. Sci. USA 109, 10942-10947
- KJ Kugeler , RA Jordan , TL Schulze e KS Griffith , “ Will Culling White-Tailed Deer Prevent Lyme Disease? », Zoonoses and public health , vol. 63, n o 5,agosto de 2016, p. 337-45. ( ISSN 1863-1959 , PMID 26684932 , PMCID PMC4912954 , DOI 10.1111 / zph.12245 , ler online , acessado em 5 de maio de 2018 )
- (em) Meagan F. Vaughn e Steven R. Meshnick , " Estudo Piloto Avaliando a Eficácia da Roupa Impregnada com Permetrina de Longa Duração para a Prevenção de Picadas de Carrapato " , Vector-Borne and Zoonotic Diseases , vol. 11, n o 7,julho de 2011, p. 869-875 ( ISSN 1530-3667 e 1557-7759 , DOI 10.1089 / vbz.2010.0158 , ler online , acessado em 24 de setembro de 2020 )
- (en) Robert Prose , Nicole E Breuner , Tammi L Johnson e Rebecca J Eisen , " Contact Irritancy and Toxicity of Permethrin-Treated Clothing for Ixodes scapularis, Amblyomma americanum, and Dermacentor variabilis Ticks (Acari: Ixodidae) " , Journal of Medical Entomology ,24 de maio de 2018( ISSN 0022-2585 e 1938-2928 , PMID 29800259 , PMCID PMC6119117 , DOI 10.1093 / jme / tjy062 , ler online , acessado em 24 de setembro de 2020 )
- (em) Michael K. Faulde Martin Rutenfranz Alexander Keth e Jürgen Hepke , " Estudo piloto Avaliando a eficácia de roupas impregnadas de permetrina de longa duração tratadas em fábrica para a prevenção de picadas de carrapato Durante a exposição ocupacional, carrapato em áreas de treinamento militar altamente infestadas , Alemanha ” , Parasitology Research , vol. 114, n o 2fevereiro de 2015, p. 671-678 ( ISSN 0932-0113 e 1432-1955 , DOI 10.1007 / s00436-014-4232-y , ler online , acessado em 24 de setembro de 2020 )
- (em) Meagan F. Vaughn , Sheana Whelan Funkhouser , Chang Feng Lin e Jason Fine , " Long-duration Permethrin Impregnated Uniforms " , American Journal of Preventive Medicine , vol. 46, n o 5,Maio de 2014, p. 473-480 ( DOI 10.1016 / j.amepre.2014.01.008 , lido online , acessado em 24 de setembro de 2020 )
- (em) Cedar Mitchell , Megan Dyer , Feng Chang Lin e Natalie Bowman , " Protective Effectiveness of Long-Lasting Permethrin Impregnated Clothing Against Carrapatos No Ano Endemic Lyme Disease Setting: A Randomized Control Trial Entre Outdoor Workers " , Journal of Medical Entomology , vol. 57, n o 5,7 de setembro de 2020, p. 1532–1538 ( ISSN 0022-2585 e 1938-2928 , DOI 10.1093 / jme / tjaa061 , ler online , acessado em 24 de setembro de 2020 )
- (en) Neeta P Connally , Dominic A Rose , Nicole E Breuner e Robert Prose , " Impact of Wearing and Wash / Drying of Permethrin-Treated Clothing on Your Contact Irritancy and Toxicity for Nymphal Ixodes scapularis (Acari: Ixodidae) Ticks ” , Journal of Medical Entomology , vol. 56, n o 1,8 de janeiro de 2019, p. 199–214 ( ISSN 0022-2585 e 1938-2928 , PMID 30165532 , PMCID PMC6326861 , DOI 10.1093 / jme / tjy138 , ler online , acessado em 24 de setembro de 2020 )
- Cuidado com os carrapatos: jardins em risco , Notícias da TWC França;
- (en-US) “ Preventing Tick Bites on People | Doença de Lyme | CDC ” , em www.cdc.gov (acessado em 5 de maio de 2018 )
- (en) Piesman J, Eisen L. " Prevenção de doenças transmitidas por carrapatos " Annu Rev Entomol . 2008; 53: 323--43.
- (em) Ginsberg HS, M Butler, Zhioua E. "O efeito da cerca de exclusão de cervos é pela abundância de Amblyomma americanum (Acari: Ixodidae) em Fire Island " Nova York, EUA, J Vector Ecol . 2002; 27: 215--21,13,14.
- (en-US) Daphne Cybele , " Tick Control: How a Flock of Chickens May Be Your Best Bet " , em Wide Open Pets ,11 de maio de 2019(acessado em 12 de julho de 2019 )
- (en-US) “ Prevenção de carrapatos em seus animais de estimação | Doença de Lyme | CDC ” , em www.cdc.gov ,11 de agosto de 2017(acessado em 5 de maio de 2018 )
- Watson SC, Liu Y, Lund RB, Gettings JR, Nordone SK, McMahan CS, et al. (2017) Um modelo espaço-temporal bayesiano para prever a prevalência de anticorpos para Borrelia burgdorferi, agente causador da doença de Lyme, em cães domésticos nos Estados Unidos contíguos. PLoS ONE 12 (5): e0174428. https://doi.org/10.1371/journal.pone.0174428
- Gétaz G, Loutan L, N Mezger, “ Doenças transmitidos por carrapatos de aqui e noutros lugares [ doenças transmitidas por carraças localmente e no exterior ] ”, Rev Med Suisse , vol. 8, n o 340,2012, p. 974-6. ( PMID 22662624 , leia online [html] )
- (en-US) “ remoção e testes Tick | Doença de Lyme | CDC ” , em www.cdc.gov ,10 de agosto de 2017(acessado em 5 de maio de 2018 )
- A instrução para girar lentamente no sentido REVERSO das agulhas de um relógio está claramente escrita em uma caixa contendo dois “tira-carrapatos”, produzidos, vendidos em farmácias, nos laboratórios Clément-Thékan em Montrouge (França). Na verdade, você tem que escolher uma direção de rotação e girar o instrumento nessa direção, duas ou três voltas ou mais se necessário, sem mudar de direção durante a operação, para que o tick desapareça. No sentido anti-horário (como para desparafusar) seria mais conveniente para destros, e o outro (como para aparafusar) para canhotos: perguntas frequentes sobre alicates .
- (em) " profilaxia de picada de carrapato (p. 20) " , em cdc.gov (acessado em 5 de maio de 2018 )
- Monica E. brasas e Sukanya Narasimhan , “ A vacinação contra a doença de Lyme: passado, presente e futuro ”, Frontiers in Cellular and Infection Microbiology , vol. 3,12 de fevereiro de 2013( ISSN 2235-2988 , PMID 23407755 , PMCID PMC3569838 , DOI 10.3389 / fcimb.2013.00006 , ler online , acessado em 6 de maio de 2018 )
- (in) Angela K. Shen , Paul S. Mead e Charles B. Beard , " A doença de Lyme Vaccine-A perspectiva de saúde pública " , Clinical Infectious Diseases , vol. 52, n o suppl_3,1 ° de fevereiro de 2011, s247 - s252 ( ISSN 1537-6591 e 1058-4838 , DOI 10.1093 / cid / ciq115 , ler online , acessado em 24 de setembro de 2020 )
- L. E. Nigrovic e KM THOMPSON , “ A vacina de Lyme: um conto preventivo ”, Epidemiology and Infection , vol. 135, n o 1,janeiro de 2007, p. 1–8 ( ISSN 0950-2688 , PMID 16893489 , PMCID PMC2870557 , DOI 10.1017 / S0950268806007096 , ler online , acessado em 6 de maio de 2018 )
- (em) Hanner, M., W. Schüler, A. Meinke, U. Lundberg, Plos One Design e desenvolvimento de uma nova vacina para proteção contra borreliose de Lyme , PLoS ONE 9 (11): e113294. Doi: 10.1371 / journal.pone.0113294.
- (in) Stanley A Plotkin, " necessidade de uma nova Lyme Disease Vaccine " , The New England Journal of Medicine , vol. 375, n o 10,8 de setembro de 2016, p. 911-913
- Joseph Martin , " Vaccine against Lyme: a French Laboratory pretende ser comercializado até 2025 " , na RSE Magazine (acessado em 4 de agosto de 2020 ) .
- Maria Gomes-Solecki , “ Bloqueio da transmissão de patógenos na fonte: vacinas baseadas em OspA direcionadas a reservatórios contra Borrelia burgdorferi ”, Frontiers in Cellular and Infection Microbiology , vol. 4,26 de setembro de 2014( ISSN 2235-2988 , PMID 25309883 , PMCID PMC4176399 , DOI 10.3389 / fcimb.2014.00136 , ler online , acessado em 24 de setembro de 2020 )
- Cees C Van den Winjngaard et al. (2017) O custo da borreliose de Lyme . European Journal of Public Health, 27, 3, pp. 538-547. doi: 10.1093 / eurpub / ckw269
- Lohr IB (2015) Epidemiologia e custo dos cuidados hospitalares para borreliose de Lyme na Alemanha: Lições de uma análise de banco de dados de utilização de cuidados de saúde . Carrapatos e doenças transmitidas por carrapatos, 6, 1, pp. 56-62. doi: 10.1016 / j.ttbdis.2014.09.004
- Alison Tonks , “ Lyme wars, ” British Medical Journal , vol. 335, n o 7626,3 de novembro de 2007, p. 910–912 ( ISSN 0959-8138 , PMID 17974685 , PMCID PMCPMC2048873 , DOI 10.1136 / bmj.39363.530961.AD , ler online , acessado em 9 de junho de 2019 )
- C. Eldin , A. Raffetin , K. Bouiller e Y. Hansmann , “ Revisão das diretrizes europeias e americanas para o diagnóstico de borreliose de Lyme ”, Medecine Et Maladies Infectieuses , vol. 49, n o 2março de 2019, p. 121-132 ( ISSN 1769-6690 , PMID 30528068 , DOI 10.1016 / j.medmal.2018.11.011 , ler online , acessado em 9 de maio de 2020 )
- (em) J Nemeth , E Bernasconi , U Heininger e o Sr. Abbas , " Atualização das diretrizes suíças sobre a síndrome da doença de Lyme pós-tratamento " , Swiss Medical Weekly ,5 de dezembro de 2016( ISSN 1424-7860 e 1424-3997 , DOI 10.4414 / smw.2016.14353 , ler online , acessado em 24 de setembro de 2020 )
- (em) Samuel Shor , Christine Green , Beatrice Szantyr e Steven Phillips , " Chronic Lyme Disease: An Evidence-Based Definition ILADS by the Working Group " , Antibiotics , vol. 8, n o 4,16 de dezembro de 2019, p. 269 ( ISSN 2079-6382 , PMID 31888310 , PMCID PMC6963229 , DOI 10.3390 / antibióticos8040269 , ler online , acessado em 24 de setembro de 2020 )
- A. Kersten , C. Poitschek , S. Rauch e E. Aberer , “ Effects of penicillin, ceftriaxone, and doxycycline on morphology of Borrelia burgdorferi ”, Antimicrobial Agents and Chemotherapy , vol. 39, n o 5,Maio de 1995, p. 1127-1133 ( ISSN 0066-4804 , PMID 7625800 , PMCID PMC162695 , DOI 10.1128 / aac.39.5.1127 , ler online , acessado em 24 de setembro de 2020 )
- (em) Vera Preac Mursic Sylvia Reinhardt , Bettina Wilske e U. Busch , " Training and cultivo ofBorrelia burgdorferi spheroplast L-form options " , Infection , Vol. 24, n o 3,Maio de 1996, p. 218-226 ( ISSN 0300-8126 e 1439-0973 , DOI 10.1007 / BF01781096 , ler online , acessado em 24 de setembro de 2020 )
- (em) Judith Miklossy Sandor Kasas Anne D Zurn e Sherman McCall , " Persistente atípico e formas císticas de Borrelia burgdorferi e inflamação local em Lyme neuroborreliose " , Journal of Neuroinflammation , vol. 5, n o 1,2008, p. 40 ( ISSN 1742-2094 , PMID 18817547 , PMCID PMC2564911 , DOI 10.1186 / 1742-2094-5-40 , ler online , acessado em 24 de setembro de 2020 )
- Paul M. Lantos , Paul G. Auwaerter e Gary P. Wormser , " A Systematic Review of Borrelia burgdorferi Morphologic Variants Does Not Support a Role in Chronic Lyme Disease ", Clinical Infectious Diseases: An Official Publication of the Infectious Diseases Society of America , vol. 58, n o 5,1 r março 2014, p. 663-671 ( ISSN 1058-4838 , PMID 24336823 , PMCID PMC3922218 , DOI 10.1093 / cid / cit810 , ler online , acessado em 8 de maio de 2018 )
- Natalie Rudenko , Maryna Golovchenko , Katerina Kybicova e Marie Vancova , “ Metamorfoses de espiroquetas da doença de Lyme: fenômeno de persistência de Borrelia ”, Parasites & Vectors , vol. 12,16 de maio de 2019( ISSN 1756-3305 , PMID 31097026 , PMCID 6521364 , DOI 10.1186 / s13071-019-3495-7 , ler online , acessado em 18 de maio de 2020 )
- Paul Lantos apresenta-se como especialista no uso de SIG para epidemiologia; Autor sênior de um relatório (2010) do Painel de Revisão das Diretrizes de Doenças de Lyme para a Sociedade de Doenças Infecciosas da América. Ele co-presidiu um painel (30 membros) sobre as diretrizes da doença de Lyme (de autoria da American Academy of Neurology, do American College of Rheumatology e da Infectious Diseases Society of America).
- (em) Erica Weitzner , Donna McKenna , John Nowakowski e Carol Scavarda , " Avaliação a longo prazo dos sintomas de pós-tratamento em pacientes com doença de Lyme precoce confirmada por cultura " , Clinical Infectious Diseases , vol. 61, n o 12,15 de dezembro de 2015, p. 1800-1806 ( ISSN 1058-4838 e 1537-6591 , PMID 26385994 , PMCID PMC4657537 , DOI 10.1093 / cid / civ735 , ler online , acessado em 24 de setembro de 2020 )
- (em) Erica Weitzner , Paul Visintainer e Gary P. Wormser , " Comparison of mach versus female with Culture-confirmado early Lyme disease at presentation and on 11-20 Years After Diagnostic " , Diagnostic Microbiology and Infectious Disease , Vol. 85, n o 4,agosto de 2016, p. 493-495 ( DOI 10.1016 / j.diagmicrobio.2016.04.012 , ler online , acessado em 24 de setembro de 2020 )
- (em) " Eventos anteriores de defesa da doença de Lyme " .
- (em) "Avaliações de evidências e recomendações de diretrizes na doença de Lyme: o manejo clínico de picadas de carrapatos, erupções cutâneas e eritema migrans persistente. | National Guideline Clearinghouse ” , em www.guideline.gov (acessado em 8 de fevereiro de 2017 )
- Y. Hansmann, " Does Chronic Lyme Disease Exist?" », La Revue du Praticien , vol. 66,setembro de 2016, p. 711-714.
- TEM 2014 , p. 41-42
- " Activity report April 2018 - March 2019 " , em francelyme.fr (acessado em 26 de julho de 2019 )
- TEM 2014 , p. 44
- HAS 2014 , p. 46
- " consenso 2006 "
- HAS 2014 , p. 39
- HAS 2014 , p. 46-47 ..
- " Doença de Lyme: Matthias, em greve de fome, exige 'o direito de ser curado' ", The Obs ,2016( leia online , consultado em 11 de maio de 2018 )
- " Doença de Lyme: o grito de alarme de 100 médicos: 'Há uma emergência' ", The Obs ,2016( leia online , consultado em 11 de maio de 2018 )
- " Doença de Lyme: a longa luta do Professor Perronne ", leparisien.fr ,3 de fevereiro de 2017( leia online , consultado em 11 de maio de 2018 )
- " Doença de Lyme:" Tive que passar minha ficha como a de um animal " ", leparisien.fr ,3 de fevereiro de 2017( leia online , consultado em 11 de maio de 2018 )
- " resumo do plano de 2016 "
- " Doença de Lyme: necessidade urgente de atualizar as recomendações " [vídeo] , no Medscape (acessado em 3 de julho de 2020 ) .
- " Doença de Lyme: Por que a França está tão tarde ", The Huffington Post ,13 de julho de 2016( leia online , consultado em 11 de maio de 2018 )
- " Doença de Lyme: posição do SPILF - doença de Lyme: posição de " , em www.infectiologie.com (acessado em 8 de fevereiro de 2017 )
- " Conclusões da doença de Lyme " , em academie-medecine.fr (acessado em 7 de maio de 2018 )
- “ Haute Autorité de Santé - Lyme Borreliosis e outras doenças transmitidas por carrapatos ” , em www.has-sante.fr (acessado em 5 de julho de 2018 )
- " Comunicado de imprensa de 2 de julho de 2018:" Atualização da Haute Autorité de Santé (HAS) sobre a doença de Lyme: Reações e decepções da National Academy of Medicine "- National Academy of Medicine | Uma instituição no seu tempo ”, Academia Nacional de Medicina | Uma instituição em seu tempo ,2 de julho de 2018( leia online , consultado em 4 de agosto de 2018 )
- "Comunicado de imprensa de todas as sociedades científicas envolvidas no manejo de doenças transmitidas por carrapatos", 19 de julho de 2018 .
- Science et Avenir (2019) Doença de Lyme: a situação está se tornando onipresente ; Olivier Hertel; 08/04/2019
- Ex para literatura médica francófona: com Scholar
- Não deve ser confundida com subnotificação, uma doença pode ser diagnosticada e tratada (correta ou incorretamente) sem ser notificada aos sistemas de vigilância. Veja https://www.cdc.gov/lyme/stats/humancases.html
- " Boletim epidemiológico semanal, 7 de maio de 2019 " , em invs.santepubliquefrance.fr (acessado em 9 de junho de 2019 )
- medicalXpress (2018) Lacunas na prevenção, gerenciamento de doenças transmitidas por carrapatos identificadas, publicado em 6 de setembro de 2018
- Paris Match , " Lyme disease: the masked killer 1/2 " , em parismatch.com (acessado em 25 de junho de 2021 )
- " A propagação da doença de Lyme se deve a experimentos militares dos EUA?" » , Em www.franceinter.fr (consultado em 26 de junho de 2021 )
- " Os militares dos EUA criaram a doença de Lyme?" » , On Sciences et Avenir (acessado em 25 de junho de 2021 )
- " Poderia um experimento que deu errado poderia ser a causa da epidemia de Lyme nos Estados Unidos?" » , Em SudOuest.fr (acessado em 25 de junho de 2021 )
- Adrien Sénécat, " Quem é realmente Christian Perronne, referindo médico dos conspiradores?" : o chefe do departamento de doenças infecciosas do hospital Garches é o suporte científico do documentário Hold-up e um seguidor de “teorias alternativas” ”, Le Monde , 18-19 de novembro de 2020 ( ler online , consultado a 6 de abril de 2021 ), cf. seção intitulada "Adepto em teorias alternativas " .
- Isabelle Léouffre (artigo atualizado em5 de janeiro de 2017), " Doença de Lyme: o assassino mascarado (1/2) ", Paris Match "Realidade ou lenda? Acredita-se que a doença de Lyme seja devida à manipulação genética de carrapatos ”,14 de junho de 2016( leia online , consultado em 7 de abril de 2021 ).
- Anne-Laure Barret, " doença de Lyme, conspiração aplicada a ácaros ", Le Journal du dimanche , 18 de setembro de 2016 com modificação e atualização em 21 de junho de 2017 ( leia online , consultado em 28 de abril de 2020 ).
- " Lyme, doença imaginária? », Actu.fr - L'Orne Hebdo , Normandia,26 de maio de 2016( leia online , consultado em 6 de abril de 2021 ).
- ladepeche.fr, " Em lágrimas, Avril Lavigne relata sua luta contra a doença de Lyme ", La Dépêche ,30 de junho de 2015( leia online , consultado em 3 de julho de 2020 ).
- " Avril Lavigne sobre a doença de Lyme:" Estes foram os piores anos da minha vida "- Elle " , em elle.fr ,12 de setembro de 2018(acessado em 3 de julho de 2020 ) .
- RTL Newmedia , " Shania Twain com doença de Lyme ficou sem palavras: 'Eu realmente pensei que era o fim da minha carreira' ", RTL People ,17 de julho de 2017( leia online , consultado em 23 de setembro de 2018 )
- (em) Steve Ginsburg, " doença de Lyme nunca longe dos pensamentos da estrela da WNBA Delle Donne " , Yahoo,15 de setembro de 2015(acessado em 15 de setembro de 2015 )
- (en) http://www.dailymail.co.uk/tvshowbiz/article-3265978/Bella-Anwar-Hadid-battling-Lyme-disease-mom-Yolanda-Foster-reveals.html
- " 8 estrelas vítimas da doença de Lyme " , em Medicite.fr ,11 de dezembro de 2017(acessado em 5 de julho de 2018 )
- " Doença de Lyme: as estrelas afetadas pela doença " , em Doctissimo.fr (acessado em 5 de julho de 2018 )
- (em) " Alec Baldwin pensou que 'morreria da doença de Lyme.' O que saber sobre a doença transmitida por carrapato ” , em Health.com (acessado em 25 de dezembro de 2018 )
- " Doença de Lyme: estrelas afetadas pela doença " , em Doctissimo (acessado em 25 de dezembro de 2018 )
- " Doença de Lyme: um ciclista de alto nível quase parou por causa de um carrapato " , em www.pourquoidocteur.fr (acessado em 30 de julho de 2019 )
- " arbusto-foi-tratado-para-doença-de-lima-casa-branca "
- " Fédrigo sofreu de uma infecção bacteriana " , em velochrono.fr ,27 de julho de 2011(acessado em 27 de julho de 2011 )
- Prisma Media , " Justin Bieber revela que tem a doença de Lyme - Aqui está " , em Ici.fr (acessado em 9 de janeiro de 2020 )
- " doença de richard-gere-lyme "
Veja também
Bibliografia
- “ TEM. Borreliose de Lyme ' ,2014(acessado em 11 de maio de 2018 ) .
- Judith Albertat , doença de Lyme: minha jornada para recuperar a saúde , Vergèze, Thierry Souccar ,2012, 224 p. ( ISBN 978-2-36549-001-6 ).
- Chantal Perrin e Roger Lenglet , O caso da doença de Lyme: uma investigação , Arles, Actes Sud ,2016, 155 p. ( ISBN 978-2-330-05800-5 , apresentação online ).
- Christian Perronne , The Truth About Lyme Disease: Hidden Infections, Shattered Lives: Towards a New Medicine , Paris, Odile Jacob ,2017, 298 p. ( ISBN 978-2-7381-3509-4 , apresentação online ).
Filmografia
- Ryszard Hunka, roteiro e direção; Erna Buffie & Merit Jensen-Carr, produção; Sandra Moore, gerente de produção; David McGunigal, publicação; Annick Bergeron, narração, O mistério da doença de Lyme , Canada Media Fund / Rogers Documentary and Cable Network Fund / CBC / France 5 ,10 de outubro de 2013, “Na última década, a doença de Lyme, uma doença misteriosa transmitida por carrapatos, se espalhou a uma taxa alarmante no Canadá. O documentário explora esse flagelo devastador, muitas vezes mal diagnosticado e, portanto, mal tratado, que continua a gerar polêmica. Investigação de um mistério médico. » ( Leia online [vídeo] )
- Doença de Lyme: quando os carrapatos atacam! Documentário francês transmitido na France 5 em 2014 e produzido em 2014, 52 '. Página da Web (descrição) .
- Axel na terra dos pacientes imaginários , documentário francês transmitido na França 3 Pays de la Loire, em novembro de 2020, 52 min . “ Axel na terra dos pacientes imaginários ” , em france.tv .
Artigos relacionados
- Ecoepidemiologia
- Doença emergente
- Borreliose
- Doenças transmitidas por carrapatos
- Síndrome de ativação de mastócitos
links externos
- Pesquisa nacional sobre mapeamento de mordidas na França
- " Doença de Lyme " , no Ministério de Assuntos Sociais e Saúde (França) ,18 de janeiro de 2017(acessado em 26 de janeiro de 2017 )
- Jean-Paul Krivine , “ Lyme disease: between psychosis and false information ” , SPS n o 321 , em pseudo-sciences.org , AFIS,julho de 2017(acessado em 15 de agosto de 2017 )
- Aurélie Haroche , " Diseases of" no Lyme ": nossa sociedade ignorou o sofrimento de " no Medicine International Journal ,28 de março de 2018(acessado em 6 de abril de 2018 )
- https://socialyme.com blog e informações sobre a doença de Lyme
- Registros de autoridade :
- Avisos em dicionários gerais ou enciclopédias :
- Recursos relacionados à saúde :
- NCI Thesaurus
- Orphanet
- (en) Ontologia de doenças
- (en) DiseasesDB
- (en + es) Centro de Informação de Doenças Raras e Genéticas
- (en) Títulos de Assuntos Médicos
- (en + es) MedlinePlus
- (cs + sk) WikiSkripta