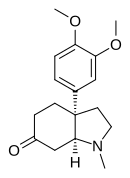
Mesembrine
| Mesembrine | |
|
|
| Identificação | |
|---|---|
| Nome IUPAC | (3a S , 7a S ) -3a- (3,4-dimetoxifenil) -1-metilocta-hidro-6H-indol-6-ona |
| N o CAS |
[(+) - (3aR, 7aR)] [(-) - (3aS, 7aS)] |
| PubChem | 193296 |
| SORRISOS |
COc1ccc (cc1OC) [C @@] 23CCC (= O) C [C @ H] 3N (C) CC2 , |
| InChI |
InChI: InChI = 1 / C17H23NO3 / c1-18-9-8-17 (7-6-13 (19) 11-16 (17) 18) 12-4-5-14 (20-2) 15 ( 10-12) 21-3 / h4-5,10,16H, 6-9,11H2,1-3H3 / t16-, 17- / m1 / s1 |
| Propriedades quimicas | |
| Fórmula bruta |
C 17 H 23 N O 3 [Isômeros] |
| Massa molar | 289,3694 ± 0,0163 g / mol C 70,56%, H 8,01%, N 4,84%, O 16,59%, |
| Unidades de SI e STP, salvo indicação em contrário. | |
O Mesembrine é um alcalóide indol presente em muitas plantas da família Aizoaceae como Mesembryanthemum crystallinum e Sceletium tortuosum (Kanna), ambos originários da África do Sul .
Estereoquímica
A mesembrina foi isolada e caracterizada pela primeira vez por K. Bodendorf e W. Krieger em 1957. A mesembrina é uma molécula bicíclica e tem dois átomos de carbono na cabeça da ponte quiral entre o anel de cinco membros e o anel de seis membros. As restrições estéricas não permitem a existência de um par de enantiômeros : a (+) - (3a R , 7a R ) -mésembrina e (-) - (3a S , 7a S ) -mésembrina. Os descritores de quiralidade a R e a S nesta molécula não se referem à quiralidade axial, mas correspondem ao sistema de numeração de átomos que atribui um "a" aos átomos da parte indol da molécula, conforme mostrado pelo número do ramo - 3a do Grupo 3,4-dimetoxifenil nesta parte. O isômero levógiro , (-) - mesembrina, constitui a forma natural. De facto, determinou-se, em 1970, resolvendo a estrutura cristalina metiodeto de derivado de 6-epimésembranol que é monoclínico , grupo espaço P 2 1 ( n o 4).
Propriedade
Na medicina tradicional, uma propriedade antidepressiva é atribuída a esse alcalóide. No rato, é observada uma inibição da recaptação da serotonina acompanhada por ataxia : este segundo efeito pode limitar o seu potencial terapêutico, embora o alcalóide pareça exibir baixa toxicidade in vivo . A mesembrina também é um inibidor da fosfodiesterase .
Síntese total
Devido à sua estrutura e bioatividade, a mesembrina tem sido um alvo através da síntese total desde a década de 1970. Mais de quarenta sínteses totais foram relatadas para a mesembrina, a maioria das quais se concentra em diferentes abordagens e estratégias para construir a célula. Sistema bicíclico e átomo de carbono quaternário .
A primeira síntese total da mesembrina foi relatada por Maurice Shamma e Herman R. Rodriguez em 1965. Essa rota sintética tem vinte e uma etapas, o que a coloca entre as mais longas para a mesembrina. As principais etapas incluem a construção do anel de seis membros com uma cetona pela reação de Diels-Alder , α - alilação para síntese de carbono quaternário e uma reação de adição de conjugado para o fechamento final do anel de cinco membros. O produto final desta rota sintética é a mistura racêmica de (+) - e (-) - mesembrina:
Em 1971, Shun-ichi Yamada relatou a primeira síntese assimétrica total de (+) - mesembrina. O carbono quaternário é introduzido por uma anelação assimétrica de Robinson promovida por um derivado de L-prolina .
Origens
- (en) / (de) Este artigo é parcial ou totalmente de artigos intitulados em inglês " Mesembrine " ( ver a lista de autores ) e alemão " Mesembrin " ( ver a lista de autores ) .
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- JS Glasby, ((Directory Of Plants Containing Secondary Metabolites , Taylor & Francis, London, New York, 1991, p. 780. ( ISBN 978-0-85066-423-2 ) .
- MT Smith, NR Crouch, N. Gericke, M. Hirst, Constituintes psicoativos do gênero Sceletium NEBr. e outros Mesembryanthemaceae: A Review , Journal of Ethnopharmacology, 1996, vol. 50 (3), pp. 119-130. DOI : 10.1016 / 0378-8741 (95) 01342-3 , .
- K. Bodendorf, W. Krieger ,, Arch. Pharm., 1957, vol. 290, pp. 441-448
- P. Coggon, DS Farrier, PW Jeffs, AT McPhail, A configuração absoluta de mesembrina e alcalóides relacionados: análise de raios-X de metiodeto de 6-epimesembranol. , J. Chem. Soc. B, 1970, pp. 1267–1271. DOI : 10.1039 / J29700001267 .
- Peter W. Jeffs, Richard L. Hawks, DS Farrier, Structure of the mesembranols and the absoluto configuration of mesembrine and related alkaloids , J. Am. Chem. Soc. , 1969, vol. 91 (14), pp. 3831–3839. DOI : 10.1021 / ja01042a025 .
- GI Stafford, ME Pedersen, J. van Staden, AK Jäger, Review on plants with CNS-effects used in medicina tradicional sul-africana contra doenças mentais , Journal of Ethnopharmacology, 2008, vol. 119 (3), pp. 513–537. DOI : 10.1016 / j.jep.2008.08.010 , .
- MJ Loria, Z. Ali et al., Effects of Sceletium tortuosum in rats , J Ethnopharmacol., 2014, vol. 155, pp. 731–735. DOI : 10.1016 / j.jep.2014.06.007 ,
- Uma avaliação de segurança toxicológica de um extrato padronizado de Sceletium tortuosum (Zembrin (®)) em ratos , Food Chem Toxicol., 2014, vol. 74, pp. 190–199. DOI : 10.1016 / j.fct.2014.09.017 , .
- AL Harvey, LC Young, AM Viljoen, NP Gericke, Ações farmacológicas da planta alimentar sul-africana medicinal e funcional Sceletium tortuosum e seus principais alcalóides , Journal of Ethnopharmacology, 2011, vol. 137 (3), pp. 1124–1129. DOI : 10.1016 / j.jep.2011.07.035 , .
- Maurice Shamma, Herman R. Rodriguez, A síntese total de (±) -mesembrine , Tetrahedron Lett., 1965, vol. 6 (52), pág. 4847-4851. DOI : 10.1016 / S0040-4039 (01) 89046-8 .
- Shun-ichi Yamada, síntese total de (+) - mesembrina por síntese assimétrica com aminoácido , Tetrahedron Lett., 1971, vol. 12 (16), pp. 1133-1136. DOI : 10.1016 / S0040-4039 (01) 96647-X .