Óxido de lítio
| Óxido de lítio | |
| |
| Identificação | |
|---|---|
| Sinônimos |
litina, óxido de litina |
| N o CAS | |
| N o ECHA | 100.031.823 |
| N o EC | 235-019-5 |
| Aparência | em pó |
| Propriedades quimicas | |
| Fórmula bruta |
Li 2 O [isômeros] |
| Massa molar | 29,881 ± 0,004 g / mol Li 46,46%, O 53,54%, |
| Propriedades físicas | |
| Fusão T ° | 1.570 ° C |
| Solubilidade | Hidrólise violenta em LiOH |
| Massa volumica | 2013 kg · m -3 |
| Cristalografia | |
| Símbolo Pearson | |
| Classe de cristal ou grupo espacial | Fm 3 m (n ° 225) |
| Strukturbericht | C1 |
| Estrutura típica | CaF 2 |
| Precauções | |
| WHMIS | |
 E, E : O material corrosivo em contato com a água forma uma substância corrosiva: hidróxido de lítio Divulgação a 1,0% de acordo com os critérios de classificação |
|
| Diretiva 67/548 / EEC | |
 VS Símbolos : C : Corrosivo Frases R : R34 : Provoca queimaduras. Frases S : S26 : Em caso de contato com os olhos, lavar imediata e abundantemente com água e consultar um especialista. S45 : Em caso de acidente ou mal-estar, consulte imediatamente um médico (mostre o rótulo sempre que possível). S36 / 37/39 : Use roupas de proteção adequadas, luvas e proteção para os olhos / face. Frases R : 34, Frases S : 26, 36/37/39, 45, |
|
| Unidades de SI e STP, salvo indicação em contrário. | |
O óxido de lítio é um composto químico da fórmula Li 2 O. É formado com pequenas quantidades de hidróxido de lítio LiOH quando o metal de lítio queima no ar e é combinado com o oxigênio e a água do ar:
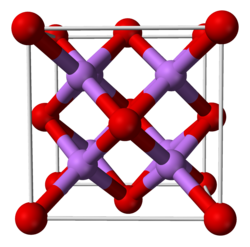
4 Li + O 2→ 2 Li 2 O 4 Li + 2 H 2 O + O 2 → 4 LiOHO óxido de lítio tem no estado sólido uma estrutura cristalina do tipo antifluorina, ou seja, uma estrutura modelada na do fluoreto de cálcio CaF 2, mas onde os cátions e ânions desempenham papel oposto. No estado de gás fundamental, a molécula de Li 2 O é linear, ao contrário dos resultados previstos pela teoria VSEPR (segundo a qual a molécula de Li 2 O deve ter a mesma forma que a molécula de H 2 O ), o que é consistente com um geometria governada por ligações iônicas.
Li 2 O resulta da decomposição térmica do peróxido de lítio Li 2 O 2e ataca a sílica em temperatura elevada.
Referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- " The Fluorite (C1) Structure " , em http://cst-www.nrl.navy.mil/ (acessado em 17 de dezembro de 2009 )
- " Óxido de lítio " no banco de dados de produtos químicos Reptox da CSST (organização de Quebec responsável pela segurança e saúde ocupacional), acessado em 25 de abril de 2009
