Reação de eliminação
Em química orgânica , a eliminação (ou β-eliminação ) é uma reação orgânica que transforma um alcano substituído ( haloalcanos , álcoois, etc.) em um derivado de etileno, ou mesmo em um alceno , se a molécula de partida, além do grupo de saída , n 'é apenas uma cadeia de carbono do tipo alcano.
As condições são, além de severas, as de uma substituição nucleofílica , uma reação semelhante em muitos aspectos e concorrente: a eliminação ocorre na presença de uma base forte e pelo aquecimento da mistura de reação.
Equação geral
Um dos principais exemplos de eliminação é a conversão de um haloalcano em um alceno ; então falamos de desidrohalogenação :
As bases mais comumente usadas são refrigerante (Na + , HO - ), potássio (K + , HO - ), até íons alcoolato (RO - ) (obtidos pela reação de sódio em um álcool ROH, anidro ).
Assim como para a substituição nucleofílica, há uma eliminação monomolecular e uma eliminação bimolecular que é comumente conhecida como E1 e E2, respectivamente.
No restante deste artigo, os exemplos são dados com um derivado halogenado como reagente.
Eliminação monomolecular
Cinética E1
A reação de eliminação monomolecular é realizada em dois estágios: um estágio monomolecular que envolve apenas a molécula do derivado halogenado do lado do reagente, que é o estágio cineticamente limitante, seguido por um estágio bimolecular. Consequentemente, a cinética da reação, na aproximação da etapa cinética determinante (ou limitante ), depende apenas da concentração da espécie RX.
A reação é, portanto, caracterizada por uma cinética de ordem geral 1, de ordens parciais 1 em relação à derivada halogenada e 0 em relação à base B | : v = k. [RX] , onde:
- [RX] representa a concentração do derivado halogenado em mol.L −1
- v representa a taxa da reação de eliminação. É expresso em mol.s -1 .
- k é a constante de velocidade: é de fato aquela da etapa cineticamente limitante (k 1 ). Sua unidade, Ls −1 , é deduzida das dos outros dois termos.
Mecanismo de E1
A reação ocorre em duas etapas.
- Primeiro passo: partida do nucleófugo, formação de um carbocátion. esta etapa de formação de carbocátions é uma etapa lenta e reversível e impõe sua velocidade em toda a reação.
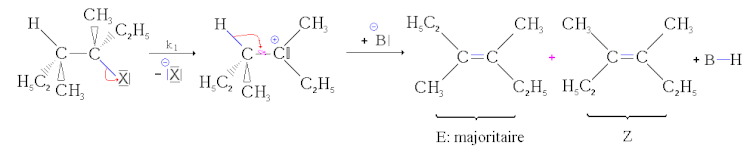
- Segunda etapa: reação ácido-base. A base arranca o próton. O dupleto então "dobra" sobre a ligação carbono-carbono para formar uma ligação dupla . Uma vez que a ligação simples carbono-carbono pode girar, dois estereoisômeros podem se formar. Como essa reação é muito mais rápida que a anterior, sua velocidade não influencia a velocidade geral.

Estereosseletividade e regiosseletividade
EstereoquímicaConforme mostrado pelo mecanismo, a passagem por um carbocátion, que é uma estrutura plana, remove qualquer elemento de estereoespecificidade, ao contrário (veja a seguir) do mecanismo de eliminação bimolecular.
Mas, se dois estereoisômeros geométricos podem se formar, eles não se formam nas mesmas proporções. O isômero mais estável, ou seja, o de menor energia, é formado predominantemente (é a regra de Zaitsev). É, portanto, o isômero E que se forma principalmente na ausência de mesomério. Por outro lado, se a dupla ligação de apenas um dos dois produtos pode ser deslocalizada pelo mesomério, então é esta que será formada principalmente. Isso é chamado de estereosseletividade parcial.
 Regioquímica
Regioquímica
Quando vários isômeros constitucionais podem ser formados, o alceno termodinamicamente mais estável é preferencialmente formado. Se houver apenas grupos alquil, este é o alqueno mais substituído. Se a mesomeria pode intervir, é o alceno mais conjugado que está na maioria. Isso é conhecido como regiosseletividade ou regra de Zaïtsev .
No entanto, às vezes, o alceno menos estável termodinamicamente é formado preferencialmente, isso é conhecido como eliminação de Hofmann . Este é particularmente o caso quando a base usada está congestionada (por exemplo, KtBuO) ou quando há um íon amônio que é eliminado, por exemplo. (Molécula que carrega uma amina na presença de MeI em um número de equivalentes suficientes para formar o sal de amônio, então colocada na presença de óxido de prata úmido e aquecido. Formação do alceno por eliminação de Hofmann e, portanto, partida. De N (Me ) 3.)
Fatores que influenciam a resposta
Os parâmetros que influenciam a eliminação E1 são:
- o efeito de R-: a etapa cineticamente determinante é a formação do carbocátion (e não sua reatividade), portanto, quanto mais estável, mais favorecida a reação.
- a nucleófuga: a clivagem da ligação do grupo de saída C sendo a etapa chave no mecanismo, a reação depende fortemente da natureza desta nucleófaga. Quanto melhor for o grupo inicial, mais rápida será a reação. Por exemplo, para a desidratação de álcoois, a primeira etapa é a protonação do álcool para formar um oxônio e, portanto, um melhor grupo de saída (H 2 O⇒HO - ). Uma classificação rápida dos grupos iniciais seria:
(o sinal ">" significa: "melhor grupo inicial do que")
Note que a base não influencia este tipo de reação de ordem 1 e esta na medida em que não intervém durante a primeira etapa que determina a velocidade global da reação.
Grupo alquil do derivado de halogênioO mecanismo passa por um intermediário de reação do tipo carbocátion. Este último é tanto mais estável quanto mais é substituído. Assim, a taxa de reação (portanto de formação do carbocátion) progride dos derivados primários para os secundários e depois para os terciários. Na prática, apenas o último, e alguns derivados secundários, reagem por esse mecanismo.
NucleofugeQuanto mais polarizável for o link RX, mais fácil será quebrá-lo. Esta ligação é, portanto, de labilidade decrescente ("fragilidade") de flúor para iodo: F> Cl> Br> I.
(o símbolo ">" significa: "mais rápido que")
Solvente- Polaridade: um solvente polar estabiliza o carbocátion; assim, torna a primeira reação mais fácil. A velocidade, portanto, aumenta com a polaridade do solvente.
- Proticidade: um solvente prótico é mais uma desvantagem: na verdade, corre o risco de competir com o carbocátion durante a (forte) reação ácido-base.
Concorrência
Esta reação não compete apenas com a outra eliminação, mas também com as reações de substituições nucleofílicas, em particular com S N 1 . Este último ocorre de fato em condições semelhantes (exceto aquecimento).
Eliminação bimolecular
Cinética
A reação de eliminação bimolecular tem uma cinética de ordem global 2 e ordem parcial 1 em relação ao derivado halogenado RX e à base B: - . A reação ocorre em uma única etapa, que é bimolecular, portanto, a velocidade da reação segue uma lei de tipo: v = k. [RX]. [B: - ] .
ou :
- [RX] representa a concentração do derivado halogenado (expresso em mol.L -1)
- [B: - ] representa a concentração de base (expressa em mol.L −1 )
- v representa a taxa da reação de eliminação. É expresso em mol.s -1 .
- k é a constante de taxa. Sua unidade, Ls −1 .mol −1 , é deduzida das dos outros dois termos.
Mecanismo de E2
A eliminação bimolecular é uma reação bimolecular de uma etapa.
Durante a mesma etapa elementar, ocorre o rompimento do próton pela base, a formação da ligação dupla e a saída do átomo de halogênio (nucleofuge) na forma de um íon haleto. Falamos de um mecanismo síncrono ou combinado.
Estereoquímica
E2 é uma reação estereoespecífica .
A reação só ocorre quando o hidrogênio e o grupo de saída estão na posição anti-pleurplanar .
Fatores que influenciam a resposta
- A taxa de reação de um E2 varia apenas ligeiramente dependendo da classe (primária: I, secundária: II, terciária: III) do haleto considerado. Porém, quanto maior a classe, mais rápida é a reação (III> II> I) por razões estéricas (a eliminação permite remover substituintes volumosos, e portanto "volumosos" no produto final, presentes no produto inicial, o reagente , uma vez que se passa de um ângulo de valência de 109 ° 28 'neste, ao nível do carbono "sp 3 ", levando o próton H, a um ângulo de valência de 120 °, no produto final onde este mesmo carbono está agora "hibridizado sp 2 "). Um haloalcano primário é geralmente preferido neste caso, mas quando um está na presença de um haloalcano secundário, as reações do tipo E1 e E2 são distinguidas pelos efeitos mesoméricos potenciais ( efeito de "mesômero": termo geral que define um efeito eletrônico correspondente a uma deslocalização da carga, aqui positiva, sobre um grupo Arilo, por exemplo, um vizinho imediato, portanto "em α", da ligação CH rompida, fala-se de "desprotonação", pela base forte). Qualquer substituinte na cadeia de carbono capaz de estabilizar o íon carbênio (carbocátion C + ) por meio desse tipo de efeito eletrônico irá promover o mecanismo E1.
- A velocidade de reação aumenta com a força da base, portanto, uma base forte é necessária.
- O caráter de nucleofuga do grupo de saída também tem influência na reação, mas essa influência não é o parâmetro principal, ao contrário do mecanismo de eliminação unimolecular (E1).
- Para promover um mecanismo de reação de eliminação bimolecular de E2, é sensato usar um solvente aprótico (DMSO, THF, tolueno, n-hexano, etc.)
Concorrência
Esta reação compete não apenas com E1, mas também com reações de substituição nucleofílica, em particular com S N 2 , que ocorre em condições semelhantes. Observe que uma reação de eliminação exigirá mais energia do que uma reação de substituição correspondente, geralmente por meio de aquecimento.
Observações
A base usada também é um nucleófilo . Isso explica a competição com as reações das substituições. Ao final da reação, encontram-se, misturados, produtos de eliminação e produtos substitutos.