Sulfeto de ferro (II)
| Sulfeto de ferro (II) | |

| |
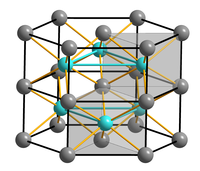 __ Fe 2+ __ S 2- Estrutura de sulfeto de ferro (II) |
|
| Identificação | |
|---|---|
| Nome IUPAC | Sulfeto de ferro (II) |
| Sinônimos |
sulfureto de ferro, sulfureto ferroso, sulfureto de ferro preto |
| N o CAS | |
| N o ECHA | 100.013.881 |
| N o EC | 215-268-6 |
| PubChem | |
| Aparência | Cinza de carvão sólido a preto metálico na aparência com cristais planos ou em forma de haste |
| Propriedades quimicas | |
| Fórmula bruta | FeS |
| Massa molar | 87,91 ± 0,007 g / mol Fe 63,53%, S 36,48%, |
| Propriedades físicas | |
| Fusão T ° | 1.195 ° C |
| Solubilidade | Ks = 10 -16,4 |
| Massa volumica | 4,84 g · cm -3 ( 20 ° C ) |
| Termoquímica | |
| S 0 sólido | 60,3 J · K -1 · mol -1 a 25 ° C |
| Δ f H 0 sólido | -100,0 kJ · mol -1 a 25 ° C |
| Δ fus H ° | 31,5 kJ · mol -1 a 1188 ° C |
| C p | 50,5 J · K -1 · mol -1 ( 25 ° C , cristais) |
| Cristalografia | |
| Estrutura típica | NiAs |
| Unidades de SI e STP, salvo indicação em contrário. | |
O sulfeto de ferro (II) , também conhecido como sulfeto ferroso , é o composto químico de fórmula FeS. Como o óxido de ferro (II) , é um composto não estequiométrico . É pirofórico (inflama espontaneamente no ar) em um estado pulverulento .
Diferentes sulfuretos de ferro
Existem várias variedades de sulfuretos de ferro, que diferem entre si em sua estequiometria e propriedades, apresentando certas analogias com os óxidos correspondentes:
- a pirrotita , um ferromagnético inorgânico , como o ferro, de fórmula Fe 1-x Scristalizando no sistema monoclínico.
- a troilita , uma variedade estequiométrica pirrotita, fórmula FeS com uma simetria hexagonal
- o mackinawite , o menos estável dos sulfetos de ferro, com estrutura de fórmula Fe camadas 1 + x S
- a pirita e marcassita , de minerais diamagnéticos , que são dissulfeto de ferro (II) de fórmula FeS 2
- a greigita , sulfeto de ferro (II, III) da fórmula Fe 3 O 4análogo à magnetita Fe 3 O 4quanto às suas propriedades ferromagnéticas .
O sulfeto de ferro (III) da fórmula Fe 2 O 3, é bastante instável e tende a se dissociar em enxofre e sulfeto de ferro (II).
Reações químicas
No laboratório, o sulfeto de ferro (II) pode ser obtido pela reação direta de ferro elementar e enxofre , em uma reação exotérmica :
Fe + S → FeSSulfeto de ferro (II) reage com ácido clorídrico para dar cloreto de ferro (II) e sulfeto de hidrogênio :
FeS + 2 HCl → FeCl 2+ H 2 SBioquímica e biologia
Em um ambiente hipóxico , as bactérias redutoras de sulfato podem degradar a matéria orgânica oxidando-a com sulfatos dissolvidos em água, que libera sulfeto de hidrogênio, que pode reagir com íons metálicos dissolvidos para produzir sulfetos de metais insolúveis; esses compostos, como o sulfeto de ferro (II), costumam ser marrons ou pretos, conferindo uma cor escura ao ambiente em que são depositados.
A presença de um precipitado negro de sulfeto de ferro (II) em meio de cultura rico em ferro ( ágar-ágar , ferro e peptona ) permite identificar os microrganismos que metabolizam a cisteína por meio da cisteína desulfidrase , enzima que libera sulfeto de hidrogênio. , que reage com o citrato de ferro para formar sulfeto de ferro (II).
A mesma reação entre H 2 Se o ferro ocorre durante o cozimento de ovos cozidos , na interface entre a gema e a clara : o ferro da gema oxida em contato com o sulfeto de hidrogênio liberado pelo cozimento da clara para formar uma camada acastanhada de ferro sulfuroso ( II) em contato entre as duas partes do ovo.
Notas e referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- Entry "Iron (II) sulfide" no banco de dados química GESTIS da IFA (organismo alemão responsável pela segurança e saúde ocupacional) ( alemão , Inglês ), acessado 01 de maio de 2010 (JavaScript obrigatório)
- "Sulfeto ferroso" no Banco de dados de substâncias perigosas , acessado em 1º de maio de 2010
- (em) Bodie E. Douglas, Shih-Ming Ho, Structure and Chemistry of Crystalline Solids , Pittsburgh, PA, EUA, Springer Science + Business Media, Inc.,2006, 346 p. ( ISBN 0-387-26147-8 ) , p. 64
- D. Vaughan, J. Craig, Mineral Chemistry of Metal Sulfides , Cambridge University Press, 1978. ( ISBN 0-521-21489-0 )
- (in) A formação de sulfeto ferroso em ovos cozidos