Dihidrogênio
| Dihidrogênio | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificação | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome IUPAC | hidrogênio | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinônimos |
hidrogênio |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.014.187 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 215-605-7 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E949 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISOS |
[HH] , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H2 / h1H |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | gás comprimido inodoro, incolor | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades quimicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula |
H 2 [isômeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molar | 2,01588 ± 0,00014 g / mol H 100%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fusão T ° | -259,1 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fervendo | -252,76 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidade |
21,4 ml em 1 l de água (ou seja, 1,92 mg / l ) ( 0 ° C ) 8,5 ml em 1 l de água ( ou seja, 0,76 mg / l ) ( 80 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parâmetro de solubilidade δ | 6,9 MPa 1/2 ( 25 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
0,089 88 g / l (gás, CNTP ), 0,070 8 kg / l (líquido, −253 ° C ), equação:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Temperatura de autoignição | 500 a 571 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de inflamação | gás inflamável | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limites explosivos no ar | 4 - 76 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressão de vapor de saturação |
equação:
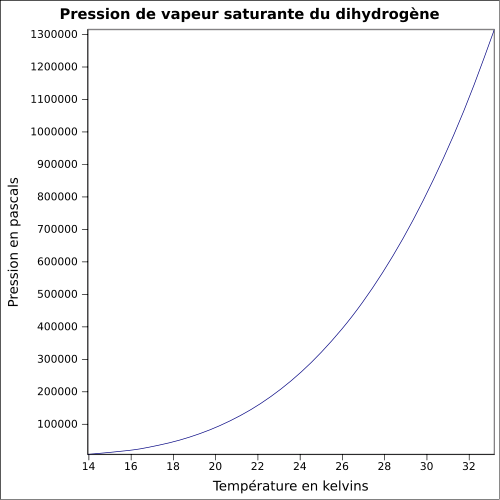
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto crítico | 13,0 bar, -239,95 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto Triplo |
-259,3467 ° C ; 7,205 kPa abs |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 42,5 × 10 −5 cal cm −1 s −1 K −1 a 16,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidade do som | 1310 m s −1 ( 27 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gás, 1 bar | 130,68 J K −1 mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ fus H ° | 0,058 68 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° | 0,90 kJ mol −1 ( 1 atm , −252,76 ° C ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p | 14 266 J kg −1 K −1 a 293 K | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 285,8 kJ / mol ( 25 ° C , gás) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | 242,7 kJ / mol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauções | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Perigo H220 H220 : Gás extremamente inflamável |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  A, B1, A : Temperatura crítica do gás comprimido = −239,9 ° C B1 : Limite inferior de inflamabilidade do gás inflamável = 4,0% Divulgação a 1,0% de acordo com os critérios de classificação |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| gás:
4
0
0
líquido refrigerado: 4 3 0 |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transporte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
23 : gás inflamável Número UN : 1049 : HIDROGÊNIO COMPRIMIDO Classe: 2.1 Código de classificação: 1F : Gás comprimido, inflamável; Etiqueta: 2.1 : Gases inflamáveis (corresponde aos grupos designados por F maiúsculo); 
223 : gás liquefeito refrigerado, inflamável Número UN : 1966 : LÍQUIDO REFRIGERADO A HIDROGÊNIO Classe: 2.1 Código de classificação: 3F : Gás liquefeito refrigerado, inflamável; Etiqueta: 2.1 : Gases inflamáveis (corresponde aos grupos designados por F maiúsculo);  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inalação | asfixia | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI e STP, salvo indicação em contrário. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
O dihidrogênio é a forma molecular do elemento hidrogênio que existe como gás em condições padrão de temperatura e pressão . As moléculas têm dois átomos de hidrogênio; sua fórmula química é H 2 . É também denominado "hidrogênio molecular" ou, no estado gasoso, "gás hidrogênio". Na linguagem cotidiana, quando não há ambigüidade com o elemento químico de mesmo nome, ele é frequentemente referido simplesmente como "hidrogênio", e às vezes falamos simplesmente de "molécula de hidrogênio" para a molécula de hidrogênio.
Foi usado em aeronaves do tipo zepelim , com as propriedades de empuxo de Arquimedes , antes de ser substituído pelo hélio , que é menos perigoso por não ser combustível. Hoje, o consumo global de hidrogênio é de cerca de 50 milhões de toneladas por ano. A maior parte da produção de hidrogênio é consumida localmente, principalmente na indústria química e petroquímica: síntese de amônia (50%), refino e dessulfuração de hidrocarbonetos (37%), síntese de metanol (12%). É feito 96% de hidrocarbonetos (metano, petróleo, carvão) e 4% por eletrólise da água . Essa produção é acompanhada em 2020 pela produção de 830 milhões de toneladas de CO 2por ano, ou cerca de 2% das emissões globais .
É um gás leve que a gravidade da Terra não pode conter. Ele queima no ar produzindo água , daí seu nome composto pelo prefixo "hidro", do grego ὕδωρ (hudôr) que significa "água", e pelo sufixo "gene", do grego γεννᾰν (gennen), "Gerar" . Tem sido usado principalmente para conservar carne . Di-hidrogenofosfato tem uma temperatura de vaporização de 20,27 K e uma temperatura de fusão de 14,02 K . Sob pressões muito altas , como as que existem no centro dos gigantes gasosos , essas moléculas se dissociam e o hidrogênio se torna um metal líquido. No espaço, as nuvens de H 2 são a base do processo de formação estelar .
Histórico
O primeiro cientista conhecido a descrever a produção de dihidrogênio foi o suíço Paracelsus (1493-1541). Ele fez essa descoberta derramando vitríolo sobre o pó de ferro , mas não entendeu a natureza exata do gás liberado durante o experimento .
O químico inglês Henry Cavendish (1731-1810), repetindo as experiências de Paracelso com diversos metais diferentes, descobre que o gás assim produzido é diferente do ar, é inflamável e tem baixa densidade. Ele chamou esse gás de "ar inflamável" (em inglês: ar inflamável ) e descobriu que é o produto da combustão da água . O dioxigênio sendo ele denominado "ar vital".
O químico francês Antoine Lavoisier, tendo confirmado as experiências de Cavendish, propõe a palavra "hidrogénio" em substituição da expressão "ar inflamável". Esta palavra é formada com o prefixo hidro (do grego ὕδωρ (hudôr), “água”) e o sufixo gene (do grego γεννᾰν (gennen), “gerar”). A palavra hidrogênio, portanto, significa que gera água .
Posteriormente, no campo científico, a palavra "hidrogênio" será usada para denominar o elemento químico H e a palavra "hidrogênio" para a molécula H 2 .
Propriedades quimicas
Teste de Reconhecimento
Para testar a presença de dihidrogênio, um registro em chamas é aproximado de um tubo de ensaio contendo dihidrogênio. A reação química de combustão do hidrogênio com o oxigênio do ar, iniciada pela fonte de calor, produz um ruído característico denominado "latido" ou "latido".
Combustão
A combustão do hidrogênio em dioxigênio , que produz água , é 2 H 2 (g) + O 2(g) → 2 H 2 O(a). É particularmente violento (ver teste de reconhecimento) e muito exotérmico : seu valor calorífico é 141,86 MJ / kg [ou 141,79 MJ / kg ] (a 25 ° C [ou 15 ° C ] abaixo de 1 atm ), ou uma entalpia padrão de combustão , a 25 ° C , de −285,84 kJ / mol , a 100 ° C , de −283,45 kJ / mo l ( gás H 2 , gás O 2 , mas H 2 O líquido , como maior poder calorífico ou PCS), mas de 120,1 MJ / kg [ou 119,93 MJ / kg ], ou seja , uma entalpia de combustão, a 100 ° C , de -242,8 kJ / mol ( gás H 2 , O 2 gasoso, vapor de H 2 O , como valor calorífico inferior ou NCV , contando 40,660 kJ / mol para a vaporização de água a 100 ° C ), contra, por exemplo, apenas 49,51 MJ / kg para butano . Esta propriedade o torna um combustível de escolha para espaçonaves, mas torna seu armazenamento perigoso.
A mesma oxidação mais lenta é usada para produzir eletricidade na célula de combustível .
Formas orto e para
O gás hidrogênio é uma mistura de dois tipos de moléculas isoméricas que diferem entre si na rotação de seus núcleos atômicos . Essas duas formas são chamadas de orto e para-hidrogênio , e a forma orto (spins paralelos, estado tripleto) corresponde a um estado excitado que não existe em seu estado puro. Sob condições normais de temperatura e pressão , por excitação térmica, o hidrogênio é composto de 75% da forma orto e 25% da forma para. A 77 K a mistura em equilíbrio (atingida espontaneamente em vários dias, mas em poucas horas com catalisadores) está em 50%. Mas em temperaturas muito baixas, a forma orto se transforma completamente no estado para (spins antiparalelos, estado singlete) com o tempo. As duas formas têm níveis de energia ligeiramente diferentes e, portanto, propriedades físico-químicas ligeiramente diferentes . Por exemplo, o ponto de fusão e o ponto de ebulição do para-hidrogênio são cerca de 0,1 K menores do que o de orto- .
Fontes de hidrogênio
Dihidrogênio é um gás muito leve. Uma vez que a gravidade da Terra não pode segurá-lo, ele escapa naturalmente da atmosfera terrestre. Portanto, está presente apenas em pequenas quantidades (0,5 ppmv ) no ar . Essa escassez atmosférica significa que todo o di-hidrogênio usado é produzido industrialmente por vários processos, a partir de moléculas onde os átomos de hidrogênio estão quimicamente ligados.
No entanto, existem alguns contextos geológicos onde o dihidrogênio surge naturalmente da Terra . O hidrogênio que emana dessas zonas é designado pelo termo hidrogênio natural .
Hidrogênio artificial
A produção de hidrogênio envolve muitos processos diferentes , o átomo de hidrogênio formando várias moléculas ( água , hidrocarbonetos , açúcares , etc. ).
Método histórico de produçãoHistoricamente, na XIX th século, o di-hidrogenofosfato foi obtida por emissão de vapor de água (H 2 O) em um tambor cheio com limalha de ferro e fichas. O vapor d'água oxidou o metal, criando óxido de ferro de um lado e liberando hidrogênio do outro. Este último então saiu do barril, onde foi filtrado para outro barril cheio de água e armazenado diretamente em um aeróstato . Este dispositivo permitiu ao exército encher um balão de observação em qualquer lugar e em poucas horas .
Métodos atuaisEm 2015, o hidrogênio foi produzido industrialmente por vários processos:
- para 49% por reforma a vapor de hidrocarbonetos (em particular de metano , consulte Reforma de metano );
- para 29% por oxidação parcial do petróleo
- para 18% por gaseificação de carvão
- para 4% por eletrólise da água .
Outros processos também estão sendo estudados, desde craqueamento ou oxidação parcial, que tem a vantagem de ser exotérmico .
Reforma de vapor de hidrocarbonetoO vapor de reformação de hidrocarbonetos é o método que no início do XXI th século, é o mais utilizado à escala industrial. Seu princípio é baseado na reação de hidrocarbonetos (metano, etc.) na presença de vapor d'água e calor. A reação global está escrita:
.A eficiência energética é de cerca de 40 a 45% em algumas instalações . Na prática industrial, é necessário acelerar a reação por meio de catalisadores ou queimadores. Tem a desvantagem de produzir dióxido de carbono , um gás de efeito estufa .
Tecnologias catalíticas, ou mais inovadoras, como reformadores de plasma, estão atualmente em estudo.
Eletrólise de águaA eletrólise da água é uma tecnologia que consiste em passar uma corrente elétrica (direta) na água (à qual foi previamente adicionado um eletrólito como a soda cáustica ) para obter a dissociação das moléculas da água em hidrogênio e oxigênio .
Reação no ânodo :
2 H 2 O(l) → O 2(g) + 4 H + (aq) + 4 e -Reação no cátodo :
4 H 2 O(l) + 4 e - → 2 H 2 (g) + 4 OH - (aq)Reação na água:
4 H + (aq) + 4 OH - (aq) → 4 H 2 O (a)Reação geral:
2 H 2 O(l) → 2 H 2 (g) + O 2 (g)onde (l), (g) e (aq) significam "em fase líquida", "em fase gasosa" e "em solução aquosa", respectivamente.
Essa tecnologia requer grandes quantidades de eletricidade. De acordo com a Ademe, em 2020, a eficiência da cadeia do hidrogênio em Power-to-H2-to-Power é de 25%, enquanto a das baterias elétricas é de 70%. Portanto, é relativamente pouco usado.
Oxidação parcial de hidrocarbonetosEsta reação é uma combustão “rica” no sentido de que o objetivo é produzir um gás rico em H 2 e CO (gás de síntese); em vez dos produtos “clássicos” de CO 2 e H 2 O.
A reação está escrita:
.Na maioria das vezes, o ar é usado como oxidante. Então temos:
.A reação é exotérmica: por exemplo, a entalpia da reação com o metano é −35,7 kJ mol −1 .
Como na reação de reforma a vapor, é necessário catalisar a reação.
O interesse da reação de oxidação parcial reside na sua natureza exotérmica (ao contrário da reação de reforma a vapor), que ajuda a catálise (aumento da temperatura).
A principal desvantagem reside no fato de que as porcentagens de H 2 são menores do que as obtidas pela reforma a vapor, devido à presença majoritária de nitrogênio no ar. Além disso, existe o risco de obtenção de NO x .
Ação de um ácido sobre um metalDihidrogênio é produzido pela ação de um ácido sobre um metal. Exemplo :
.Dihidrogênio também pode ser produzido pela reação de hidróxido de sódio com alumínio, de acordo com a fórmula:
Produção por fotossíntese (cianobactérias)Algumas cianobactérias podem quebrar quimicamente a água em oxigênio e hidrogênio usando reações fotossintéticas. Isso possibilitaria a produção de hidrogênio a partir da energia solar . Pesquisas estão em andamento nesta área, principalmente em termos de engenharia genética .
Hidrogênio natural
O hidrogênio produzido na Terra naturalmente, ao contrário do hidrogênio produzido artificialmente pela reforma do metano ou dos hidrocarbonetos , é denominado hidrogênio natural ou hidrogênio nativo .
A distribuição, capacidade de produção e os mecanismos físico-químicas de suas fontes ou depósitos são ainda objecto de estudos exploratórios no início do XXI th século. Assim, em abril de 2019, foi lançado e cofinanciado pela Agência Espacial Europeia o projeto de investigação sen4H2 , que visa detetar emissões de hidrogénio natural a partir de imagens de satélite.
Fontes de hidrogênio naturalA produção de hidrogênio natural na espinha dorsal é conhecida desde a década de 1970 e estudada mais recentemente. São reações de serpentinização ( redox de olivina ) entre a água e as rochas ígneas rentes ao manto terrestre , facilitadas pelo calor dessas reações exotérmicas : o oxigênio das moléculas de H 2 O.capturados pelo ferro na rocha, os átomos de hidrogênio são livres para se associar em H 2. O hidrogênio assim produzido escapa através de respiradouros hidrotérmicos e pode, opcionalmente, reagir para formar metano , e então hidrocarbonetos mais pesados. Muito profundos, esses depósitos não podem ser explorados em 2018
As emissões de hidrogênio também foram descobertas no meio dos crátons continentais pelo geólogo russo Nicolay Larin, após seu trabalho sobre a hipótese da Terra hidratada. A IFP Energies nouvelles confirmou esta descoberta em 2013, relatando questões localmente importantes, na maioria dos continentes, Rússia , Estados Unidos , no Brasil , em Omã ou Mali .
O fenômeno ainda é pouco compreendido e o debate sobre o mecanismo exato que gera essas emissões ainda não foi encerrado. Poderia ser sobre a hidratação do ferro por água infiltrada, esta presente nas faixas de greenstone , presente nos crátons. Assim, em Kansas , perto de Junction City , um depósito foi identificado na década de 1980 e foi objeto de renovado interesse na década de 2000; o dihidrogênio seria obtido a partir de tais reações de oxidação do ferro. Na Rússia, o IFP estimou em 2010 o fluxo diário de uma única depressão em várias dezenas de milhares de metros cúbicos , ou o consumo equivalente a 500 táxis. Um geológico ou hidrogeológico original também prevalece para as liberações de hidrogênio estudadas no Brasil, em alguns círculos de fadas localizados na bacia do São Francisco .
Em Yanartaş , Turquia, os "fogos milenares" do Monte Quimera seriam a combustão de um gás composto de metano (87%), hidrogênio (7,5 a 11%) e dinitrogênio (2 a 4,9%), tendo uma origem dupla: o serpentinização, por um lado, um gás termogênico, por outro. Eles seriam a fonte original da chama olímpica .
O Mali é, em 2015, o único país onde é aproveitado o hidrogénio natural, na aldeia de Bourakébougou , 60 quilómetros a norte de Bamako . O gás viria de um "amadurecimento excessivo do petróleo" provavelmente enterrado nas proximidades e suas reservas são estimadas em cerca de 1,5 bilhão de metros cúbicos . A pressão nos poços não diminui, por isso o aterro é constantemente enchido, o que permite a sustentabilidade desta operação.
Os gases vulcânicos geralmente contêm vestígios de hidrogênio. Assim, no Havaí, um estudo espectroscópico realizado em um incêndio de gás vulcânico mostrou que se tratava de uma combustão de dihidrogênio.
Qualquer rocha ígnea conteria hidrogênio, até cerca de 5 l / m 3 ; portanto, todos os furos mostram desgaseificação de hidrogênio. Durante o experimento russo de perfuração sg3 , a lama extraída do buraco foi descrita como borbulhando com este gás .
DesafiosAo contrário do hidrogênio artificial, que exige energia para ser produzida, o que o reduz a ser apenas um portador de energia , o hidrogênio natural é uma verdadeira fonte de energia , cuja combustão não produz apenas água. Além disso, co-produções poderiam ser possíveis com energia geotérmica ou extração de hélio , o que poderia ajudar o setor a ser competitivo. No entanto, em 2020, o potencial industrial não é quantificado com precisão e a legislação de mineração não leva o hidrogênio em consideração em muitos países. A detecção de hidrogênio in situ é realmente difícil, embora detectores mais eficientes tenham sido desenvolvidos.
Usos industriais
O consumo global de hidrogênio hoje é de cerca de 50 milhões de toneladas por ano. A maior parte da produção de hidrogênio é consumida localmente, principalmente na indústria química e petroquímica: síntese de amônia (50%), refino e dessulfuração de hidrocarbonetos (37%), síntese de metanol (12%).
Os principais usos industriais do hidrogênio são:
- o método Haber-Bosch (produção de amônia ), a hidrogenação de gorduras e óleos e a produção de metanol ;
- a fabricação de ácido clorídrico , a soldagem , os combustíveis para foguete e a redução de minérios de metal;
- o dihidrogênio líquido é usado para pesquisas em temperaturas muito baixas, incluindo o estudo da supercondutividade ;
- o hidrogênio é utilizado como gás traçador para realizar operações de detecção de vazamentos em diversos campos (refino de petróleo, automóveis, instalações de aquecimento, rede de distribuição de água, tanques de aeronaves, etc.);
- o hidrogênio é um aditivo alimentar autorizado sob o código E949 , na categoria dos traçadores;
- o hidrogênio também é usado como fluido de transferência de calor em certas máquinas de alta potência (alternador de usina síncrona, por exemplo);
- o hidrogênio foi usado em aeróstatos porque é catorze vezes menos denso que o ar, mas foi substituído pelo hélio por razões de segurança; ainda é usado para alguns balões meteorológicos em estações remotas.
- Dihidrogênio foi testado como combustível para a aeronáutica durante um vôo em 15 de abril de 1988 com o Tupolev Tu-155.
Certos isótopos de hidrogênio também têm um uso industrial ou tecnológico particular:
- o deutério ( 2 H) é usado em aplicações nucleares como moderador ( água pesada ou D 2 O) para desacelerar os nêutrons . Os compostos de deutério também são usados em química e biologia para estudar ou usar o efeito isotópico ;
- o trítio ( 3 H), outro isótopo, é produzido em reatores nucleares e é utilizado para a construção de bombas atômicas . Também é usado como marcador isotópico em biociências e como fonte de radiação em tintas luminescentes;
- deutério e trítio também são fundidos em reatores de pesquisa e considerados para projetos de fusão nuclear controlada na Terra.
Até o momento, três formas principais de armazenar hidrogênio a bordo de um veículo estão sendo consideradas:
- armazenamento na forma de gás comprimido;
- armazenamento na forma líquida a baixa temperatura;
- armazenamento na forma sólida, sendo o hidrogênio então ligado a outros componentes (por adsorção ou na forma de um composto químico).
Gás comprimido
É a forma mais comum de armazenamento de hidrogênio.
O armazenamento do gás na forma comprimida (atualmente 350 bar) permite atingir uma densidade de massa satisfatória com tanques compostos. A densidade do volume de armazenamento permanece baixa: uma pressão de 700 bar é inevitável para tornar a tecnologia competitiva.
A tecnologia existe e é comumente usada. Sua desvantagem está na energia necessária para a compressão e na baixa eficiência em termos de tamanho em comparação com outros métodos. Esse volume é uma das dificuldades para o uso de dihidrogênio na forma de gás comprimido em aplicações automotivas.
Quando comprimido, a densidade do hidrogênio a 20 MPa ( 200 bar) é de aproximadamente 16,8 kg / m 3 , a 35 MPa ( 350 bar) de aproximadamente 23 kg / m 3 e a 70 MPa ( 700 bar) de aproximadamente 38 kg / m 3 . Isso corresponde a uma densidade de densidade de energia de 767 kWh / m 3 (27 ° C, 35 MPa) e ainda a uma densidade de densidade de energia de 33,3 kWh / kg.
O armazenamento de líquidos a 20 K ( −253 ° C ) abaixo de 10 bar permite atingir volumes e densidades de massa interessantes, mas requer tanques com alto isolamento térmico para minimizar a evaporação.
A tecnologia está aí. Possui melhor eficiência de volume do que o armazenamento de gás comprimido ( 70 kg / m 3 contra 10 kg / m 3 a 115 bar e 0 ° C ). No entanto, esta vantagem é moderada pelo volume relativamente grande dos gabinetes de isolamento necessários.
Por outro lado, uma quantidade significativa de energia é necessária para passar para a fase líquida: a liquefação consome 30 a 40% do conteúdo energético do gás e a perda no uso real é significativa (atualmente 1,25 por mil por hora), fortemente penalizando o armazenamento além de uma semana.
Esta técnica é utilizada em particular no setor espacial onde, apesar do curto tempo de implementação, o enchimento é contínuo até ao último momento.
Hidretos metálicos
O armazenamento em substratos na forma adsorvida, em particular em hidretos metálicos, tem uma densidade de volume muito interessante, mas uma densidade de peso baixa. Além disso, a cinética, a temperatura e a pressão de ciclo permanecem pontos difíceis de controlar.
Os átomos de hidrogênio são armazenados em alguns compostos metálicos. O hidrogênio é recuperado por aquecimento ou redução da pressão. Essa técnica é mal compreendida hoje. Tem a desvantagem de exigir um di-hidrogênio extremamente puro para evitar a destruição da capacidade de absorção dos hidretos. O aquecimento para recuperar o gás também é uma desvantagem. Este tipo de armazenamento, que continua a ser objecto de investigação, encontra-se em fase de desenvolvimento industrial e estão previstos alguns projectos de demonstração, por exemplo com a start-up McPhy que está a desenvolver tecnologia de hidreto de magnésio (tecnologia do CNRS, Instituto NEEL) .
Capacidade de armazenamento de certos hidretos.
| Hidreto | Porcentagem de massa de conteúdo de H 2 |
|---|---|
| LaNi 5 H 6,5 | 1,4 |
| ZnMn 2 H 3,6 | 1,8 |
| TiFeH 2 | 1,9 |
| Mg 2 NiH 4 | 3,6 |
| VH 2 | 3,8 |
| MgH 2 | 7,6 |
Um metal muito estudado é o paládio que, através de seu hidreto PdH 2, tem a capacidade de absorver uma grande quantidade de hidrogênio em sua estrutura cristalina. À temperatura ambiente e à pressão atmosférica, o paládio pode absorver até 900 vezes seu volume de gás hidrogênio, sendo o processo reversível.
A adsorção no carbono permite armazenar na superfície de certas estruturas de carbono , como o carvão ativado ou os nanotubos , as moléculas de hidrogênio. Torna possível armazenar 0,05 a 2% em massa de dihidrogênio .
Este tipo de armazenamento está em fase de pesquisa.
Produção e usos
Em um relatório publicado em junho de 2019, a Agência Internacional de Energia observa a versatilidade do hidrogênio, que pode ser produzido a partir de todos os combustíveis fósseis, renováveis e nucleares, pode ser transportado na forma gasosa ou líquida e ser transformado em eletricidade ou em metano para uma ampla gama de usos.
Podemos distinguir três categorias de hidrogênio produzido, dependendo de como ele é produzido (consulte a seção Métodos atuais ):
- o cinza do hidrogênio , produzido pela conversão de combustíveis fósseis sem captura e armazenamento de carbono ;
- o azul de hidrogênio , produzido pela conversão de combustíveis fósseis com captura e armazenamento de carbono;
- o hidrogênio verde produzido a partir da eletricidade de fontes renováveis ou nuclear ( roxo para alguns, amarelo para outros).
O hidrogênio produzido na crosta terrestre (por diagênese e radiólise ), assim como o hidrogênio primordial (presente desde a formação da Terra ) são outras fontes possíveis, mas ainda não exploradas.
Em 2020, o custo do hidrogênio cinza está entre 1 e 2 € / kg contra 4 a 7 € / kg para o hidrogênio verde produzido de forma industrial. Segundo Julien Chauvet, diretor da Hydrogen France da Engie Solutions , “o quilo permite viajar 100 km, o que se equipara à gasolina e é semelhante ao diesel para veículos leves” .
Produção industrial
O hidrogênio é atualmente produzido quase inteiramente a partir do gás natural , petróleo e carvão .
Para suas próprias necessidades, a indústria produz hidrogênio ( por exemplo: na França, mais de 900.000 t / ano de hidrogênio, em particular para a dessulfurização de combustíveis de petróleo e para a fabricação de amônia em fertilizantes de nitrato ; o hidrogênio é então um insumo químico e não uma energia operadora ). O processo industrial mais barato para produzir esse hidrogênio, em 2018, é a reforma de hidrocarbonetos , na maioria das vezes por reforma a vapor do gás natural (que é composto principalmente de metano ). A uma temperatura entre 700 e 1.100 ° C , o vapor de água reage com o metano para dar monóxido de carbono e hidrogênio. Sendo a purificação do hidrogênio mais fácil sob alta pressão, a reforma é realizada sob uma pressão de vinte bar . A mistura de hidrogênio / monóxido de carbono é comumente referida como " gás de síntese ". Se a reação for feita na presença de excesso de vapor d'água, o monóxido de carbono é oxidado ao nível de oxidação mais alto, levando a dióxido de carbono , que aumenta a produção de hidrogênio .
A empresa Air Liquide tem um domínio particular deste processo. Em 2015, comissionou na Arábia Saudita , no site de Yanbu , uma unidade com capacidade total de produção de hidrogênio de 340.000 m 3 / h nos CNTPs .
Em 2019, a Australian Renewable Energy Agency (ARENA) disponibilizará 9,41 milhões de dólares australianos (8,5 milhões de euros ) para um projeto do grupo Hazer (empresa australiana de energia renovável) que visa converter o biogás da metanização de lodo de esgoto em hidrogênio e grafite . A Hazer quer construir uma planta de demonstração de US $ 15,8 milhões em Munster (Austrália Ocidental).
Setor de hidrogênio e desafios para o desenvolvimento sustentável
A produção industrial “tradicional” de hidrogênio a partir de hidrocarbonetos fósseis tem uma pegada de carbono pobre e emite muitos gases de efeito estufa , chegando a 830 milhões de toneladas de CO 2.por ano em 2020, ou seja, cerca de 2% das emissões globais e quase tanto quanto o setor de aviação ou transporte marítimo. Na França, essas emissões chegam a quase dez milhões de toneladas de CO 2 equivalente.por ano entre 2015-2017, ou seja, 7,5% das emissões de gases de efeito estufa da indústria francesa, de acordo com a ADEME . A produção de hidrogênio a partir de eletricidade renovável, que é mais virtuosa, pode ver seu custo cair 30% até 2030, graças ao boom das energias renováveis e às economias de escala relacionadas.
O setor de hidrogênio produz, armazena, promove e aprimora a pesquisa sobre hidrogênio e hidrogênio. Em 2015, experimentos com hidrogênio verde (livre de carbono) estão em andamento, mas esse gás ainda é "produzido principalmente a partir do gás natural ( fóssil ) e utilizado como componente químico em processos industriais" , com baixo balanço de carbono e contribuição significativa para o efeito estufa . O setor, entretanto, é apresentado como interessante para o desenvolvimento sustentável , Porque:
- se for produzido por eletrólise de água e de forma livre de carbono pela recuperação de excedentes de eletricidade renováveis intermitentes (principalmente eólica e fotovoltaica), este vetor de energia pode ser armazenado, em particular em ciclos inter-sazonais, então usado em metanação e / ou injectado na rede de gás (6 a 20% do volume consoante as condições), facilitando o equilíbrio e flexibilidade da rede eléctrica ;
- eletricidade que pode ser armazenada graças à sua conversão em gás (hidrogênio ou metano) permitiria armazenar “da ordem de um terawatt-hora por ano” e até várias dezenas de terawatt-hora por ano de eletricidade de acordo com a ADEME , quando a taxa de penetração das energias renováveis no mix elétrico chegar a 80%, e como tal poderá “dar um importante contributo para a transição para um modelo energético de baixo carbono, nomeadamente no sector do armazenamento de energia” ;
- o hidrogênio pode ser usado para produzir eletricidade localmente, mas com perda de eficiência; o da eletrólise da água está se aproximando de 70%, mas a eficiência geral da produção de eletricidade a partir de H 2 seria em torno de 25% de acordo com a Ademe em 2020;
- O hidrogênio é compatível com o autoconsumo de uma casa, ilha ou bairro, permitindo o armazenamento por vários dias, semanas ou meses, além de baterias mais úteis para armazenamento de curto prazo. Já seria economicamente justificado Em áreas não interligadas à rede elétrica continental ( por exemplo: ilhas isoladas, comunidades francesas ultramarinas onde a produção de eletricidade ainda depende de combustível a alto custo, a 225 € / MWh em média em 2013 de acordo para ADEME);
- o hidrogênio pode abastecer certas frotas de veículos profissionais, sem exigir uma rede cara de várias centenas de postos de serviço em todo o país. Segundo a Ademe, “o modelo económico de estação para frota é acessível para um consumo diário superior a 80 kg H 2 / dia, para a comercialização de hidrogénio inferior a 10 € / kg ” . Neste caso, tem as vantagens de um tempo de recarga rápido e uma grande autonomia;
- o hidrogênio pode ser usado na indústria do aço como substituto do carvão ou do gás natural para a redução do minério de ferro. Usar este processo na França consumiria 700.000 toneladas de hidrogênio, mas evitaria a emissão De 22 MtCO 2/ ano, ou quase 5% das emissões do país, indica a Associação Francesa de Hidrogênio e Células de Combustível (Afhypac).
a 8 de julho de 2020, a Comissão Europeia apresenta um programa para o desenvolvimento do hidrogênio verde, estabelecendo o objetivo de que o hidrogênio cubra de 12 a 14% das necessidades energéticas até 2050, a fim de descarbonizar determinados setores da indústria e dos transportes. Depende do hidrogênio para contribuir para a transição energética e para a redução das emissões de gases de efeito estufa. Ao mesmo tempo, o Comissário Europeu para o Comércio Interno, Thierry Breton, anuncia a criação da aliança do hidrogênio.
Na FrançaA ADEME está considerando um mix de eletricidade para 40% composto por "renováveis" em 2035, depois para 60% e 70% em 2050 (contra quase 18% em 2017, enquanto a maioria de fonte hidrelétrica).
O setor busca industrializar seus processos para reduzir seus custos (em particular o da célula a combustível ). O desenvolvimento da “mobilidade do hidrogênio” também é dificultado por um número ainda muito baixo de estações de carregamento (e sua capacidade ainda baixa: 10 a 80 kg H 2 / d a 350 bar). O hidrogênio pode melhorar a potência do veículo, estender seu alcance e melhorar a velocidade de recarga, em comparação com as baterias.
A Ademe considera que o hidrogénio terá um papel importante na transição energética, como vector de optimização de redes energéticas, de armazenamento de energia no autoconsumo solar ou fotovoltaico, e de determinados veículos profissionais, desde que descarbonize a sua produção de energia por electrólise usando eletricidade verde e a transformação da biomassa ( reforma a vapor do biogás , pirogasificação da biomassa sólida). O desempenho ambiental do setor dependerá sobretudo “da fonte primária de produção do hidrogênio”. A agência pede que a distância de transporte de hidrogênio entre o ponto de fabricação e a estação de distribuição seja limitada a menos de cem quilômetros. Os veículos movidos a bateria devem ser preferidos, quando possível (alcance, disponibilidade, etc.), dado o melhor desempenho deste tipo de armazenamento, e a economia de energia continua sendo uma prioridade. Uma das vias de desenvolvimento (atualmente em teste em 2018/2019) é a injeção na rede de gás na França por meio de dois demonstradores: GRHYD e Jupiter 1000 , para remover as barreiras técnicas que ainda existem.
Em junho de 2018, o governo francês encarrega a Ademe de lançar o "plano nacional de implantação de hidrogênio" (ou "plano de hidrogênio"), a fim de impulsionar este setor cujo "alto potencial" é percebido pelos atores públicos. O objetivo do governo é "criar um setor industrial francês livre de carbono, abrir novas perspectivas para o armazenamento de energias renováveis e desenvolver soluções de emissão zero para o transporte" . Um ano depois, o órgão público fez várias convocatórias de projetos , entre elas “Ecossistemas de mobilidade de hidrogênio”, o que possibilitou selecionar projetos “em todos os territórios” e diversificados, como “entrega de última milha em áreas urbanas., Transporte coletivo de passageiros por ônibus ou transporte marítimo, aluguel de automóveis, coleta de lixo, frotas empresariais e comunitárias, ou ainda a utilização de veículos pesados de mercadorias como veículos de construção ” .
O CEA promete uma nova tecnologia de eletrólise industrial, chamada rSOC com um único metal precioso: o índio (metal usado em telas de LCD ), com temperaturas mais baixas (de 700 ° C a 800 ° C ) e menor consumo de energia. Também é reversível, possibilitando a produção de hidrogênio ou a restauração de energia elétrica, como uma célula a combustível.
No final de 2019, a Air Liquide e a Engie uniram forças com a Durance-Luberon-Verdon Agglomeration (DLVA) para produzir, armazenar e distribuir "hidrogênio verde" (como parte do projeto "HyGreen Provence" lançado em 2017, visando 1.300 GWh de eletricidade solar e vários milhares de toneladas: ano de hidrogênio produzido por eletrólise Várias dezenas de milhares de toneladas de hidrogênio renovável por ano poderiam ser produzidas a longo prazo, que podem ser armazenados em uma cavidade salina local.
A francesa McPhy , que já instalou 17 MW de capacidade de produção de hidrogênio por eletrólise pressurizada, incluindo 6 MW na Audi na Alemanha, anuncia em janeiro de 2020 a assinatura do contrato de engenharia para um projeto de produção de hidrogênio verde industrial de 20 MW , o maior projeto até o momento na Europa, localizado em Delfzijl na Holanda até 2022. A planta irá produzir 3.000 toneladas de hidrogênio por ano por eletrólise de água usando energia eólica e será usada para fabricar bioetanol. O projeto beneficia de 15 milhões de euros em bolsas da União Europeia e de um fundo holandês. Segundo McPhy, a escala certa será de 100 ou 200 MW para atingir um preço competitivo no setor.
A Lei do Clima de Energia de novembro de 2019 dá ao governo um ano para criar um mecanismo de apoio para "hidrogênio produzido a partir de energia renovável ou por eletrólise da água usando eletricidade de baixo carbono" . Antes de 2023, o programa plurianual de energia visa descarbonizar 10% do hidrogênio consumido na indústria, o que requer a produção de 90.000 toneladas de hidrogênio verde. Em janeiro de 2020, o governo lança um convite à manifestação de interesse , com o objetivo de testar o apetite dos industriais pelo assunto, que recebe mais de 160 projetos. Por exemplo, em janeiro, a H2V Industry registra pedidos de licença de construção para duas fábricas de produção de hidrogênio na área industrial de Port-Jérôme, na Normandia, e no grande porto marítimo de Dunquerque a partir de eletricidade renovável; se conseguirem se beneficiar de um mecanismo de apoio, seu comissionamento poderá ocorrer em 2023-2024 e produzirão 56.000 toneladas de hidrogênio. Os principais players industriais franceses (Engie, EDF, Air Liquide, Vinci, etc. ) também se posicionaram.
O governo Castex anunciou em setembro de 2020 um plano muito mais ambicioso do que o apresentado por Nicolas Hulot em 2018, dotado de € 100 milhões: o plano de 2020 prevê a destinação de € 7,2 bilhões até 2030 para o hidrogênio verde ou de baixo carbono, incluindo € 2 bilhões em 2021 e 2022 como parte do plano de recuperação. O governo planeja subsidiar a produção de hidrogênio verde por meio de licitações, baseadas em energias renováveis, e a construção de usinas de células a combustível para veículos movidos a hidrogênio. Parcerias com a Alemanha, que revelou um plano de hidrogênio de € 9 bilhões em junho, estão sendo consideradas para evitar a duplicação.
Este plano de hidrogénio inclui uma primeira componente de € 1,5 mil milhões destinada ao fabrico de electrolisadores, de forma a reduzir o custo, melhorando-o e aumentando os volumes, para uma capacidade de 6,5 GW . A segunda componente de quase mil milhões de euros será utilizada até 2023 para desenvolver uma oferta de mobilidade pesada de hidrogénio, reduzindo o custo e melhorando a eficiência das células de combustível para comboios, camiões, autocarros e aeronaves, através de vários convites à apresentação de projectos (350 milhões de euros para demonstradores, 275 milhões para experiências regionais, etc.). Por fim, serão estimulados os auxílios à investigação e inovação, com um envelope elevado para 650 milhões até 2023. Bruno Le Maire espera que este plano gere entre 50.000 e 150.000 empregos diretos e indiretos. O governo está considerando uma cooperação com a Alemanha descrita como "Airbus para eletrólise", como o "Airbus para baterias". A França estabeleceu como objetivo produzir 600.000 toneladas por ano de hidrogênio verde, a partir de eletricidade sem carbono, de origem renovável ou nuclear. Ao contrário da Alemanha, Paris não vai, no entanto, subsidiar a captura de carbono do hidrogênio “cinza”. Bruno Le Maire espera ver "o surgimento de um setor de eletrólise francês": ao lado de gigantes como a Air Liquide, as start-ups também são numerosas, como a Lhyfe , com sede em Nantes, que está desenvolvendo unidades de produção de hidrogênio verde para fabricantes e autoridades locais, ou ainda a McPhy , produtora Drôme de eletrolisadores da qual a EDF é acionista.
Na BélgicaUma equipe da KUL está projetando um protótipo de célula fotoeletroquímica de 1,6 m 2 , produzindo em média 250 litros de hidrogênio por dia a partir do vapor de água atmosférico. O aparelho converte 15% da energia solar em hidrogênio e oxigênio. E essa tecnologia não usa metais preciosos ou outros materiais caros. Com vinte painéis, uma casa bem isolada seria autossuficiente em eletricidade e aquecimento por um ano.
O Grupo Colruyt (um grande varejista belga) quer descarbonizar suas atividades o máximo possível. Em 2018, um de seus centros logísticos foi equipado com 75 elevadores movidos a hidrogênio “livre de carbono” e sua frota de caminhões deve ser convertida até 2030. Com um player de gás, está sendo elaborado um projeto de instalação de 12 a 25 MW . (Expansível) para converter eletricidade de turbinas eólicas offshore em hidrogênio , em escala industrial.
No JapãoNo final de 2017, o Japão, um grande importador de energia, confirmou que queria se tornar líder como uma “ empresa de hidrogênio ” com o objetivo de “paridade de custos” com a gasolina e o GNL para a produção de eletricidade. Assim como o nuclear no passado, o hidrogênio é apresentado como o principal meio de descarbonização da energia, mas os projetos-piloto darão suas conclusões por volta de 2020. Em 2018, o Japão está na liderança da mobilidade do hidrogênio, com cerca de 2.500 carros com células a combustível de hidrogênio em circulação e mais de cem estações de hidrogênio (em comparação com 45 na Alemanha, 42 nos Estados Unidos e cerca de 20 na França ao mesmo tempo). O país pretende dividir o custo de produção por mais de três antes de 2030, depois em 80% antes de 2050. Entre 2013 e 2017, o estado japonês já investiu US $ 1,5 bilhão em P&D e no desenvolvimento do hidrogênio.
Em califórniaEm outubro de 2019, Califórnia tem 7.570 carros a hidrogênio registrados e 42 estações públicas dos EUA.
Na AlemanhaO governo alemão adota um ambicioso plano de desenvolvimento do hidrogênio “verde”, dotado de 9 bilhões de euros.
Motor a hidrogênio
Fusão nuclear: bomba H e reatores de fusão
Perigos, riscos e precauções
Dihidrogênio é um gás classificado como "extremamente inflamável ". É caracterizado por uma faixa de inflamabilidade muito ampla (de 4 a 75% do volume no ar), causando uma deflagração de uma entrada de energia de ativação muito baixa (uma faísca é suficiente se fornecer uma energia de 0,02 milijoules (mJ) enquanto leva 0,29 mJ para desencadear uma explosão de metano ). Dihidrogênio misturado com oxigênio em proporções estequiométricas é um poderoso explosivo . Dihidrogênio no ar é uma mistura explosiva quando a razão H 2 / volume de ar está entre 13 e 65%
A história de seu uso em aeronaves está repleta de acidentes graves, o mais famoso dos quais é o desastre de Hindenburg . O zepelim LS 129 , inflado com 200.000 metros cúbicos de hidrogênio (porque os Estados Unidos haviam declarado um embargo ao hélio contra a Alemanha ) queimou o6 de maio de 1937na chegada ao Lakehurst Airfield , perto de Nova York ). 36 pessoas morreram de um total de 97 embarcados. A mídia presente divulgou amplamente as imagens do desastre, o que gerou o descontentamento do público com os balões. As investigações sobre a origem do acidente, facilitadas pela abundância de documentos fotográficos, não incriminaram porém uma explosão de hidrogênio, mas uma ignição por contiguidade, de um incêndio no envelope (provavelmente causado por descarga de eletricidade estática). A composição do revestimento impermeável do envelope (butiratos e alumínio) teria favorecido uma violenta reação aluminotérmica . No entanto, o acidente teria sido muito menos violento se o balão tivesse sido inflado com hélio.
A substituição do hidrogênio por hélio (muito mais caro e mais denso) não produziu o renascimento esperado da preferência. O medo do hidrogênio permaneceu; a “síndrome de Hindenburg” provavelmente penalizou injustamente a indústria.
Dihidrogênio reage ainda mais violentamente com o cloro para formar ácido clorídrico (HCl), mesmo sem ativação, e com difluoreto para formar ácido fluorídrico (HF) perigoso, mesmo em temperaturas onde o hidrogênio é líquido e o flúor é sólido, sendo a última reação o produto químico mais exotérmico reação existe .
Os padrões de segurança são reforçados para fazer face aos riscos decorrentes da passagem em túneis e do estacionamento em garagens ou parques subterrâneos.
Regulamentações globais de veículos estão sendo desenvolvidas sob os auspícios da ONU com base em propostas dos fabricantes, mas com relação ao dihidrogênio, os fabricantes japoneses, americanos e europeus não concordam. A Comissão Europeia pode decidir sobre regulamentos comunitários provisórios.
Na França, o INERIS e o CEA trabalham com a International Organization for Standardization ( ISO ) em um comitê técnico denominado TC 197 sobre o risco do hidrogênio. Um projecto europeu Hysafe também trata do assunto, onde o INERIS criticou o projecto de regulamento ao sugerir uma abordagem mais global e sistémica e não por componente para a homologação de veículos híbridos . Em 2015, o MEDDE preparou uma atualização do regulamento dos postos de gasolina e frotas de veículos movidos a hidrogênio.
Risco de camada de ozônio
Uma liberação maciça de gás hidrogênio levantou a hipótese de um risco para a camada de ozônio .
Medidas de segurança
Os seguintes pontos são notáveis:
- o hidrogênio não é inerentemente tóxico;
- é oito vezes mais leve que o metano. Sua molécula muito pequena lhe dá um coeficiente de difusão muito bom no ar (quatro vezes o do metano); em um ambiente não confinado, o hidrogênio, portanto, tende a subir e se diluir rapidamente no ar (é um fator de segurança ao ar livre e um fator de perigo em locais confinados);
- é a espécie química mais energética por unidade de massa (120 kJ / g ); mas por unidade de volume de gás, a energia explosiva teórica é 3,5 vezes menor para o hidrogênio do que para o gás natural;
- seu limite inferior de ignição é de 4% em volume, comparável ao do gás natural (5% em volume); mas seu limite superior de inflamação é significativamente maior (75% contra 15%); isso significa que, em caso de vazamento, o hidrogênio se inflama muito mais facilmente do que o gás natural ou os combustíveis líquidos;
- a energia necessária para acendê-lo na estequiometria também é significativamente menor (cerca de 10 vezes) do que o gás natural ou propano;
- a chama de hidrogênio, azul claro, é quase invisível durante o dia (risco para serviços de emergência);
- a chama do hidrogênio se propaga cerca de sete vezes mais rápido que a do gás natural e o risco de detonação (explosão com efeito de explosão muito forte) é agravado por seu alto coeficiente de difusividade.
A inflamabilidade pode ser ainda mais reduzida diluindo o hidrogênio em hélio, mesmo em temperaturas muito altas.
Referência da ONU para o transporte de mercadorias perigosas
- Nome (francês): Hidrogênio comprimido
- Classe: 2
- número: 1049
- Nome (francês): Hidrogênio líquido refrigerado
- Classe: 2
- número: 1966
- Nome (inglês): Hidrogênio em um dispositivo de armazenamento de hidreto de metal
- Classe: 2
- número: 3468
Notas e referências
- HIDROGENE , ficha (s) de segurança do Programa Internacional de Segurança de Substâncias Químicas , consultado em 9 de maio de 2009
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (en) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press Inc,2009, 90 th ed. , 2804 p. , Capa dura ( ISBN 978-1-4200-9084-0 ).
- Jean-Louis Vignes ( dir. E membro da Sociedade de Química de França) et al. , " Dihydrogen: Physico-Chemical Data " , site de promoção e educacional relacionado a elementos químicos (da tabela periódica de Dmitri Mendeleïev ), em lelementarium.fr , Paris & Puteaux , Société Chimique de France & France Chimie (acessado em 3 de novembro de 2019 ) .
- Pierre Ravarini (engenheiro químico e hidrólogo), " Gaz-Hydrogen " , site de informações científicas, técnicas e ecológicas sobre a água, Côte de Nacre ( Calvados ), 2019(acessado em 3 de novembro de 2019 ) .
- (em) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 p. ( ISBN 978-0-387-69002-5 e 0-387-69002-6 , ler online ) , p. 294
- (en) Robert H. Perry e Donald W. Green , Perry's Chemical Engineers 'Handbook , EUA, McGraw-Hill,1997, 7 th ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- " Propriedades de vários gases, " em flexwareinc.com (acessado em 12 de abril de 2010 )
- Atas do Comitê Internacional de Pesos e Medidas , 78 a Sessão, 1989, pp. T1-T21 (e p. T23-T42, versão em inglês).
- (em) W. M Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 p. ( ISBN 978-1-4398-2077-3 ) , p. 14-40.
- (em) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 de junho de 2002, 83 th ed. , 2664 p. ( ISBN 0849304830 , apresentação online ) , p. 5-89
- Magalie Roy-Auberger, Pierre Marion, Nicolas Boudet, Gasification of coal , ed. Técnicas do Engenheiro, referência J5200 , 10 de dezembro de 2009, p. 4
- " Office of Radiation, Chemical & Biological Safety (ORCBS) " (acessado em 16 de abril de 2009 )
- Regulamento CE n o 1272/2008 , 16 de dezembro de 2008 [PDF] em EUR-Lex , p. 923 : Anexo VI, quadro 3.1, número de índice .
- " Hidrogênio " no banco de dados de produtos químicos Reptox da CSST (Organização de Quebec responsável pela segurança e saúde ocupacional), acessado em 23 de abril de 2009
- "hidrogênio" , em ESIS , acessado em 15 de fevereiro de 2009
- " A descoberta de fontes de hidrogênio abre caminho para uma nova energia " , Le Monde .
- “ Hidrogênio natural, um El Dorado energético? » , Sciences et Avenir .
- Experimentos de Lavoisier , em lavoisier.cnrs.fr
- " Energia de hidrogênio " , sobre Conhecimento de Energias ,30 de agosto de 2011(acessado em 10 de dezembro de 2019 ) (atualizado9 de abril de 2015)
- Rendimento da cadeia de hidrogênio (ficha técnica), Ademe ,janeiro de 2020( leia online [PDF] ).
- " Detecção de emanações naturais de hidrogênio por meio de imagens de satélite - Lançamento do projeto sen4H2 " , no IFP Énergies nouvelles (acesso em 6 de abril de 2019 ) .
- “ Deep-sea mineral resources ” , no Ifremer (acesso em 28 de outubro de 2019 ) .O artigo apresenta um mapa do fundo do mar dando a distribuição serpentina conhecida ao longo das cristas.
- Sylvestre Huet , “ hidrogênio Native, uma nova fonte de energia? » , Em sciences.blogs.liberation.fr , Liberation ,23 de abril de 2013(acessado em 28 de outubro de 2019 ) .
- " Reação da água do mar-manto: formação de serpentina " , no Ifremer (acessado em 28 de outubro de 2019 ) .
- " Síntese de hidrogênio, metano e hidrocarbonetos no fundo do mar, rumo a novos recursos energéticos ... " , no Ifremer (acesso em 28 de outubro de 2019 ) .
- " Hidrogênio, sim, mas hidrogênio natural " , no La Tribune ,28 de junho de 2018(acessado em 3 de outubro de 2020 ) .
- Hidrogênio natural: uma contribuição para a matriz energética? , IFP Novas energias ,11 de abril de 2013.
- Julia Guélard , Caracterização das emanações de hidrogênio natural em um contexto intracratônico: exemplo de uma interação gás / água / rocha no Kansas (tese de doutorado em geoquímica), Universidade Pierre-et-Marie-Curie e IFP Énergies nouvelles ,2016( apresentação online , leia online ).
- (em) J. Guélard , V. Beaumont , V. Rouchon e F. Guyot , " Natural H2 in Kansas: Deep gold shallow origin? » , Geochemistry, Geophysics, Geosystems , vol. 18, n o 5,3 de abril de 2017, p. 1841–1865 ( ISSN 1525-2027 , DOI 10.1002 / 2016GC006544 , resumo , ler online , acessado em 28 de outubro de 2019 ).
- Alain Prinzhofer, Eric Deville, hidrogênio Natural - A próxima revolução energética? , Ed. Belin, 2015 ( ISBN 978-27011-83848 ) .
- J. Guélard et al. , “ H 2 natural em Kansas: origem profunda ou rasa? ", Geochemistry Geophysics Geosystems ,abril de 2017( DOI 10.1002 / 2016GC006544 , apresentação online , ler online [PDF] , acessado em 25 de outubro de 2109 ).
- (in) Isabelle Moretti, Emyrose Brouilly, Keanu Loiseau, Alain Prinzhofer Eric Deville, " Hydrogen Fumes in Intracratonic Areas: New Guide Lines for Early Screening Basin Exploration " em hmdpi.com ,22 de março de 2021(acessado em 16 de junho de 2021 )
- (em) Maria Rosanne Fabian Rupin Louis Gorintin Julio Aguilar, Helena-Fog, Werly Julien Olivier Lhote, Xi Yao, " PARHYS SYSTEM: A NEW ABORDAGE TO H2 CONCENTRATION MEASUREMENTS IN THE SUBSURFACE " em hnatsummit.com ,26 de abril de 2021(acessado em 16 de junho de 2021 )
- (em) H. Hosgormez G. Etiope e MN Yalçin , " Nova evidência para uma origem inorgânica e orgânica mista do fogo olímpico Chimaera (Turquia): uma infiltração de gás abiogênico em costa larga " , Geofluids , vol. 8, n o 4,25 de novembro de 2008, p. 263-273 ( DOI 10.1111 / j.1468-8123.2008.00226.x ).
- " Bourakébougou: a promessa de uma usina de hidrogênio " ,18 de fevereiro de 2013(acessado em 28 de outubro de 2019 ) .
- " Hidrogênio de acordo com Isabelle Moretti - Sciences et Avenir " , Sciences et Avenir (acessado em 2 de junho de 2021 ) .
- (in) "Gases vulcânicos: queima de hidrogênio no vulcão Kilauea, Havaí" em mendeley.com.
- (en) Deep Hydrogen em astrobio.net.
- (en) GJ MacDonald (1988). “Principais questões sobre estruturas continentais profundas” Perfuração profunda em rocha cristalina, v. 1 : 28-48 p., Berlin: Springer-Verlag. .
- " Hidrogênio natural uma fonte muito mais importante do que se pensava de acordo com o CNRS " , em http://erh2-bretagne.mystrikingly.com ,Maio 112019(acessado em 12 de novembro de 2019 ) .
- Isabelle Moretti, " hidrogênio Natural:? Curiosidade geológica ou principal fonte de energia no futuro" » , Sobre o conhecimento das energias .
- " Em 15 de abril de 1988, o Tu-155 voa com hidrogênio " , no Aerobuzz ,2 de outubro de 2020(acessado em 12 de novembro de 2020 )
- Hidrogênio, novas tecnologias de energia. As chaves CEA, n o 50/51, inverno 2004-2005, ( ISSN 0298-6248 )
- Relatório StorHy do projeto europeu, p. 8, taxa de perda de hidrogênio
- Artigo do Tribune Europa financia bateria gigante para armazenar energia renovável
- (em) T. Mitsui, MK Rose E. Fomin, DF Ogletree e M. Salmeron, " Dissociative hidrogênio adsorção é paládio requer agregados de três ou mais vagas " , Nature , vol. 422,17 de abril de 2003, p. 705-707 ( DOI 10.1038 / nature01557 , leia online [PDF] ).
- (en) O Futuro do Hidrogênio - Aproveitando as oportunidades de hoje [PDF] , Agência Internacional de Energia , junho de 2019.
- Caminhos de descarbonização de gás (in) 2020-2050 , Gás para o clima,abril de 2020, 226 p. ( leia online [PDF] ) , p. 17.
- " Plano de recuperação: que lugar para a energia? » , Em connancedesenergies.org ,4 de setembro de 2020.
- (em) "O hidrogênio produzido a partir da energia nuclear será considerado 'de baixo carbono', disse um funcionário da UE " ["O hidrogênio produzido a partir da energia nuclear será considerado" de baixa pegada de carbono ", de acordo com um funcionário da UE»], Em EURACTIV ,19 de novembro de 2020.
- " O plano francês para o hidrogênio confirma discretamente o relançamento da energia nuclear " , no Reporterre ,2 de fevereiro de 2021.
- " Hidrogênio natural: uma curiosidade geológica ou uma importante fonte de energia no futuro?" » , Em connancedesenergies.org ,22 de maio de 2020.
- “ Hidrogênio verde, o elo que faltava na transição ” , Alternatives économique (acessado em 8 de agosto de 2020 ) .
- Interactions (carta aos acionistas da Air Liquide), Air Liquide , setembro de 2015 [PDF] , p. 5 .
- (in) Liz Gyekye [ https://biomarketinsights.com/australia-backs-tech-that-converts-biogas-into-hydrogen-and-graphite/ "Australia apóia tecnologia que converte biogás em hidrogênio e grafite"] Biomarketing , 4 de setembro de 2019.
- Jérôme Marin, " Lhyfe produzirá hidrogênio verde com turbinas eólicas " , La Tribune ,17 de janeiro de 2020.
- "The Ademe lista as" principais contribuições "do hidrogênio para a transição de energia" , Connaissance des energies , 4 de abril de 2018.
- O vetor hidrogênio na transição energética , Parecer da ADEME, abril de 2018 [PDF] .
- Séverine Fontaine, " O Ademe quer hidrogênio a partir de energias renováveis ", L'Automobile & L'Entreprise , n o 5,fevereiro de 2016( leia online ).
- " A Comissão Europeia revela seu plano de desenvolvimento de hidrogênio verde " , no EnerGeek ,10 de julho de 2020(acessado em 11 de julho de 2020 ) .
- Hidrogênio na transição energética , Ademe , fevereiro de 2016, 7 páginas [PDF] .
- Joseph Martin , “ Desenvolvimento do hidrogênio, ADEME faz um balanço ” , na RSE Magazine (acessado em 17 de maio de 2019 ) .
- " Pesquisadores de Grenoble otimizam a fotossíntese artificial para produzir hidrogênio " , em placegrenet.fr ,21 de abril de 2018(acessado em 30 de março de 2019 ) .
- Véronique Pouzard, " A eletrólise de alta temperatura do CEA transportada pela start-up Sylfen " , Les Échos ,26 de fevereiro de 2019(acessado em 30 de março de 2019 ) .
- AFP (2019) Hidrogênio “verde”: cooperação entre a Air Liquide, Engie e a aglomeração Durance, Lubéron, Verdon ; 13 de novembro de 2019
- McPhy no centro da maior unidade de produção de hidrogênio com carbono zero da Europa , Les Échos , 22 de janeiro de 2020.
- Plano de recuperação: França muda escala em hidrogênio , Les Échos , 3 de setembro de 2020.
- Hidrogênio: França detalha seu plano de 7 bilhões de euros , Les Échos , 8 de setembro de 2020.
- Hidrogênio: o governo quer criar um "Airbus para eletrólise" , Les Échos , 8 de setembro de 2020.
- (em) " Cientistas da KU Leuven decifram o código do gás hidrogênio acessível e ecologicamente correto " , na KU Leuven (acessado em 31 de outubro de 2019 ) .
- " Pesquisadores belgas estão desenvolvendo um painel solar que produz hidrogênio " , em RTBF Info ,1 ° de março de 2019(acessado em 31 de outubro de 2019 ) .
- " Grupo Colruyt: a aposta na mobilidade do hidrogênio " , no RTBF Info ,8 de outubro de 2018(acessado em 31 de outubro de 2019 ) .
- " Colruyt e Fluxys querem construir uma usina de hidrogênio, a primeira na Bélgica " , Le Soir ,8 de outubro de 2019(acessado em 31 de outubro de 2019 ) .
- " Driving on hidrogênio: nossa experiência " , automóvel Le Moniteur (acesso em 31 de outubro de 2019 ) .
- (en) Monica Nagashima (Instituto de Economia da Energia, Japão), a estratégia de hidrogênio do Japão e suas implicações econômicas e geopolíticas , Institut Français des internationales relações , outubro 2018 [PDF] .
- "A" estratégia do hidrogênio "do Japão" , Conhecimento das energias, 9 de outubro de 2018.
- (em) " Centro de dados de combustíveis alternativos: Férias na estação de abastecimento de hidrogênio " , no centro de dados de combustíveis alternativos , Departamento de Energia dos Estados Unidos (acessado em 31 de outubro de 2019 ) .
- Benoît Le Floc'h, “ E o hidrogênio para veículos comerciais leves? » , No Caradisiac ,29 de novembro de 2018(acessado em 30 de março de 2019 ) .
- " Califórnia supera a marca de 7.500 carros a hidrogênio em circulação " , em www.h2-mobile.fr (acessado em 31 de outubro de 2019 ) .
- (em) " Governo alemão adota estratégia de hidrogênio " ["O governo alemão adota estratégia de hidrogênio"], no Governo Federal (Alemanha) ,10 de junho de 2020.
- Acidentes de hidrogênio , Ministério da ecologia, energia, desenvolvimento sustentável e planejamento regional , 18 p. ( leia online [PDF] ) , p. 4.
- Radisson, Laurent (2015) Riscos do hidrogênio: o Ministério da Ecologia está trabalhando em novos textos; ; Env de notícias, publicado em 21 de outubro de 2015
- T. Rahn, JM Eiler, KA Boering, PO Wennberg, MC McCarthy, S. Tyler, S. Sc Chauffage, S. Donelly, E. Atlas, Extremo enriquecimento de deutério em hidrogênio estratosférico e o orçamento atmosférico global de H2 , Nature 424 , 918-921, 2003.
- TK Tromp , RL Shia , Sr. Allen , JM Eiler e YL Yung , " Potential Environmental impact of a hidrogênio Economy on the stratosphere ," Science , n o 300,2003, p. 1740-1742 ( DOI 10.1126 / science.1085169 ).
- Céline Duguey, " An explosive experience " , no Espace des sciences ,setembro de 2009(acessado em 16 de abril de 2020 ) .
- (in) Florent Tonus Mona Bahout , Paul F. Henry e Siân E. Dutton , " Uso de difração in situneutron para monitorar reações sólidas / gás H2 em alta temperatura " , Chemical Communications , n o 18,21 de abril de 2009, p. 2556–2558 ( ISSN 1364-548X , PMID 19532888 , DOI 10.1039 / B822419F , ler online , acessado em 16 de abril de 2020 ).
Veja também
Bibliografia
- Yver, Camille, Quantificando o uso de hidrogênio pelos solos: da escala local à global , 2011 DOI: 10.4267 / 2042/47372 ( resumo - Prix Prud'homme 2011.
- Stephen Boucher, The Hydrogen Revolution. Rumo a energia limpa e eficiente? , prefácio de Thierry Alleau, Paris, Éd. du Felin, 2006, 160 p. , ( ISBN 2-86645-616-5 ) .
- Alain Prinzhofer, Eric Deville, Hidrogênio natural - A próxima revolução energética? , Belin, 2015 ( ISBN 978-27011-83848 )
Artigos relacionados
links externos
- Associação Francesa de Hidrogênio
- Rede europeia / pólo de competência
- Desenvolvimento H2
- CEA Technologies, Hydrogen, new energy technologies , Clefs CEA n o 50-51), 23 de março de 2005
- Hidrogênio visto pelo CEA
- INERIS: feedback da experiência ligada a dificuldades de armazenamento
- Hidrogênio visto pela Sociedade Francesa de Química
- A polêmica sobre o uso do hidrogênio como combustível
- Tudo sobre a Alternativa do Hidrogênio, com resenha na imprensa, links para internet e vídeos








