Ácido fosfórico
| Ácido fosfórico | |
|
|
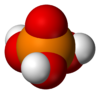
| Estrutura do ácido fosfórico. | |
| Identificação | |
|---|---|
| Nome IUPAC | ácido ortofosfórico |
| Sinônimos |
|
| N o CAS | |
| N o ECHA | 100.028.758 |
| N o EC | 231-633-2 |
| PubChem | 1004 |
| N o E | E338 |
| FEMA | 2900 |
| SORRISOS |
OP (= O) (O) O , |
| InChI |
InChI: InChI = 1S / H3O4P / c1-5 (2,3) 4 / h (H3,1,2,3,4) InChIKey: NBIIXXVUZAFLBC-UHFFFAOYSA-N |
| Aparência | Sólido branco ou líquido viscoso incolor ( T > 42 ° C ) |
| Propriedades quimicas | |
| Fórmula bruta | H 3 PO 4 |
| Massa molar | 97,9952 ± 0,0014 g / mol H 3,09%, O 65,31%, P 31,61%, |
| pKa | ( 25 ° C ) p K a1 = 2,148; 7.198; 12,319 |
| Propriedades físicas | |
| Fusão T ° | 42,35 ° C |
| T ° fervendo | Decompõe-se abaixo do ponto de ebulição a 213 ° C |
| Solubilidade | Chão. no álcool, chão. em 8 vol. de uma mistura de éter: álcool 3: 1, |
| Massa volumica | 1,834 g cm −3 a 18 ° C |
| Pressão de vapor de saturação | a 20 ° C : 4 Pa |
| Viscosidade dinamica | 3,86 mPa s (solução a 40%, 20 ° C ) |
| Precauções | |
| SGH | |
 Perigo H314, H314 : Provoca queimaduras na pele e lesões oculares graves |
|
| WHMIS | |
 E, E : Transporte de material corrosivo de mercadorias perigosas: classe 8 Divulgação a 1,0% de acordo com a lista de divulgação de ingredientes |
|
| NFPA 704 | |
| 0 3 0 | |
| Inalação | Sensação de queimadura. Tosse. Falta de ar. Dor de garganta. |
| Pele | Vermelhidão. Dor. Queimaduras na pele. Lâmpadas |
| Olhos | Dor. Vermelhidão. Graves queimaduras profundas. |
| Ingestão | Dor abdominal. Sensação de queimadura. Choque ou colapso. |
| Compostos relacionados | |
| Outros compostos | |
| Unidades de SI e STP, salvo indicação em contrário. | |
O ácido fosfórico é um composto químico de fórmula H 3 PO 4. É um oxoácido trifuncional ( triácido ) importante na química inorgânica e fundamental na bioquímica . É um ácido mineral obtido pelo tratamento da rocha fosfática ou pela queima do fósforo .
À temperatura ambiente, o ácido fosfórico é um densidade 1,83 fusão sólido cristalino a 42,35 ° C . Constitui a matéria-prima básica para a produção de fosfatos (ou sais de fosfato).
Por meio da escória de gesso , a produção de ácido fosfórico é uma fonte de um acúmulo significativo de rejeitos de baixo nível radioativo e "tecnologicamente TENORM".
Química
É um triácido mineral capaz de abrir mão de três prótons, formando sucessivamente três bases conjugadas: o íon dihidrogenofosfato H 2 PO 4 -, o íon de fosfato de hidrogênio HPO 4 2-e o íon fosfato PO 4 3-, com as seguintes constantes de equilíbrio (a 25 ° C ):
| H 3 PO 4 (s) + H 2 O (l) H 2 PO 4 - (aq) + H 3 O + (aq), | K a1 = 7,13 × 10 −3 , | p K a1 = 2,15. |
| H 2 PO 4 - (aq) + H 2 O (l) HPO 4 2− (aq) + H 3 O + (aq), | K a2 = 6,38 × 10 −8 , | p K a2 = 7,20. |
| HPO 4 2− (aq) + H 2 O (l) PO 4 3− (aq) + H 3 O + (aq), | K a3 = 3,79 × 10 −13 , | p K a3 = 12,42. |
Biologia
Os dímeros e trímeros do ácido fosfórico estão envolvidos em muitas áreas da biologia, como transportadores de energia ADP / ATP , DNA e nos ossos .
Produção industrial
O ácido fosfórico é geralmente obtido atacando a apatita (o principal minério de fosfato) em um reator com ácido sulfúrico H 2 SO 4. A apatita costuma ser uma mistura de:
- clorapatite Ca 5 (PO 4 ) 3 Cl;
- fluorapatite Ca 5 (PO 4 ) 3 F;
- hidroxiapatita Ca 5 (PO 4 ) 3 (OH).
e também carbonato-apatitas onde um grupo CO 3 OH ou CO 3 F substitui um tetraedro PO 4 .
As reações são, portanto:
Ca 5 (PO 4 ) 3 Cl + 5 H 2 SO 4 + 10 H 2 O → 3 H 3 PO 4 + 5 (CaSO 4 , 2H 2 O) + HCl.
Ca 5 (PO 4 ) 3 F + 5 H 2 SO 4 + 10 H 2 O → 3 H 3 PO 4 + 5 (CaSO 4 , 2H 2 O) + HF.
Ca 5 (PO 4 ) 3 OH + 5 H 2 SO 4 + 9 H 2 O → 3 H 3 PO 4 + 5 (CaSO 4 , 2H 2 O).
Os carbonatos fornecem dióxido de carbono e água em vez de parte do ácido fosfórico.
Após um certo tempo de residência no reator (variável dependendo do tipo de reator usado e do minério tratado), uma operação de filtração é realizada na pasta resultante (o líquido e o sólido) a fim de separar também o ácido fosfórico. feito de cristais de sulfato de cálcio di-hidratado (CaSO 4 , 2H 2 O) ou semi-hidratado (CaSO 4 , 1 / 2H 2 O) denominado fosfogesso .
Também pode ser preparado por calcinação em alta temperatura da apatita com sílica e carbono (areia e carbono). O vapor de fósforo produzido é oxidado a pentóxido de fósforo, que reage com o vapor de água .
Usos
O ácido fosfórico é amplamente utilizado em laboratório porque é resistente à oxidação , redução e evaporação.
O ácido fosfórico é usado em refrigerantes como um regulador de pH ( E338 ): principalmente em refrigerantes na Cola ( Coca Cola , Pepsi Cola , Dr. Pepper ).
O ácido fosfórico é usado como componente em fertilizantes , detergentes , cimentos dentais como catalisador ou em metais inoxidáveis, e na produção de fosfatos - usados em amaciantes de água.
O ácido fosfórico é frequentemente usado em solução em produtos usados na mecânica para remover a ferrugem de peças de metal. Também é utilizado para a fosfatação de peças metálicas para protegê-las da oxidação ao ar livre.
O ácido fosfórico também é usado como eletrólito nas células a combustível PAFC .
Riscos
A ingestão de uma grande quantidade de ácido fosfórico pode interferir na função renal e promover cálculos renais . Pesquisadores americanos entrevistaram 465 pessoas recentemente diagnosticadas com insuficiência renal e descobriram, a partir da descrição de sua dieta, que com dois copos de Coca-Cola por dia, o risco de insuficiência renal é multiplicado por dois. É o mesmo com a Coca-Cola light, embora nenhuma associação tenha sido encontrada com outros refrigerantes.
Troca
A França, em 2014, é um importador líquido de ácido fosfórico, de acordo com os costumes franceses. O preço médio de importação por quilograma foi de € 0,9.
Notas e referências
Notas
- Este ponto de fusão é que a do ácido fosfórico puro. No entanto, quando o ácido fosfórico é aquecido a uma temperatura próxima a este valor, ele se decompõe parcialmente após a reação: 2 H 3 PO 4⇌ H 2 S+ H 4 P 2 O 7. O ponto de ebulição da mistura diminui gradualmente com o avanço dessa decomposição até 34,6 ° C no equilíbrio.
Referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (em) NN Greenwood , Chemistry of the Elements , Boston Oxford, Butterworth-Heinemann,1997( ISBN 0-7506-3365-4 , OCLC 37499934 ) , p. 518.
- " Phosphoric Acid " , no Hazardous Substances Data Bank (acessado em 27 de novembro de 2009 ) .
- PHOSPHORIC ACID , folha de segurança (s) de Programa Internacional sobre a Segurança das Substâncias Químicas , consultado sobre 09 maio de 2009
- Número de índice na tabela 3.1 do apêndice VI do regulamento CE nº 1272/2008 (16 de dezembro de 2008)
- " Ácido fosfórico " no banco de dados de produtos químicos Reptox da CSST (organização de Quebec responsável pela segurança e saúde ocupacional), acessado em 23 de abril de 2009
- "ácido ortofosfórico" , em ESIS , acessado em 3 de março de 2010
- Robin des Bois Association (2005) Technologicamente aprimorada radioatividade natural ), dezembro de 2005.
- Isabelle Eustache, " Sem coca, é melhor para os rins!" » , Em e-sante.fr ,23 de julho de 2007(acessado em 15 de maio de 2008 ) .
- (in) Saldana TM, Basso O., R. Darden e Sandler DP, " Carbonated drinks andronic kidney disease " , em ncbi.nlm.nih.gov ,18 de julho de 2007(acessado em 16 de abril de 2009 ) .
- " Indicador de comércio de importação / exportação " , na Direção Geral das Alfândegas. Indique NC8 = 28092000 (acessado em 7 de agosto de 2015 )
Apêndices
Artigos relacionados
- Ácido metafosfórico
- Ácido pirofosfórico
- Ácido trifosfórico
- Ácido arsênico
- Ácido Cítrico
- Ácido málico
links externos
- "Ácido fosfórico - folha de dados toxicológicos n o 37" , INRS , novembro de 2020
- (en) “Ácido fosfórico” NIOSH , 30 de outubro de 2019

