Composto organoboro
Os compostos de organoboro são uma classe de compostos orgânicos compreendendo pelo menos uma conexão entre um átomo de carbono e um átomo de boro . O termo "organoborano" às vezes é usado como sinônimo de um composto de organoboro, mas também é usado em um sentido mais restrito para designar apenas derivados alquilados ou arilados de borano (BH 3 ), como trialquilboranos (B R 3 ). Outras famílias importantes de compostos de organoboro incluem ácidos borônicos e ésteres borônicos.
-
Organoboran (no sentido restrito)
-
Ácido borônico
-
Éster borônico
Os compostos organoboron são reagentes importantes na química orgânica, permitindo inúmeras transformações químicas, a mais importante das quais é a hidroboração .
Ligação carbono - boro
A ligação carbono - boro (CB) é fracamente polar devido à pequena diferença na eletronegatividade entre o carbono (2,55) e o boro (2,04). Como resultado, os alquilboranos são geralmente estáveis, mas facilmente oxidáveis .
Em parte devido à sua eletronegatividade mais baixa, os compostos de boro freqüentemente formam déficit de elétrons (in) , como os triorganoboranos. Os grupos vinil e aril tendem a doar seus elétrons, tornando o boro menos eletrofílico , dando à ligação CB um caráter de ligação dupla . Os derivados orgânicos do diborano são classificados na química orgânica como eletrófilos fortes porque o boro é incapaz de obter um octeto de elétrons neles.
Classes de compostos
Organoborans e hidretos
Uma das classes mais estudadas de compostos de organoboro é a dos compostos de fórmula BR n H 3 - n . Esses compostos são usados como catalisadores , reagentes ou intermediários de reação. Os derivados trialquil e triaril exibem uma geometria plana trigonal ao redor do centro do boro e são tipicamente ácidos de Lewis fracos. Com exceção de alguns derivados muito grandes, os hidretos (BR n H 3 - n com n = 1 ou 2) existem como dímeros, como o próprio borano . Os derivados trissubstituídos, como o trietilborano, são eles próprios monoméricos.
Ácidos e ésteres borínicos e borônicos (BR n (OR) 3-n )
Os compostos da BR n (OH) 3-n tipo são chamados ácidos Borínicos (n = 2) e ácidos borónicos (n = 1), e os da BR n (OR) 3-n tipo são Borínicos e borónicos ésteres . Os casos para n = 0 correspondem, respectivamente, ao ácido bórico e aos boratos, que não são considerados compostos de organoboro por não conterem uma ligação carbono-boro. O borato de trimetila , B (OCH 3 ) 3 , é usado como ésteres borônicos precursores para o acoplamento de Suzuki .
Aglomerados de boro
O boro é conhecido por formar aglomerados , por exemplo dodecaborato (en) [B 12 H 12 ] 2- . Muitos derivados orgânicos são conhecidos por formar tais aglomerados. Um exemplo é [B 12 (CH 3 ) 12 ] 2- e seu derivado de radical [B 12 (CH 3 ) 12 ] - . Os compostos relacionados a aglomerados compreendendo átomos de carbono são chamados carboranos . O mais conhecido é o ortocarborano , de fórmula C 2 B 10 H 12 . Embora tenham poucas aplicações comerciais, os carboranos têm atraído muita atenção devido à sua estrutura incomum. Seus derivados aniônicos, os dicarbolídeos, por exemplo [C 2 B 9 H 11 ] 2− , são ligantes que se comportam como ciclopentadienida .
Compostos aromáticos substituídos por boro
Existem compostos aromáticos derivados de hidrocarbonetos aromáticos onde um grupo CH é substituído por um átomo de boro. É por exemplo o caso do borabenzeno (en) (C 5 H 5 B). Este tipo de composto é sempre isolado sob a forma de aductos de, por exemplo, C 5 H 5 B-piridina. O borol , um análogo estrutural do pirrol ou do azol , nunca foi isolado, mas conhecemos derivados substituídos. A borépina (sete heterocíclica) foi isolada e ao contrário da azepina ou oxepina , é aromática.
Boryles
Os ânions Boryl têm a fórmula R 2 B - . Os compostos boril aniônicos nucleofílicos há muito tempo são elusivos, mas um estudo de 2006 descreveu um composto borilítio, que reage como um nucleófilo. Os compostos organometálicos com ligações metal-boro (ou seja, M-BR 2 ) são conhecidos com o nome de complexo de borila. Os ligantes associados são chamados de boriolos (M - B (R) –M).
A ausência de compostos de lítio de boyle é notável porque os sais de lítio são comuns entre outros membros do segundo período , por exemplo o fluoreto de lítio , o hidróxido de lítio , a amida de lítio ou metil-lítio . Esta ausência sublinha a eletronegatividade muito baixa do boro. As reações de bases com hidretos de boro (R 2 BH) não resultam em desprotonação para o ânion boril R 2 B - , mas na formação do ânion boril R 2 B - H (base) + , que possui um byte completo. Em vez disso, o composto é preparado por bromyl redutiva heterólise de uma ligação boro-bromo por metálico lítio . Este composto de borilítio é muito semelhante e isoeletrônico aos carbenos N-heterocíclicos . Ele se beneficia da estabilização aromática (6 elétrons contando os dupletos de nitrogênio livre e o orbital p vazio do boro - estrutura A) e da estabilidade cinética de grupos 2,6-diisopropilfenil volumosos. A cristalografia de raios X é usada para confirmar um boro de hibridização sp2 , e o fato de ele reagir por adição nucleofílica com o benzaldeído é mais uma evidência de que adota a estrutura proposta por ben.
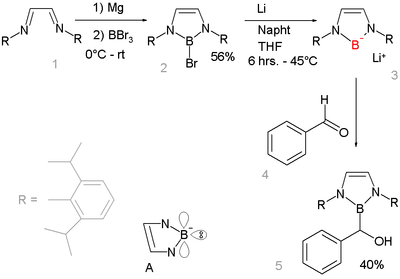
Alquilideneboranos
Alquilidenoboranos, RB = compostos do tipo CRR com uma ligação dupla carbono-boro são raros. O composto original desta subclasse é HB = CH 2 , que pode ser detectado em baixas temperaturas. Um derivado razoavelmente estável é CH 3 B = C (SiMe 3 ) 2 , mas tende a ciclodimerizar .
Adutos de boro NHC
Os carbenos N-heterocíclicos (NHC) e os boranos formam adutos estáveis, os NHC boranos . Os adutos de trietilborano podem ser sintetizados diretamente a partir do sal de imidazólio e trietilboro-hidreto de lítio . Membros desta classe de compostos estão sendo estudados para uso como reagentes ou catalisadores.
Diborenes
Os compostos que contêm uma ligação dupla boro - boro são raros. Em 2007, o primeiro diboreno neutro (RHB = BHR) foi apresentado por Gregory Robinson, da Universidade da Geórgia . Cada átomo de boro tem um próton ligado a ele e é coordenado a um carbeno N-heterocíclico (NHC). A estrutura parental com ligantes carbenos adicionais é o diborano (2) .

Um diboryne foi relatado, com base em uma química semelhante.
Síntese
De reagentes Grignard
Organoboranos simples como trietilborano ou tris (pentafluorofenil) borano podem ser preparados a partir de trifluoroborano e o correspondente reagente de Grignard etil ou pentafluorofenil. Boratos (R 4 B - ) são produzidos pela adição de R - equivalentes (RMgX, RLi, etc.) a R 3 B.
De alcenos
De alcenos podem ser inseridos em ligações BH de boranos em um processo denominado hidroboração . A hidroboração de alcenos ou alcinos por borano (BH 3 ) ou seus derivados converte apenas cerca de 33% dos reagentes iniciais, sendo o restante incluído após oxidação ou protonólise em subprodutos borados. Um reagente organoboro comumente usado na síntese é o 9-BBN . A hidroboração é sin estereoespecífica e fornece o produto anti-Markovnikov .
Por borilação
A reação de borilação CH catalisada por metal é uma reação orgânica catalisada por metal de transição que produz compostos organoboro por funcionalização de ligações C - H alifáticas ou aromáticas. Uma corrente reativa para esse tipo de reação é o bis (pinacolato) diborano (en) .
Reatividade
A ligação carbono-boro é levemente polarizada em direção ao carbono, o que a torna nucleofílica . Esta propriedade é explorada para transferir um dos grupos R para um centro eletrofílico inter- ou, mais frequentemente, intramolecularmente. No último caso, o grupo nuclofílico R é capaz de sofrer uma migração 1,2 em direção ao carbono eletrofílico ligado ao boro. O borano resultante pode então ser oxidado ou ser sujeito a protonólise para dar vários compostos orgânicos:

Hidroboração-oxidação
Na síntese orgânica , a reação de hidroboração é levada adiante para gerar outros grupos funcionais no lugar do grupo de boro. A reação de hidroboração-oxidação (in) fornece um caminho para os álcoois por oxidação do borano com peróxido de hidrogênio , ou para os compostos de carbonila com um oxidante mais forte como o trióxido de cromo .
Reorganizações
O monóxido de carbono reage com trialquilboranos. Segue-se um rearranjo 1,2 em que um substituinte alquil migra do boro para o carbono do grupo carbonil. É, portanto, possível obter álcoois primários homólogos por tratamento de organoboranos com monóxido de carbono e um hidreto:
Alilboração
A alilboração assimétrica é outra maneira conveniente de formar ligações carbono-carbono com organoboros. Pode ser mencionada, por exemplo, a síntese de Nicolaou de epotilonas em que uma alilboração assimétrica (usando alilborano derivado do α-pineno ) é usada em conjunto com uma proteção por TBS e ozonólise . Isso geralmente resulta em uma homologação adicionando dois carbonos, produzindo a sequência de acetogenina desejada .
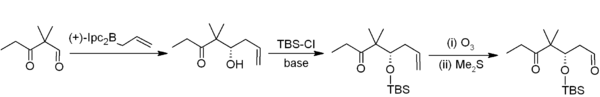
Redutor
Hidretos de borano, tais como 9-BBN ou L-Selectride (tri-sec-butilboro-hidreto de lítio) são usados como agentes redutores . O catalisador CBS que contém boro é usado como um catalisador assimétrico para a redução de carbonilas .
Boratos
Os trialquilboranos (BR 3 ) podem ser oxidados em seus boratos correspondentes (B (OR) 3 ). Esta oxidação também pode ser usada em análises químicas para determinar o número de ligações carbono-boro contidas em um composto a ser analisado; o composto é então feito reagir com óxido de trimetilamina (Me 3 N), a trimetilamina (Me 3 N) formada, em seguida, a ser titulada .
Boratos podem ser convertidos em ácidos borônicos (RB (OH) 2 ) por reação com um reagente de Grignard seguido por hidrólise. Estes ácidos podem então reagir com bifluoreto de potássio (K [HF 2 ]) para formar sais trifluoroborato (K [RBF 3 ]), precursores dos nucleófilos alquil e difluoreto de aril, ArBF 2 . Esses sais são mais estáveis do que os próprios ácidos borônicos e são usados, por exemplo, para a alquilação de certos aldeídos :

Reação de Suzuki e reações relacionadas
Os compostos de organoboro também se prestam a reações de transmetalação , em particular com os compostos de organopaládio. Este tipo de reação é ilustrado pela reação de Suzuki , que envolve o acoplamento de um ácido aril - ou vinil - borônico com um halogeneto de aril ou vinil , catalisado por um complexo de paládio (0) .

Esta reação é um método importante na criação de ligações carbono-carbono .
Outros usos
O trietilborano (TEB) foi usado para acender o combustível JP-7 do motor de ciclo variável (en) Pratt & Whitney J58 que equipa o Lockheed SR-71 Blackbird .
Notas
- A síntese mostrada aqui começa com a reação de brometo de alilmagnésio com borato de trimetila , seguida pela hidrólise do éster borônico em ácido borônico por ácido clorídrico . O aldeído alquilado é p- nitrobenzaldeído .
Referências
- (fr) Este artigo foi retirado parcial ou totalmente do artigo da Wikipedia em inglês intitulado " Química Organoboron " ( ver a lista de autores ) .
- Ruth A. Bartlett , HV Rasika Dias , Marilyn M. Olmstead , Philip P. Power e Kenneth J. Weese , “ Synthesis of the monomeric HBtrip 2 (Trip - 2,4,6-iso-Pr3C6H2) e o raio-x estruturas cristalinas de [HBMes2] 2 (Mes = 2,4,6, -Me3C6H2) e HBtrip2 ”, Organometallics , vol. 9,1990, p. 146-150 ( DOI 10.1021 / om00115a023 )
- (in) Brown, HC, Organic Syntheses via borano , New York, John Wiley & Sons ,1975( ISBN 0-471-11280-1 )
- Grimes, RN, Carboranes, 3ª edição , New York, Academic Press,2016( ISBN 9780128019054 )
- Segawa Yasutomo, Yamashita Makoto, Nozaki Kyoko, " Boryllithium: Isolation, Characterization, and Reactivity as a Boryl Anion ", Science , vol. 314, n o 5796,2006, p. 113–115 ( PMID 17023656 , DOI 10.1126 / science.1131914 , Bibcode 2006Sci ... 314..113S )
- Bethany Halford Boron Attacks Elemento eletropositivo acionado como borilítio nucleofílico Chemical & Engineering News 2006; Volume 84 (41): 11 Link
- Ácidos Borônicos: Preparação, Aplicações em Síntese Orgânica e Medicina . Dennis G. Hall ( ISBN 3-527-30991-8 )
- Paetzold Peter, Englert Ulli, Finger Rudolf, Schmitz Thomas, Tapper Alexander, Ziembinski Ralf, " Reactions at the Boron-Carbon Double Bond of Methyl (methylidene) boranes ", Z. Anorg. Allg. Chem. , vol. 630, n o 4,2004, p. 508-518 ( DOI 10.1002 / zaac.200300396 )
- Curran DP, Solovyev A., Makhlouf Brahmi M., Fensterbank L., Malacria M., Lacôte E., " Synthesis and Reactions of N-Heterocyclic Carbene Boranes ", Angewandte Chemie International Edition , vol. 50, n o 44,2011, p. 10294–10317 ( PMID 21898724 , DOI 10.1002 / anie.201102717 )
- Yuzhong Wang, Brandon Quillian, Pingrong Wei, Chaitanya S. Wannere, Yaoming Xie, R. Bruce King , Henry F. Schaefer, III , Paul v. R. Schleyer e Gregory H. Robinson, " A Stable Neutral Diborene Containing a B = B Double Bond ", J. Am. Chem. Soc. , vol. 129, n o 41,2007, p. 12412–12413 ( PMID 17887683 , DOI 10.1021 / ja075932i , leia online )
- diboreno neutro é o primeiro Ron Dagani Chemical & Engineering News , 1 de outubro de 2007 Volume 85, Número 40 p. 10 [1]
- (em) Holger Braunschweig e Rian D. Dewhurst , " Single, Double, Triple and Chains Bonds: The Formation of Electron-Precise BB Bonds " , Angewandte Chemie International Edition , Vol. 52, n o 13,25 de março de 2013, p. 3574-3583 ( ISSN 1521-3773 , PMID 23362015 , DOI 10.1002 / anie.201208189 )
- (em) Merle Arrowsmith , Holger Braunschweig e Tom E. Stennett , " Formation and Reactivity of Precise Electron-B-B Single and Multiple Bonds " , Angewandte Chemie International Edition , Vol. 56, n o 1,2 de janeiro de 2017, p. 96-115 ( ISSN 1521-3773 , PMID 27860056 , DOI 10.1002 / anie.201610072 , ler online )
- Advanced Organic Chemistry , FA carey, RJ Sundberg ( ISBN 0-306-41088-5 )
- Negishi, E.-i.; Idacavage, M. J, “ Formation of Carbon - Carbon and Carbon - Heteroatom Bonds via Organoboranes and Organoborates ”, Org. Reagir. , vol. 33, n o 1,1985, p. 1-246 ( DOI 10.1002 / 0471264180.or033.01 )
- Herbert Charles Brown, Michael W. Rathke, “ Reação do monóxido de carbono à pressão atmosférica com trialquilboranos na presença de boro-hidreto de sódio ou lítio. Um procedimento conveniente para a oximetilação de olefinas via hidroboração ”, J. Am. Chem. Soc , vol. 89, n o 11,1967, p. 2740-2741 ( DOI 10.1021 / ja00987a044 )
- Lachance H., Hall D., Allylboration of Carbonyl Compounds , vol. 73,2008( ISBN 978-0471264187 , DOI 10.1002 / 0471264180.or073.01 ) , p. 1
- Nicolaou, KC, Sarabia, F., Ninkovic, S., Finlay, MRV e Boddy, CNC, " Probing the Ring Size of Epothilones: Total Synthesis of 14-, 15-, 17- and 18 Epothilones A ", Angewandte Chemie International Edition em inglês , vol. 37, n osso 1-2,1998, p. 81–84 ( DOI 10.1002 / (sici) 1521-3773 (19980202) 37: 1/2 <81 :: aid-anie81> 3.0.co; 2-c , ler online , acessado em 2 de março de 2008 )
- Vedejs E., Chapman RW, Fields SC, Lin S., Schrimpf MR, “ Conversion of Arylboronic Acids into Potassium Aryltrifluoroborates: Convenient Precursors of Arylboron Difluoride Lewis Acids ”, J. Org. Chem. , vol. 60, n o 10,1995, p. 3020-3027 ( DOI 10.1021 / jo00115a016 )
- Molander Gary A., Canturk Belgin, “ Organotrifluoroborates and Monocoordinated Palladium Complexes as Catalysts - A Perfect Combination for Suzuki - Miyaura Coupling ”, Angew. Chem. Int. Ed. , Vol. 48, n o 49,2009, p. 9240-9261 ( PMID 19899086 , PMCID 2917751 , DOI 10.1002 / anie.200904306 )
- Batey Robert A., Quach Tan D., Shen Ming, Thadani Avinash N., Smil David V., Li Sze-Wan, MacKay D. Bruce, “ Compostos organoborons como nucleófilos leves em C catalisado por ácido de Lewis e metal de transição –C reações de formação de ligações ”, Pure Appl. Chem. , vol. 74, n o 1,2002, p. 43–55 ( DOI 10.1351 / pac200274010043 , leia online )
- Miyaura, Norio e Suzuki, Akira, “ Palladium-Catalyzed Cross-Coupling Reactions of Organoboron Compounds ”, Chemical Reviews , vol. 95, n o 7,1995, p. 2457–2483 ( DOI 10.1021 / cr00039a007 )
| CH | Ei | |||||||||||||||||
| CLi | CBe | CB | CC | CN | CO | CF | Nascer | |||||||||||
| CNa | CMg | CAl | CSi | PC | CS | CCl | Porque | |||||||||||
| CK | CCa | CSc | CTi | cv | CCr | CMn | CFe | CCo | CNi | CCu | CZn | CGa | CGe | Caso | CSe | CBr | CKr | |
| CRb | CSr | CY | CZr | CNb | CMo | CTc | Cru | CRh | CPd | CAg | CCd | CIn | CSn | CSb | CTe | ESTA | CXe | |
| CCs | CBa | * | CLu | CHf | CTa | CW | CRe | COs | CIr | CPt | CAu | CHg | CTl | CPb | CBi | CPo | Gato | Rn |
| Fr | CRa |
* * |
Lr | Rf | Db | CSg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og |
| ↓ | ||||||||||||||||||
| * | CLa | CCe | CPr | CNd | CPm | CSm | Este U | CGd | CTb | CDy | CHo | CEr | CTm | CYb | ||||
|
* * |
Ac | CTh | CPa | CU | CNp | CPU | CAm | CCm | CBk | CCf | Esses | Fm | Md | Não | ||||
| Ligação básica em química orgânica | Muitos usos em química |
| Pesquisa acadêmica, mas não de uso comum | Link desconhecido / não avaliado |
![{\ displaystyle {\ ce {2R3B \ + 3CO \ + 4H ^ {-} -> [{\ text {DG}}] [{\ text {45 °}}] -> [{\ text {KOH}}] 4ROH \ + 2RCH2OH}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/8056c0c6f13913bf9ca66a88c6b538c1b6ce5d23)