Diciclohexilcarbodiimida
| Diciclohexilcarbodiimida | |||
 
|
|||
| Identificação | |||
|---|---|---|---|
| Nome IUPAC | N, N'-diciclohexilmetanodiimina | ||
| Sinônimos |
N, N'-diciclohexilcarbodiimida |
||
| N o CAS | |||
| N o ECHA | 100.007.914 | ||
| N o EC | 208-704-1 | ||
| N o RTECS | FF2160000 | ||
| PubChem | 10868 | ||
| ChEBI | 53090 | ||
| SORRISOS |
C1CCC (CC1) N = C = NC2CCCCC2 , |
||
| InChI |
InChI: InChI = 1S / C13H22N2 / c1-3-7-12 (8-4-1) 14-11-15-13-9-5-2-6-10-13 / h12-13H, 1- 10H2 InChIKey: QOSSAOTZNIDXMA-UHFFFAOYSA-N |
||
| Aparência | sólido incolor com odor característico | ||
| Propriedades quimicas | |||
| Fórmula bruta |
C 13 H 22 N 2 [Isômeros] |
||
| Massa molar | 206,3272 ± 0,0123 g / mol C 75,68%, H 10,75%, N 13,58%, |
||
| Propriedades físicas | |||
| Fusão T ° |
34 a 35 ° C 34,5 a 37,0 ° C 35 a 36 ° C |
||
| T ° fervendo |
122 a 124 ° C 122 a 124 ° C a 6 mmHg |
||
| Solubilidade | CH 2 Cl 2 substancialmente insolúvel em água 0,1 g · ml -1 |
||
| Massa volumica | 0,95 g · cm -3 a 40 ° C | ||
| Ponto de inflamação | 113 ° C | ||
| Precauções | |||
| SGH | |||
  H302, H311, H317, H318, P280, P312, P305 + P351 + P338,
H302 : Nocivo por ingestão
H302, H311, H317, H318, P280, P312, P305 + P351 + P338,
H302 : Nocivo por ingestão H311 : Tóxico em contato com a pele H317 : Pode causar uma reação alérgica na pele H318 : Provoca lesões oculares graves P280 : Usar luvas de proteção / roupas de proteção / proteção ocular / proteção facial. P312 : Contacte um CENTRO DE INFORMAÇÃO ANTIVENENOS ou um médico / médico se não se sentir bem. P305 + P351 + P338 : Se entrar em contato com os olhos: enxágue cuidadosamente com água por vários minutos. Remova as lentes de contato se a vítima as usar e elas podem ser facilmente removidas. Continue a enxaguar. |
|||
| NFPA 704 | |||
| 1 3 0 | |||
| Transporte | |||
2811 : SÓLIDO TÓXICO, ORGÂNICO, Classe NOS : 6.1 Etiqueta: 6.1 : Material tóxico  |
|||
| Ecotoxicologia | |||
| DL 50 | 400 mg / kg (rato, oral ) | ||
| Unidades de SI e STP, salvo indicação em contrário. | |||
A N, N'-diciclohexilcarbodiimida ou DCC é um composto orgânico da família das carbodiimidas utilizado principalmente como reagente para o acoplamento de aminoácidos na síntese de peptídeos .
Síntese
Muitas rotas sintéticas foram desenvolvidas, a mais recente via reação de acoplamento oferece melhores rendimentos. Historicamente, o DCC foi formado pela desidratação da di- ciclohexil - ureia pelo cloreto de paratoluenossulfonila na presença de trifenilfosfina e trietilamina como bases . Da mesma forma, os diciclo tioureia reage com o óxido de mercúrio para formar um intermediário no qual o átomo de enxofre é trocado pelo oxigénio . Sua desidratação, então, forma DCC:

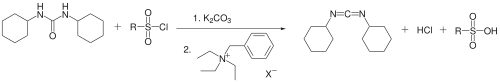
Em 1987, a utilização de carbonato de potássio em vez de trifenilfosfina e trietilamina como base e de um catalisador de transferência de fase pelo grupo de Zsuzsa Jaszay permite obter um rendimento de 50%. Diciclohexilureia, cloreto de arenossulfonil e carbonato de potássio reagem em tolueno na presença de cloreto de benzil trietilamônio para dar N, N'-diciclohexilcarbodiimida:
Ilan Pri-Bara e Jeffrey Schwartz usam acetato de paládio , iodo e oxigênio para acoplar ciclohexilamina e ciclohexil isocianeto . Rendimentos de até 67% foram obtidos seguindo esta rota:
C 6 H 11 NH 2 + C 6 H 11 N≡C + O 2 → (C 6 H 11 N) 2 C + H 2 O.Condensar a equipa de Jiansheng Tang dois isocianatos utilizando o OP (Mench 2 CH 2 ) 3 N catalisador com um rendimento de 92%:

Propriedades e caracterização
O DCC é um pó incolor com um odor forte e doce característico. O baixo ponto de fusão deste composto permite que ele seja derretido para facilitar o manuseio. É muito solúvel em diclorometano , tetrahidrofurano , acetonitrila e dimetilformamida , mas insolúvel em água.
O núcleo N = C = N das carbodiimidas é linear e está estruturalmente relacionado aos alenos (C = C = C). Três estruturas de ressonância principais descrevem carbodiimidas:
RN = C = NR ↔ RN + ≡CN - R ↔ RN - -C≡N + R.Este padrão N = C = N tem uma assinatura característica na espectroscopia de IV em 2117 cm −1 . O espectro de NMR de 15 N mostra uma característica de deslocamento químico de 275,0 ppm no campo superior em relação ao ácido nítrico e o espectro de NMR de 13 C tem um pico a cerca de 139 ppm a jusante do TMS .
Usar
O DCC é um reagente que pode ser usado para desidratação , esterificação e outras ativações sob condições muito suaves.
Desidratação
DCC é um agente desidratante para a preparação de alcenos , nitrilos . Nessas reações, o DCC se hidrata para formar diciclohexilureia (DCU), que é insolúvel em água.
Assim, a desidratação de álcoois ocorre dando primeiro o intermediário O-acil ureia que é então cortado por hidrogenólise para produzir o alceno correspondente:
RCHOHCH2R '+ (C 6 H 11 N) 2 C → RCH = CHR' + (C 6 H 11 NH) 2 CO.Oxidação Moffatt
Uma solução de DCC em dimetilsulfóxido (DMSO) permite o que é chamado de oxidação de Pfitzner-Moffatt . Esta reação é usada para a oxidação de álcoois em aldeídos e cetonas. Ao contrário das oxidações por meio de íons metálicos , as condições com DCC são suaves o suficiente para evitar a oxidação excessiva de aldeídos em ácidos carboxílicos . Em geral, três equivalentes de DCC por 0,5 equivalente de álcool em DMSO são deixados durante a noite à temperatura ambiente. A reação é interrompida por acidificação.
Esterificação e amidação
O DCC é principalmente utilizado na síntese de ésteres e amidas orgânicas, em particular quando os compostos a reagir são dificultados ou pouco reativos, permite um aumento significativo dos rendimentos. Além disso, ele realiza, ao contrário da esterificação de Fischer, essas esterificações e amidações em condições muito suaves, o que é muito vantajoso com compostos nucleofílicos baixos , como o álcool terc-butílico .
Portanto, o DCC também desempenha um papel importante na síntese de peptídeos in vitro e na introdução de grupos de proteção .
Inversão de álcoois secundáriosOs álcoois secundários podem ser estereoquimicamente revertidos pela formação de um éster formílico , seguido de saponificação . O álcool secundário é misturado diretamente com DCC, ácido fórmico e uma base forte como o metóxido de sódio .
Esterificação SteglichUma ampla gama de álcoois, incluindo até mesmo alguns álcoois terciários, podem ser esterificados com um ácido carboxílico na presença de DCC e uma quantidade catalítica de 4-dimetilaminopiridina , DMAP.
Na verdade, qualquer grupo carboxila (> C = O) adiciona-se rapidamente a uma das ligações duplas C = N de DCC, formando o derivado O-acil ureia correspondente. Este intermediário é muito reativo, sendo sua reatividade comparável à de um anidrido de ácido , de modo que é rápida e facilmente convertido em uma amida por reação com uma amina . Para o seu acoplamento com álcoois, um agente de transferência de acila como DMAP é adicionalmente necessário. Isso é chamado de esterificação de Steglich. Em suma, o resultado dessas condensações do ácido ligado ao DCC com um álcool ou uma amina é um éster ou uma amida, respectivamente, e uma molécula de água capturada pelo DCC que se transforma em N, N'-diciclohexilureia, (C 6 H 11 -NH) 2 C = O.
Acoplamento de peptídeo promovido por DCCDurante a síntese de peptídeos ou proteínas (por exemplo, pelo sintetizador de estado sólido Fmoc ), o terminal N é frequentemente usado como o local de ligação ao qual os aminoácidos são adicionados. Para melhorar a eletrofilicidade do grupo carboxilato do aminoácido desprotonado a ser adicionado, o átomo de oxigênio carregado negativamente deve primeiro ser ativado em um grupo de saída melhor . O DCC é usado para este propósito. O átomo de oxigênio carregado negativamente que é, portanto, nucleofílico facilmente ataca o átomo de carbono central do DCC que é, portanto, temporariamente ligado ao grupo carboxilato e forma um intermediário altamente eletrofílico, o que torna o ataque nucleofílico pelo grupo amino terminal do peptídeo em uma construção muito mais eficaz .
segurança
Além de ser tóxica, a diciclohexilcarbodiimida também é um forte alérgeno e efeito sensibilizante , muitas vezes causando erupções cutâneas .
Notas e referências
- ( fr ) Este artigo foi retirado parcial ou totalmente do artigo da Wikipedia em inglês intitulado " N, N'-Dicyclohexylcarbodiimide " ( ver a lista de autores ) .
- (de) Este artigo foi retirado parcial ou totalmente do artigo da Wikipedia em alemão intitulado “ Diciclohexilcarbodiimid ” ( ver lista de autores ) .
- (en) " Diciclohexilcarbodiimida " , no ChemIDplus
- Entrada "Diciclohexilcarbodiimid" na base de dados química GESTIS do IFA (organismo alemão responsável pela segurança e saúde ocupacional) ( alemão , inglês ) (JavaScript necessário)
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- N, N'-diciclo-hexilcarbodiimida ≥99.0% (GC) a partir de Sigma-Aldrich .
- (de) R. Appel, R. Kleinstück, K.-D. Ziehn, Über die gemeinsame Einwirkung von Phosphinen und Tetrachlorkohlenstoff auf Ammoniak (Derivado), IV Notiz über eine neue Carbodiimid-Synthese , Chem. Ber. , 1971, vol. 104, pág. 1335-1336. DOI : 10.1002 / cber.19711040438 .
- (De) S. Hauptmann, J. Graefe, H. Remane, Lehrbuch der organischen Chemie ' , Deutscher Verlag für Grundstoffindustrie, Leipzig, 1976, p. 433.
- Zsuzsa Jaszay, Imre Petnehazy, Laszlo Toke, Bela Szajani, Preparation of Carbodiimides Using Phase-Transfer Catalysis , Synthesis , 1987, vol. 5 (5), pág. 520-523. DOI : 10.1055 / s-1987-27992 .
- Ilan Pri-Bara, Jeffrey Schwartz, síntese de N, N-dialquilcarbodiimida por acoplamento catalisado por paládio de aminas com isonitrilos , Chem. Comum. , 1997, vol. 4 (4), pág. 347. DOI : 10.1039 / a606012i .
- Jiansheng Tang, Thyagarajan Mohan, John G. Verkade, selectiva e a síntese eficiente de per-hidro-1,3,5-triazina-2,4,6-trionas e carbodiimidas a partir de isocianatos Usando ZP (Mench 2 CH 2 ) s N Catalysts . J. Org. Chem. , 1994, vol. 59 (17), p. 4931-4938. DOI : 10.1021 / jo00096a041 .
- Issa Yavari, John D. Roberts, Nitrogen-15 Nuclear Magnetic Resonance Spectroscopy. Carbodiimidas . J. Org. Chem. , 1978, vol. 43 (25), p. 4689–4690. DOI : 10.1021 / jo00419a001 .
- H. Wiener, C. Gilon, Um método melhorado para a preparação catalítica de ésteres t-butílicos de ácido carboxílico e graxo , J. Mol. Catal. , 1986, vol. 37, pág. 45-52. DOI : 10.1016 / 0304-5102 (86) 85136-7 .
- B. Neises, W. Steglich, Esterification of Carboxylic Acids with Dicyclohexylcarbodiimide / 4-Dimethylaminopyridine: Tert-Butyl Ethyl Fumarate , Org. Synth. , col. " voar. 7 ",1990, p. 93
- B. Neises, W. Steglich, Simple Method for the Esterification of Carboxylic Acids , Angew. Chem. Int. Ed. , 1978, vol. 17, pág. 522-524. DOI : 10.1002 / anie.197805221 .
- R. Milcent e F. Chau, Química orgânica heterocíclica: Estruturas fundamentais, química e bioquímica dos principais compostos naturais , EDP Sciences, 2003. ( ISBN 9782868835833 ) , apresentação online
- EFV Scriven, 4-Dialquilaminopiridinas: Catalisadores de Superacilação e Alquilação , Chem. Soc. Rev. , 1983, vol. 12, pág. 129-161.
