Óxido de propileno
| Óxido de propileno | |||
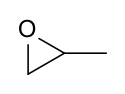 Estrutura do óxido de propileno |
|||
| Identificação | |||
|---|---|---|---|
| Nome IUPAC | metiloxirano | ||
| Sinônimos |
1,2-epoxipropano |
||
| N o CAS |
(RS) (R) - (+) (S) - (-) |
||
| N o ECHA | 100.000.800 | ||
| N o EC | 200-879-2 | ||
| PubChem | 6378 | ||
| ChEBI | 38685 | ||
| SORRISOS |
CC1CO1 , |
||
| InChI |
Padrão InChI: InChI = 1S / C3H6O / c1-3-2-4-3 / h3H, 2H2,1H3 Std. InChIKey: GOOHAUXETOMSMM-UHFFFAOYSA-N |
||
| Aparência | líquido incolor com odor de éter | ||
| Propriedades quimicas | |||
| Fórmula bruta |
C 3 H 6 O [Isômeros] |
||
| Massa molar | 58,0791 ± 0,0031 g / mol C 62,04%, H 10,41%, O 27,55%, |
||
| Propriedades físicas | |||
| Fusão T ° | -112 ° C | ||
| T ° fervendo | 34,4 ° C | ||
| Solubilidade | 680 g · l -1 a 20 ° C | ||
| Massa volumica | 0,83 g · cm -3 | ||
| Temperatura de autoignição | 430 ° C | ||
| Ponto de inflamação | -37 ° C | ||
| Ponto crítico |
209,1 C , 4,91 MPa |
||
| Precauções | |||
| SGH | |||
   Perigo H224, H302, H312, H315, H319, H332, H335, H340, H350, P201, P210, P261, P305 + P351 + P338, P308 + P313, H224 : Líquido e vapor extremamente inflamáveis H302 : Nocivo por ingestão H312 : Nocivo em contato com a pele H315 : Provoca irritação cutânea H319 : Provoca irritação ocular grave H332 : Nocivo por inalação H335 : Pode irritar as vias respiratórias H340 : Pode induzir anormalidades genéticas (indicar o via de exposição se for conclusivamente provado que nenhuma outra via de exposição leva ao mesmo perigo) H350 : Pode causar câncer (indique a via de exposição se for conclusivamente provado que nenhuma outra via de exposição leva ao mesmo perigo) P201 : Obtenha instruções especiais antes de usar. P210 : Manter afastado do calor / faísca / chama aberta / superfícies quentes. - Proibido fumar. P261 : Evite respirar poeira / fumaça / gás / névoa / vapores / spray. P305 + P351 + P338 : Se entrar em contato com os olhos: enxágue cuidadosamente com água por vários minutos. Remova as lentes de contato se a vítima as usar e elas podem ser facilmente removidas. Continue a enxaguar. P308 + P313 : Em caso de exposição comprovada ou suspeita: consultar um médico. |
|||
| Transporte | |||
33 : material líquido altamente inflamável (ponto de inflamação abaixo de 21 ° C ) Número da ONU : 1280 : ÓXIDO DE PROPILENO Classe: 3 Etiqueta: 3 : Líquidos inflamáveis Embalagem: Grupo de embalagem I : substâncias muito perigosas;  |
|||
| Classificação IARC | |||
| grupo 2B : possivelmente cancerígeno para humanos | |||
| Unidades de SI e STP, salvo indicação em contrário. | |||
O óxido de propileno ou 1,2-epoxipropano , é um composto químico de fórmula CH 3 CHCH 2 O. Apresenta-se sob a forma de um líquido combustível incolor, muito volátil, com odor a éter e capaz de formar misturas explosivas com o ar. É um epóxido quiral geralmente usado na forma racêmica . É usado principalmente para produzir polióis para a fabricação de poliuretanos . Tem um isômero , oxetano , cujo anel contém quatro átomos , não três.
Estereoquímica
O átomo de carbono que contém o substituinte metil é quiral . 1,2-epoxipropano, portanto, existe na forma de dois enantiômeros:
- ( R ) - (+) - 1,2-epoxipropano do número CAS
- ( S ) - (-) - 1,2-epoxipropano de número CAS
Produção
A produção industrial de óxido de propileno começa a partir de propileno CH 3 - CH = CH 2. Duas abordagens principais são usadas, a primeira por hidrocloração e a segunda por oxidação.
A rota de hidrocloração tradicional envolve a conversão de propileno em 1-cloro-2-propanol CH 3 -CHOH - CH 2 Cle 2-cloro-1-propanol CH 3 -CHCl - CH 2 OH :
2 CH 3 - CH = CH 2+ Cl 2+ H 2 S→ CH 3 -CHOH - CH 2 Cl+ CH 3 –CHCl - CH 2 OH.Esta mistura de cloropropanóis é então desidroclorada, por exemplo:
CH 3 -CHOH - CH 2 Cl+ OH - → CH 3 C 2 H 3 O+ Cl - + H 2 S.A cal é freqüentemente usada para absorver os íons Cl - cloreto .
A outra via principal de síntese do óxido de propileno é por meio da co-oxidação do etilbenzeno C 6 H 5 CH 2 CH 3e isobutano HC (CH 3 ) 3. Na presença de catalisadores , a oxidação do ar procede da seguinte forma:
CH 3 - CH = CH 2+ C 6 H 5 - CH 2 - CH 3+ O 2→ CH 3 C 2 H 3 O+ C 6 H 5 - CH = CH 2+ H 2 S.Os coprodutos dessas reações, seja estireno C 6 H 5 –CH = CH 2ou terc- butanol HOC (CH 3 ) 3, são matérias-primas importantes para outras reações. Por exemplo, terc- butanol pode reagir com metanol CH 3 OHpara dar éter metil terc-butílico CH 3 OC (CH 3 ) 3(MTBE), um aditivo para combustível automotivo : antes da restrição atualmente imposta ao uso do MTBE nos combustíveis pelos riscos ecológicos que acarreta, a rota sintética do propeno e do isobutano era uma das mais importantes.
Um processo alternativo começando com cumeno C 6 H 5 CH (CH 3 ) 2foi colocado em produção pela Sumitomo Chemical emabril de 2003. Esta é uma adaptação do processo por co-oxidação usando hidroperóxido de cumeno no lugar do hidroperóxido de etilbenzeno e reciclando o α-hidroxicumeno co-produzido em cumeno, por desidratação e hidrogenação .
Mais recentemente, a BASF e a Dow Chemical colocaram em produção sua primeira linha, implementando o processo HPPO no qual o propileno é oxidado por peróxido de hidrogênio H 2 O 2 :
CH 3 - CH = CH 2+ H 2 O 2→ CH 3 C 2 H 3 O+ H 2 S.Esse processo é conhecido por gerar apenas água como subproduto.
Detecção de espaço
O 14 de junho de 2016, Brett A. McGuire e colegas relatam a detecção de óxido de propileno na fase gasosa de uma casca molecular estendida a frio em torno de aglomerados protoestelares aninhados maciços na região de formação estelar B2 de Sagitário . Moléculas quirais já haviam sido detectadas em meteoritos e cometas em nosso sistema solar , mas este é o primeiro a ser detectado no espaço. É também uma das moléculas mais complexas detectadas até o momento no espaço interestelar .
Notas e referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- Entrada "Óxido de propileno" no banco de dados químico GESTIS do IFA (órgão alemão responsável pela segurança e saúde ocupacional) ( alemão , inglês ), acessado em 24 de fevereiro de 2013 (JavaScript necessário ) .
- Folha Sigma-Aldrich do composto Óxido de Propileno , consultada em 24 de fevereiro de 2013.
- [McGuire et al. 2016] Brett A. McGuire et al. , " Descoberta da molécula quiral interestelar óxido de propileno (CH 3 CHCH 2 O) "[" Descoberta da molécula quiral interestelar de óxido de propileno (CH 3 CHCH 2 O) ”], Ciência , Associação Americana para o Avanço da Ciência, vol. 352, n o 6292, 17 de junho, 2016 (primeira versão on-line 14 de junho, 2016), p. 1449-1452 ( ISSN 0036-8075 e 1095-9203 , DOI 10.1126 / science.aae0328 )Os co-autores do artigo são, além de Brett A. McGuire, P. Brandon Carroll, Ryan A. Loomis, Ian A. Finneran, Philip R. Jewell, Anthony J. Remijan e Geoffrey A. Blake. O artigo foi recebido pela editora em 31 de dezembro de 2015 e aceito para publicação em 11 de maio de 2016.
- “ uma molécula orgânica detectado no espaço ”, http://fr.canoe.ca ,16 de junho de 2016( leia online ).