Receiver Fas
| Receiver Fas | ||
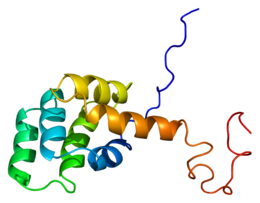 Domínio de morte de um receptor Fas humano ( PDB 1DDF ) | ||
| Principais características | ||
|---|---|---|
| Nome aprovado | Receptor de morte de superfície celular Fas | |
| Símbolo | FAS | |
| Sinônimos | TNFRSF6, APT1, ALPS1A, APO-1, CD95 | |
| Homo sapiens | ||
| Locus | 10 q 23,31 | |
| Peso molecular | 37 732 Da | |
| Número de resíduos | 335 aminoácidos | |
| Entre | 355 | |
| HUGO | 11920 | |
| OMIM | 134637 | |
| UniProt | P25445 | |
| RefSeq ( mRNA ) | NM_000043.5 , NM_001320619.1 , NM_152871.3 , NM_152872.3 | |
| RefSeq ( proteína ) | NP_000034.1 , NP_001307548.1 , NP_690610.1 , NP_690611.1 | |
| Juntos | ENSG00000026103 | |
| PDB | 1BZI , 1DDF , 2NA7 , 3EWT , 3EZQ , 3THM , 3TJE | |
|
GENATLAS • GeneTests • GoPubmed • HCOP • H-InvDB • Treefam • Vega | ||
| Links acessíveis a partir de GeneCards e HUGO . | ||
O receptor Fas (APO-1, CD95), conhecido como FasR , é uma proteína transmembrana pertencente à superfamília de receptores TNF , que pode induzir a morte celular por apoptose de células transformadas , mas também de linfócitos T humanos ativados. O sinal de morte celular pode ser induzida por anti-Fas anticorpos ou pelo ligando Fas ( FasL ), pertencente à família do TNF . A in vivo expressão destas duas moléculas FasR e FasL é regulada de forma diferente uma vez que a expressão de FasR é pleiotrópica enquanto FasL é em vez expressa nos sítios de privilégio imunitário ( testículos , ovários , cérebro , olho ) bem como por linfócitos T. Activada. As células tumorais, independentemente de suas origens nos tecidos, também podem expressar FasL (patológico).
Genética e imunológica estudos têm mostrado que o sistema Fas é por um lado envolvido no processo de periférico clonal eliminação permitindo a manutenção de auto-tolerância , por outro lado, que regula a amplitude ea duração da resposta imune. , E, finalmente, que representa um dos mecanismos de lise de células-alvo na resposta T citotóxica antiviral.
Quando a apoptose dependente de Fas não pode ocorrer, devido a mutações nos genes que codificam FasR ou FasL, síndrome linfoproliferativa e manifestações autoimunes são observadas em humanos e camundongos. Por outro lado, uma exacerbação do sistema Fas pode ser responsável pela destruição do tecido. Por exemplo, a única injecção num ratinho de anti-Fas anticorpos induz a destruição maciça do fígado e morte do rato dentro de algumas horas, que conduz à hipótese da participação do sistema Fas na hepatite fulminante .
Desencadeamento extrínseco da apoptose
Os receptores Fas são proteínas transmembrana de 335 resíduos de aminoácidos e 50 kDa , que, após a ligação de seus ligantes por seu N-terminal , são ativadas na forma de trímeros . O C-terminal intracelular compreende uma sequência de 80 resíduos de aminoácidos formando um domínio de morte ( domínio de morte em inglês ou DD). No caso de Fas, os três domínios de morte associados do trímero FasR ativado recrutam uma proteína citoplasmática FADD ( Fas Associating protein with Death Domain ) compreendendo dois domínios de proteína : um domínio DD que forma um dímero com o domínio DD de FasR, e um Domínio DED ( Death Effector Domain ) que se liga e ativa a pró- caspase 8 (forma zimogênica inativa da caspase 8 ). Ao ativar a procaspase 8, o FasR induz a cascata de ativações de proteínas levando à morte celular por apoptose. O FasR constitui a via extrínseca para desencadear a apoptose.
Não confunda
- FAS , ácido graxo sintase (do inglês: Fatty Acid Synthase ), enzima de formação de ácido graxo de malonil-CoA, Ref
- Fas significa fragmento de estimulação de apoptose ou "fragmento de indução de apoptose", Ref
Interações
Foi demonstrado que Fas interage com:
Notas e referências
- (em) Baohua Huang, Matthias Eberstadt, Edward T. Olejniczak, Robert P. Meadows e Stephen W. Fesik , " NMR structure and mutagenesis of the Fas (APO-1 / CD95) death domain " , Nature , vol. 384, n o 6610, 19 a 26 de dezembro de 1996, p. 638-641 ( PMID 008967952 , DOI 10.1038 / 384638a0 , Bibcode 1996Natur.384..638H , ler online )
- Os valores para a massa e o número de resíduos indicados aqui são aqueles do precursor da proteína resultante da tradução do gene , antes das modificações pós-tradução , e podem diferir significativamente dos valores correspondentes para o proteína funcional.
- Nagata S, Golstein P "The Fas death factor" Science, 1995, 267, 1449-14562 - Griffith T, Brunner T, Fletcher S et al.
- "Apoptose induzida pelo ligando Fas como um mecanismo de privilégio imunológico" Science, 1995, 270, 1189-1192
- Rieux-Laucat F et al. "Mutations in Fas associated with human lymphoproliferative syndrome and autoimmunity" Science, 1995, 268, 1347-1349
- Nagata S, Suda T "ligante Fas e Fas: mutações lpr e gld" Immunol Today, 1995, 16, 39-43
- Ogasawara J et al. “Efeito letal do anticorpo anti-Fas em camundongos” Nature, 1993, 364, 806-809
- Gajate C, Mollinedo F, “ citoesqueleto mediada por receptor de morte e a concentração do ligando em formas de jangadas lipídicas apoptose promotoras de aglomerados na quimioterapia do cancro ”, J. Biol. Chem. , vol. 280, n o 12,Março de 2005, p. 11641–7 ( PMID 15659383 , DOI 10.1074 / jbc.M411781200 )
- Micheau O, Tschopp J, “ Indução de receptor de TNF de apoptose mediada por I por meio de dois complexos de sinalização sequenciais ”, celular , vol. 114, n o 2Julho de 2003, p. 181–90 ( PMID 12887920 , DOI 10.1016 / s0092-8674 (03) 00521-x )
- Parlato S, Giammarioli AM, Logozzi M, Lozupone F, Matarrese P, Luciani F, Falchi M, Malorni W, Fais S, “ ligação CD95 (APO-1 / Fas) ao citoesqueleto de actina através da ezrina em linfócitos T humanos: a novo mecanismo regulador da via apoptótica de CD95 ”, EMBO J. , vol. 19, n o 19,Outubro de 2000, p. 5123–34 ( PMID 11013215 , PMCID 302100 , DOI 10.1093 / emboj / 19.19.5123 )
- Ghadimi MP, Sanzenbacher R, Thiede B, Wenzel J, Jing Q, Plomann M, Borkhardt A, Kabelitz D, Janssen O, " Identificação de parceiros de interação da região de poliprolina citosólica do ligante CD95 (CD178) ", FEBS Lett. , vol. 519, n osso 1-3,Maio de 2002, p. 50–8 ( PMID 12023017 , DOI 10.1016 / s0014-5793 (02) 02709-6 )
- Wenzel J, Sanzenbacher R, Ghadimi H, Lewitzky H, Zhou Q, Kaplan DR, Kabelitz D, Feller SM, Janssen O, “ Multiple interacções da região poliprolina citosólica das CD95 ligando: sugestões para a transdução de sinal reversa capacidade de fator de morte ”, FEBS Lett. , vol. 509, n o 2dezembro de 2001, p. 255-62 ( PMID 11741599 , DOI 10.1016 / s0014-5793 (01) 03174-x )
- Hane M, Lowin B, Peitsch M, Becker K, Tschopp J, “ Interação de peptídeos derivados do ligante Fas com o domínio Fyn-SH3 ”, FEBS Lett. , vol. 373, n o 3,Outubro de 1995, p. 265–8 ( PMID 7589480 , DOI 10.1016 / 0014-5793 (95) 01051-f )
- Yu KY, Kwon B, Ni J, Zhai Y, Ebner R, Kwon BS, “ Um membro recém-identificado da superfamília do receptor do fator de necrose tumoral (TR6) suprime a apoptose mediada por LIGHT ”, J. Biol. Chem. , vol. 274, n o 20,Maio de 1999, p. 13733–6 ( PMID 10318773 , DOI 10.1074 / jbc.274.20.13733 )
- Hsu TL, Chang YC, Chen SJ, Liu YJ, Chiu AW, Chio CC, Chen L, Hsieh SL, " Modulation of dendritic cell differentiation and maturation by decoy receptor 3 ", J. Immunol. , vol. 168, n o 10,Maio de 2002, p. 4846-53 ( PMID 11994433 , DOI 10.4049 / jimmunol.168.10.4846 )
- Pitti RM, Marsters SA, Lawrence DA, Roy M, Kischkel FC, Dowd P, Huang A, Donahue CJ, Sherwood SW, Baldwin DT, Godowski PJ, Wood WI, Gurney AL, Hillan KJ, Cohen RL, Goddard AD, Botstein D, Ashkenazi A, " amplificação genômica de um receptor chamariz para ligante Fas no câncer de pulmão e cólon ", Nature , vol. 396, n o 6712dezembro de 1998, p. 699-703 ( PMID 9872321 , DOI 10.1038 / 25387 )