Epicloridrina
| (±) -Epicloridrina | |||
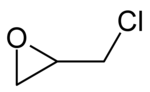
| |||
  R- enantiômero de epicloridrina (à esquerda) e S- epiclorohidrina (à direita) |
|||
| Identificação | |||
|---|---|---|---|
| Nome IUPAC | 2- (clorometil) oxirano | ||
| Sinônimos |
Cloreto de glicidil
|
||
| N o CAS | (R,S) | ||
| N o ECHA | 100.003.128 | ||
| N o EC | 203-439-8 | ||
| PubChem | |||
| SORRISOS |
ClCC1CO1 , |
||
| InChI |
InChI: InChI = 1 / C3H5ClO / c4-1-3-2-5-3 / h3H, 1-2H2 |
||
| Aparência | líquido incolor | ||
| Propriedades quimicas | |||
| Fórmula |
C 3 H 5 Cl O [Isômeros] |
||
| Massa molar | 92,524 ± 0,005 g / mol C 38,94%, H 5,45%, Cl 38,32%, O 17,29%, 92,52 g / mol |
||
| Propriedades físicas | |||
| Fusão T ° | −48 ° C | ||
| T ° fervendo | 116,56 ° C | ||
| Solubilidade | 6,59 g / 100ml (água, 25 ° C ); Miscível com álcool, éter, clorofórmio , tricloroetileno , tetracloreto de carbono ; Imiscível com hidrocarbonetos de petróleo |
||
| Parâmetro de solubilidade δ | 22,5 MPa 1/2 ( 25 ° C ) | ||
| Massa volumica | 1,18066 g · cm -3 a 20,0 ° C | ||
| Temperatura de autoignição | 415,6 ° C | ||
| Ponto de inflamação | 40,6 ° C | ||
| Pressão de vapor de saturação | 1,333 kPa a 16,6 ° C | ||
| Viscosidade dinamica | 1,03 MPa · s a 25 ° C | ||
| Precauções | |||
| SGH | |||
     H226, H301, H311, H314, H331, H350,
H226 : Líquido e vapor inflamáveis
H226, H301, H311, H314, H331, H350,
H226 : Líquido e vapor inflamáveis H301 : Tóxico por ingestão H311 : Tóxico em contato com a pele H314 : Provoca queimaduras na pele e lesões oculares graves H331 : Tóxico se inalado H350 : Pode causar câncer (indicar a rota de exposição se for conclusivamente comprovado que não outra via de exposição leva ao mesmo perigo) |
|||
| WHMIS | |||
   B3, D1A, D2A, E, |
|||
| NFPA 704 | |||
| 3 3 2 | |||
| Transporte | |||
63 : material tóxico e inflamável (ponto de inflamação 23 a 60 ° C , incluindo valores limite) Número da ONU : 2023 : EPICLORHYDRIN Classe: 6.1 Etiquetas: 6.1 : Substâncias tóxicas 3 : Líquidos inflamáveis Embalagem: Grupo de embalagem II : materiais moderadamente perigosos ;   |
|||
| Classificação IARC | |||
| Grupo 2A, cancerígeno | |||
| Inalação | TLV: 2 ppm | ||
| Pele | 7,6 mg / m3 | ||
| Ecotoxicologia | |||
| DL 50 |
90 mg · kg -1 (rato, oral ) 154 mg · kg -1 (rato, iv ) 150 mg · kg -1 (rato, sc ) 113 mg · kg -1 (rato, ip ) |
||
| LogP | 0,45 | ||
| Limiar de odor | baixo: 0,93 ppm | ||
| Unidades de SI e STP, salvo indicação em contrário. | |||
A epiclorohidrina ou epiclorohidrina e 1-cloro-2,3-epoxipropano , é um composto orgânico clorado de fórmula estrutural CH 2 CHOCH 2 Cl, líquido volátil tóxico, incolor a forte odor de alho. Um átomo de carbono da epicloridrina é quiral , então existem duas formas enantioméricas desse composto.
Apesar do nome, a epicloridrina não pertence à família da clorohidrina , pois não é um álcool halogenado, mas um epóxido . Por outro lado, certos intermediários diretos em sua síntese, como 2,3-dicloro-1-propnol e 1,3-dicloro-2-propnol, são clorohidrinas.
Produção
A epicloridrina é feita de cloreto de alila em duas etapas, primeiro, hidrocloração com ácido hipocloroso , resultando em uma mistura de clorohidrinas :
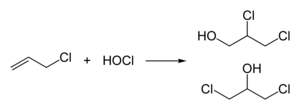
A segunda fase resulta na formação do epóxi por tratamento com uma base :

Por essa rota, mais de 800.000 toneladas (1997) de epicloridrina são produzidas anualmente.
Via do glicerol
A epicloridrina foi descrita pela primeira vez em 1848 por Marcelino Berthelot . O composto foi isolado durante estudos das reações entre o glicerol e o gás cloreto de hidrogênio .
Relembrando a experiência de Berthelot, fábricas de glicerol-epicloridrina (GTE, para glicerol em epicloridrina ) foram comercializadas. Essa tecnologia aproveita a disponibilidade de gliceróis baratos do processamento de biocombustíveis . No processo desenvolvido pela Dow Chemical , o glicerol sofre duas reações de substituição quando tratado com cloreto de hidrogênio na presença de um ácido carboxílico utilizado como catalisador . A reação forma um dos mesmos dois intermediários como no processo de cloreto de alila / ácido hipocloroso, 1,3-dicloro-2-propnol, e também é tratada com uma base para formar epicloridrina.

Outras rotas
Outras rotas envolvendo menos intermediários clorados continuam a ser exploradas. Pode ser feita menção, por exemplo, à epoxidação de cloreto de alilo .
usar
Síntese de glicerol e resinas epóxi
A epicloridrina é convertida principalmente em bisfenol-A-diglicidiléter (en) , um bloco de construção básico na fabricação de resinas epóxi . É também um precursor de monômero para outras resinas e polímeros, incluindo resinas de troca iônica , poliéterpoliol para espumas de poliuretano retardantes de chama, alquilgliceril éterulfonatos para detergentes, elastômeros ( códigos de polímero CO, ECO) e resinas especiais para processamento de papel.
Outro uso é a conversão para glicerol sintético. No entanto, o rápido aumento da produção de biodiesel , onde o glicerol é um resíduo, resultou em uma superabundância de glicerol no mercado, tornando esse processo não lucrativo. O glicerol sintético agora é usado apenas em aplicações farmacêuticas e de biotecnologia sensíveis, onde os padrões de qualidade são muito elevados.
Aplicações menores e de nicho
A epicloridrina é um precursor versátil na síntese de muitos compostos orgânicos. Por exemplo, pode ser convertido em nitrato de glicidila , um aglutinante energético usado em composições explosivas e propelentes. A epiclorohidrina reage com um nitrato alcalino, como o nitrato de sódio , produzindo nitrato de glicidila e um cloreto alcalino. É usado como solvente para celulose , resinas e tintas, e encontrou uso como fumigante contra insetos.
Polímeros feitos de epicloridrina, por exemplo resinas de poliamida-epicloridrina, são usados no reforço de papel e na indústria de alimentos para fazer saquinhos de chá , filtros de café e tripas de embutidos / embutidos sintéticos , bem como para purificação de água .
Uma importante aplicação bioquímica da epicloridrina é seu uso como agente de reticulação para a produção de resinas de cromatografia de exclusão de tamanho em Sephadex (en) a partir de dextrano .
segurança
A epicloridrina é classificada por várias agências e grupos internacionais de pesquisa em saúde como um provável ou provável carcinógeno em humanos. O consumo prolongado (oral) de níveis elevados de epicloridrina pode causar problemas estomacais e aumentar o risco de câncer. A exposição ocupacional à epicloridrina por inalação pode causar irritação nos pulmões e aumentar o risco de câncer de pulmão.
A epicloridrina é inflamável, formando produtos de decomposição perigosos em condições de incêndio. É tóxico por inalação, em contacto com a pele e por ingestão, podendo causar queimaduras. Pode causar sensibilização em contato com a pele.
Notas e referências
- ( fr ) Este artigo foi retirado parcial ou totalmente do artigo da Wikipedia em inglês intitulado " Epichlorohydrin " ( veja a lista de autores ) .
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (en) Guenter Sienel, Robert Rieth, Kenneth T. Rowbottom, epóxidos , Wiley-VCH Verlag GmbH & Co, Coll. "Ullmann's Encyclopedia of Industrial Chemistry",15 de junho de 2000( DOI 10.1002 / 14356007.a09_531 , apresentação online )
- "EPICHLOROHYDRIN" em Hazardous Substances Data Bank , acessado em 16 de julho de 2012
- (em) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 p. ( ISBN 978-0-387-69002-5 e 0-387-69002-6 , ler online ) , p. 294
- Entry "A epicloridrina" no banco de dados química GESTIS da IFA (organismo alemão responsável pela segurança e saúde ocupacional) ( alemão , Inglês ), acessada 3 de dezembro de 2010 (JavaScript obrigatório)
- "Epicloridrina" no banco de dados de produtos químicos Reptox da CSST (Organização de Quebec responsável pela segurança e saúde ocupacional), acessado em 3 de dezembro de 2010
- Universidade UCB do Colorado
- (em) " Epicloridrina " no ChemIDplus , acessado em 3 de dezembro de 2010
- "1-cloro-2,3-epoxipropano" , em ESIS , acessado em 3 de dezembro de 2010
- Enciclopédia de Química Industrial de Ullmann , Weinheim, Wiley-VCH,2005( DOI 10.1002 / 14356007.a01_425 )
- Marcellin Berthelot , “ Sobre as combinações de glicerina com ácidos e sobre a síntese dos princípios imediatos das gorduras animais ”, Ann. Chim. Phys. , vol. 41,1854, p. 216-319 ( leia online [ arquivo de2 de abril de 2015] , acessado em 2 de março de 2015 )
- Doris de Guzman, " Growing glycerine-to-ECH plants " , ICIS Green Chemicals,20 de janeiro de 2011
- Bruce M. Bell , John R. Briggs , Robert M. Campbell , Susanne M. Chambers , Phil D. Gaarenstroom , Jeffrey G. Hippler , Bruce D. Hook , Kenneth Kearns , John M. Kenney , William J. Kruper , D James Schreck , Curt N. Theriault e Charles P. Wolfe , “ Glycerin as a Renewable Feedstock for Epichlorohydrin Production. The GTE Process ”, CLEAN - Solo, Ar, Água , vol. 36, n o 8,2008, p. 657 ( DOI 10.1002 / clen.200800067 , leia online [ arquivo de18 de julho de 2012] [reimpressão do texto completo], acessado em 5 de março de 2012 )
- Jun Li, Gongda Zhao, Shuang Gao, Ying Lv, Jian Li e Zuwei Xi, " Epoxidação de cloreto de alila para epicloroidrina por um catalisador com suporte reversível com H2O2 sob condições livres de solvente ", Org. Process Res. Dev. , vol. 10, n o 5,2006, p. 876-880 ( DOI 10.1021 / op060108k )
- Ha Q. Pham e Maurice J. Marks , " Epoxy Resins ", Wiley-VCH , Weinheim,2012( ISBN 978-3527306732 , DOI 10.1002 / 14356007.a09_547.pub2 )
- " Limiares de toxicidade aguda - epicloridrina " , INERIS
- Phil Taylor , “ A glicerina sintética está de volta (mas nunca foi embora)! » , On In-Pharma Technologist ,16 de outubro de 2008(acessado em 29 de novembro de 2018 )
- Gould, RF Advanced Propellant Chemistry , ACS Chemistry Series 54, 1966
- " Laboratórios de testes de águas suburbanas: Folha de dados de epicloroidrina " [ arquivo de5 de abril de 2012] , H2otest.com (acessado em 2 de dezembro de 2011 )
- " Substâncias químicas do governo do Canadá: Oxirano, (clorometil) - (epiclorohidrina) Número de registro CAS 106-89-8 " (acessado em 7 de maio de 2013 )
- " GE Healthcare Life Sciences - Instruções para Sephadex Media " [ arquivo de18 de fevereiro de 2012] , .gelifesciences.com (acessado em 2 de dezembro de 2011 )
- " Sistema de informação de risco integrado da EPA: epicloridrina (CASRN 106-89-8) " (acessado em 7 de maio de 2013 )
- " Governo do Canadá: Avaliação de triagem para epiclorohidrina " (acessado em 7 de maio de 2013 )
- " NIOSH Pocket Guide to Chemical Hazards - Epichlorohydrin " (acessado em 20 de setembro de 2013 )
- " Informações básicas sobre epicloridrina na água potável " (acessado em 7 de maio de 2013 )
- " Governo do Canadá: Avaliação de triagem para epiclorohidrina " (acessado em 7 de maio de 2013 )
