Ácido carboxílico
O termo ácido carboxílico se refere a uma molécula que compreende um grupo carboxila (–C (O) OH). Eles são ácidos e suas bases conjugadas são chamadas de íons carboxilato .
Em química orgânica , um grupo carboxila é um grupo funcional composto de um átomo de carbono , ligado por uma ligação dupla a um átomo de oxigênio e ligado por uma ligação simples a um grupo hidroxila -OH.
Em geral
Em química , os ácidos carboxílicos R-COOH constituem com os ácidos sulfônicos R-SO 3 H os dois tipos de ácidos da química orgânica . Eles são encontrados abundantemente na natureza como ácidos graxos ( lipídios ) e são muito importantes na química industrial . Por exemplo, o ácido acético não é apenas um bloco de construção importante para as moléculas complexas encontradas na biologia , mas também uma molécula produzida industrialmente encontrada no vinagre . Um dos mais conhecidos é o ácido acetilsalicílico ou aspirina. O bloco de construção das proteínas , os aminoácidos são ácidos carboxílicos.
O grupo funcional característico é o grupo carboxila, em que R é hidrogênio ou um grupo orgânico:

Os ácidos carboxílicos têm a fórmula bruta C n H 2 N S 2 quando o R é um alquilo grupo . Calcular o número de insaturação dá: . Essa insaturação reflete a ligação dupla carbono-oxigênio .
Os grupos carboxila são freqüentemente escritos na forma reduzida: -COOH (forma não ionizada do grupo). A forma ionizada do grupo é: -COO - .
Ele está sempre localizado no final da cadeia de carbono . A adição de um grupo carboxila a um composto orgânico é uma carboxilação , a remoção desse mesmo grupo é uma descarboxilação .
Íons carboxilato
Estas são as bases conjugadas R-COO - ácidos carboxílicos. Essas bases são geralmente bastante fracas . A carga negativa na molécula é deslocalizada nos dois átomos de oxigênio do grupo carboxila por mesomerismo, o que explica a estabilidade relativa desse tipo de molécula.

O íon carboxilato é um surfactante anfifílico , é a espécie detergente do sabão . Na verdade, o grupo _COO-carboxilato é hidrofílico porque é muito polar . Por outro lado, a cadeia de carbono R é apolar e, portanto, hidrofóbica e lipofílica .
Nomenclatura
- Sistemático: se o átomo de carbono do grupo carboxila COOH estiver incluído na cadeia principal do hidrocarboneto correspondente (tendo o mesmo número de átomos de carbono, com CH 3 em vez de COOH), segue-se o nome deste. Hidrocarboneto com o sufixo " -oico "(dióico para um diácido), e precedendo-o com a palavra" ácido ". Caso contrário (em séries cíclicas, por exemplo), a palavra “ ácido ” é seguida pelo nome do hidrocarboneto ao qual o sufixo “-carboxílico” é adicionado.
| Aula | Fórmula * do grupo de características |
Sufixo |
|---|---|---|
| Ácidos carboxílicos | - (C) OOH -COOH |
ácido- ... ácido óico ... -carboxílico |
- ácido heptanóico CH 3 (CH 2 ) 5 -COOH pode ser alternativamente denominada hexano-1-carboxílico, se o átomo de carbono de COOH não está incluída na numeração de cadeia;
- O ácido HOOC- (CH 2 ) 5 -COOH heptanodioico é um ácido dicarboxílico . O sufixo -oic é precedido pelo prefixo multiplicativo di- ;
- ácido ciclopentanocarboxílico: -COOH .
- Comum: como muitos compostos orgânicos, os ácidos carboxílicos têm nomes comuns freqüentemente usados na literatura e que lembram a fonte de onde foram isolados pela primeira vez. No entanto, uma lista definida pela IUPAC regula o uso de nomes triviais aceitos junto com nomes sistemáticos.
| Modelo | Estrutura | Nome IUPAC | nome comum | Fonte |
|---|---|---|---|---|
| Monoácidos alifáticos | H-COOH | ácido metanóico | ácido fórmico | secretado por algumas formigas (latim: fórmica , formigas) |
| CH 3 -COOH | ácido etanóico | ácido acético | Latim: acetum , vinagre | |
| CH 3 CH 2 -COOH | ácido propanóico | ácido propiónico | Grego: peão , gordo | |
| CH 3 (CH 2 ) 2 -COOH | ácido butanóico | ácido butírico | Grego: bouturos , manteiga | |
| CH 3 (CH 2 ) 3 -COOH | ácido pentanóico | ácido valérico | valeriana | |
| CH 3 (CH 2 ) 4 -COOH | ácido hexanóico | ácido capróico | ||
| CH 3 (CH 2 ) 5 -COOH | ácido heptanoico | ácido enântico | ||
| CH 3 (CH 2 ) 6 -COOH | ácido octanóico | ácido caprílico | coco , leite materno | |
| CH 3 (CH 2 ) 7 -COOH | ácido nonanoico | ácido pelargônico | ||
| CH 3 (CH 2 ) 8 -COOH | ácido decanóico | ácido cáprico | ||
| CH 3 (CH 2 ) 9 -COOH | ácido undecanóico | ácido undecílico | ||
| CH 3 (CH 2 ) 10 -COOH | ácido dodecanoico | ácido Laurico | óleo de côco | |
| CH 3 (CH 2 ) 11 -COOH | ácido tridecanóico | ácido tridecílico | ||
| CH 3 (CH 2 ) 12 -COOH | ácido tetradecanóico | ácido mirístico | noz-moscada | |
| CH 3 (CH 2 ) 13 -COOH | ácido pentadecanóico | ácido pentadecílico | ||
| CH 3 (CH 2 ) 14 -COOH | ácido hexadecanóico | Ácido palmítico | azeite de dendê | |
| CH 3 (CH 2 ) 15 -COOH | ácido heptadecanóico | ácido margarico | ||
| CH 3 (CH 2 ) 16 -COOH | ácido octodecanoico | ácido esteárico | gorduras animais | |
| CH 3 (CH 2 ) 17 -COOH | ácido não adecanóico | ácido não adecílico | ||
| CH 3 (CH 2 ) 18 -COOH | ácido eicosanóico | ácido araquídico | óleo de amendoim , óleos de peixe e óleos vegetais | |
| CH 3 (CH 2 ) 20 -COOH | ácido docosanóico | ácido beénico | ||
| Monoácidos aromáticos | C 6 H 5 -COOH | ácido benzóico | benzeno | |
| HO-C 6 H 4 -COOH | Ácido 2-hidroxibenzoico | ácido salicílico | fruta (como salicilato de metila ) | |
| Ácidos tiol | CH 3 CH (SH) -COOH | Ácido 2-mercaptopropanóico | ácido tiolático |
NB: um dispositivo mnemônico para lembrar os nomes dos ácidos lineares, em ordem crescente do número de átomos de carbono, é a seguinte frase: " O n M anjo S aucisse G rillée A P ungido" ( O xalique, M alonique, S uccinic , G lutaric, A dipic, P imelic). Os diácidos são usados para a síntese de poliamidas e poliésteres .
Outros tipos de ácidos carboxílicos podem ser mencionados: ácidos dicarboxílicos , os ácidos tricarboxílicos , os ácidos alfa- hidroxilados , os cetoácidos , os aminoácidos e os ácidos graxos .
Propriedades físicas e estruturais
Estado
Os ácidos carboxílicos são líquidos em condições normais, desde que sua cadeia de carbono tenha menos de oito átomos de carbono. Eles são sólidos além disso.
Os ácidos de baixo peso molecular têm um odor forte; por exemplo, o ácido butanóico é responsável pelo cheiro de manteiga rançosa.
Polaridade, solubilidade
A função do ácido carboxílico é altamente polar e ao mesmo tempo doadora e aceitadora de ligações de hidrogênio . Isso permite a criação de ligações de hidrogênio, por exemplo, com um solvente polar, como água, álcool e outros ácidos carboxílicos.

Devido a essa propriedade, pequenos ácidos carboxílicos (até o ácido butanóico) são completamente solúveis em água. As moléculas de ácido também são capazes de formar dímeros estáveis por ligações de hidrogênio, o que explica por que seu ponto de ebulição é superior ao dos álcoois correspondentes.
Acidez
Em solução em água, o ácido se dissocia parcialmente no íon carboxilato, de acordo com a equação de equilíbrio :
Estes são ácidos fracos na água ( p K A entre 4 e 5).
Como os álcoois, os ácidos carboxílicos apresentam um caráter ácido e básico: a desprotonação em íons carboxilato é fácil, mas a protonação é mais difícil. Portanto, eles têm um p K A mais baixo do que os álcoois. Na verdade, a acidez dos ácidos carboxílicos é explicada pelo efeito indutivo no grupo carboxila: a ligação C = O é muito polarizada ( eletronegatividade do oxigênio maior que a do carbono) o que torna o carbono eletrofílico , e portanto atrai elétrons do outro oxigênio. Agora, esse outro oxigênio está ligado a um hidrogênio, e essa ligação também é polarizada , de modo que o elétron do hidrogênio que se aproximou do oxigênio é, por sua vez, atraído pelo carbono eletrofílico. Este hidrogênio, portanto, torna-se facilmente móvel, daí a acidez do grupo carboxila.
A solubilidade do ácido carboxílico aumenta com o pH .
Espectroscopia
No infravermelho (IR), o ácido carboxílico tem duas bandas de valência:
| Vibração | C = O | OH |
|---|---|---|
| Número da onda (cm −1 ) | 1.680-1.710 | 2.500-3.200 |
| Intensidade | (Forte) | grande, médio a forte |
Estrutura

De acordo com a teoria VSEPR :
- a geometria em torno do átomo de carbono (ligações) é do tipo trigonal;
- a geometria em torno do átomo de oxigênio da função carbonila (ligação dupla + dupletos livres) também é do tipo trigonal;
- a geometria em torno do átomo de oxigênio da função hidroxila (ligações + dupletos livres) é do tipo tetraédrico (AX 2 E 2 ).
O ácido carboxílico tem várias formas mesoméricas .
Reatividade
Conforme mostrado, entre outros, as diferentes fórmulas mesoméricas de ácido carboxílico:
- os átomos de oxigênio são locais nucleofílicos, bem como bases de Lewis;
- o carbono central é eletrofílico;
- o átomo de hidrogênio eletrofílico é ácido.
Derivados
Os ácidos carboxílicos têm muitos derivados:
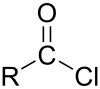
-
Anidrido ácido
- os ésteres
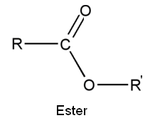
- as amidas

- o nitrilo
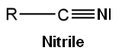
Em termos de grupo de saída (nucleofuge), a ordem de facilidade é:
Cl - (cloreto de acilo), RCOO - (anidrido), RO - (éster), - NH 2, e - NR 1 R 2 (amidas).
Redução
Oxidação
- Dióxido de carbono (CO 2)
Síntese
Síntese por oxidação
álcoois ou aldeídos Os ácidos carboxílicos podem ser obtidos por oxidação de aldeídos , portanto, de fato, por oxidação dupla de álcoois primários .de alcenos exemplo: síntese de ácido acético por oxidação de propeno
Síntese de um derivado de ácido
É simplesmente a hidrólise de vários derivados de ácido.
éster- hidrólise em meio ácido: retroesterificação
- hidrólise em meio básico: saponificação do éster
Síntese por reação de um reagente de Grignard em dióxido de carbono
ReaçãoA síntese ocorre em baixa temperatura ( −40 ° C ). O dióxido de carbono está então na forma sólida, chamada de gelo seco . É colocado em excesso. Após a reação, a hidrólise é realizada em meio ácido para obter o ácido carboxílico.
MecanismoPrimeira etapa : adição do reagente de Grignard ao CO 2

Segunda etapa : hidrólise em meio ácido
Síntese malônica
A síntese malônica é um conjunto de reações que permite a síntese de muitos ácidos carboxílicos primários ou secundários a partir do malonato dietílico .
Ela está composta:
- uma reação ácido-base entre malonato dietílico e etanoato ( sódio , potássio, etc. );
- uma substituição nucleofílica , onde o grupo desejado (primário ou secundário) é inserido para o ácido carboxílico final;
- uma saponificação dupla das duas funções éster do malonato dietílico substituído, seguida por acidificação do meio;
- descarboxilação (liberação de dióxido de carbono no aquecimento);
- rearranjo do produto final em ácido carboxílico por tautomerismo .
Esta síntese é tanto mais interessante quanto a priori , torna-se possível sintetizar qualquer ácido carboxílico, uma vez que, para além de um grupo terciário, parece que podemos colocar o que queremos no lugar de R .
Notas e referências
- R. Panico e J.-C. Richer, IUPAC nomenclature of organic compostos , Masson, 1994, p. 70, 118- ( ISBN 978-2-225-84479-9 ) . Uma matriz de sufixos (e prefixos) usada para descrever alguns grupos de características importantes na nomenclatura substitutiva está disponível em uma referência IUPAC online (em inglês): sufixos e prefixos para as características principais Alguns grupos na nomenclatura substitutiva .
- Robert Panico, Jean-Claude Richer e Jean Rigaudy , Nomenclatura e terminologia em química orgânica - Aulas funcionais. Stereochemistry , Engineering Techniques , 1996, p. 20 ( ISBN 2 85 059-001-0 ) .
- http://www.acdlabs.com/iupac/nomenclature/93/r93_705.htm











