Dióxido de carbono
| Dióxido de carbono | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
  Estrutura do dióxido de carbono. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificação | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome IUPAC | Dióxido de carbono | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinônimos |
Dióxido de carbono, dióxido de carbono |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.004.271 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 204-696-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Código ATC | V03 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 280 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ChEBI | 16526 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o E | E290 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISOS |
C (= O) = O , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1S / CO2 / c2-1-3 InChIKey: CURLTUGMZLYLDI-UHFFFAOYSA-N |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | Gás comprimido liquefeito, incolor e inodoro | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades quimicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula |
C O 2 [Isômeros] |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molar | 44,0095 ± 0,0014 g / mol C 27,29%, O 72,71%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fusão T ° | −78,48 ° C (sublimação a 760 mmHg ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fervendo | -56,6 ° C ( 5,12 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidade | em água a 20 ° C : 88 ml / 100 ml sob 1 bar de CO 2, ou seja , 1,69 g / kg de água (3,35 g a 0 ° C , 0,973 g a 40 ° C e 0,576 g a 60 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
1,87 kg m- 3 ( gás a 15 ° C 1,013 bar ) mais denso que o ar equação:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressão de vapor de saturação |
5.720 kPa ( 20 ° C ) 569,1 mmHg ( -82 ° C ); equação:

|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viscosidade dinamica | 0,07 mPa s a -78 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto crítico | 31,3 ° C ; 72,9 atm e 0,464 g cm −3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto Triplo | -56,6 ° C a 5,11 atm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Condutividade térmica | 3,840 × 10 −5 cal cm −1 s −1 K −1 a 20 ° C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Velocidade do som | 259 m s −1 ( 0 ° C , 1 atm ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gás | −393,52 kJ mol −1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
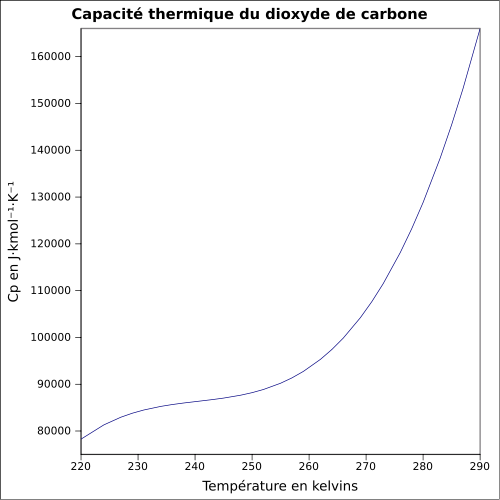
| C p |
equação:
equação:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades eletrônicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 energia de re ionização | 13,773 ± 0,002 eV (gás) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cristalografia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classe de cristal ou grupo espacial | P42 / mnm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parâmetros de malha |
a = 3,535 Å b = 3,535 Å |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Volume | 51,73 Å 3 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades ópticas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Índice de refração | 1.00045 (1 atm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauções | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 Aviso H280 , P403 e P410 H280 : Contém gás sob pressão; pode explodir se aquecido P403 : Armazenar em local bem ventilado. P410 : Proteger da luz solar. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 PARA, A : Temperatura crítica do gás comprimido = 31,1 ° C Divulgação a 1,0% de acordo com a lista de divulgação de ingredientes |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transporte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
20 : gás asfixiante ou gás que não apresenta risco subsidiário Número ONU : 1013 : DIÓXIDO DE CARBONO Classe: 2.2 Código de classificação: 2A : Gás liquefeito, asfixiante; Etiqueta: 2.2 : Gases não inflamáveis e não tóxicos (corresponde aos grupos designados por A ou O maiúsculo); 
22 : gás liquefeito refrigerado, asfixiante Número ONU : 2187 : DIÓXIDO DE CARBONO LÍQUIDO REFRIGERADO Classe: 2.2 Código de classificação: 3A : Gás liquefeito refrigerado, asfixiante; Etiqueta: 2.2 : Gases não inflamáveis e não tóxicos (corresponde aos grupos designados por A ou O maiúsculo); 
- Número ONU : 1845 : DIÓXIDO DE CARBONO, SÓLIDO; ou NEVE DE CARBONO Classe: 9 Código de classificação: M11 : Outras substâncias que representam um risco durante o transporte, mas que não correspondem à definição de nenhuma outra classe. Tag: 9 : Substâncias e artigos perigosos diversos  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI e STP, salvo indicação em contrário. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
O dióxido de carbono , também conhecido como dióxido de carbono ou dióxido de carbono é um composto inorgânico cuja fórmula química é CO 2, A molécula que tem uma estrutura linear da forma S = C = O . Apresenta-se, nas condições padrão de temperatura e pressão , como um gás incolor, inodoro, o espiga.
CO 2é utilizado pelo anabolismo das plantas para produzir biomassa por meio da fotossíntese , processo que consiste na redução do dióxido de carbono pela água , graças à energia luminosa recebida do Sol e captada pela clorofila , pela liberação de oxigênio para a produção de monossacarídeos , e primeiro da glicose pelo ciclo de Calvin . CO 2é liberado, através do ciclo de Krebs , pelo catabolismo de plantas , animais , fungos (fungos ou fungos ) e microrganismos . Esse catabolismo consiste principalmente em oxidar os lipídios e carboidratos da água e do dióxido de carbono com o oxigênio do ar para gerar energia e poder redutor, respectivamente na forma de ATP e NADH + H + . CO 2é, portanto, uma parte fundamental do ciclo do carbono em nosso planeta. Também é produzido pela queima de combustíveis fósseis como carvão , gás natural e petróleo , bem como de toda matéria orgânica em geral. É um indesejado subproduto em processos industriais em larga escala.
Quantidades significativas de CO 2também são rejeitados por vulcões e outros fenômenos geotérmicos , como gêiseres .
Em janeiro de 2021, a atmosfera da Terra continha 415,13 ppmv (partes por milhão em volume) de CO 2, ou 0,04153%. Esse nível era de 283,4 ppmv em 1839, de acordo com amostras de gelo retiradas da Antártica , um aumento geral de cerca de 46% em 182 anos.
CO 2é um importante gás de efeito estufa , transparente na luz visível, mas absorvente na faixa do infravermelho , de modo que tende a bloquear a reemissão para o espaço da energia térmica recebida no solo sob o efeito da radiação solar . É responsável por cerca de 26% do efeito estufa em ação na atmosfera terrestre ( o vapor de água fornece 60%); aumentando sua concentração é em parte responsável pelo aquecimento observado em todo o planeta ao longo dos últimos décadas do XX ° século. Além disso, a acidificação resultante da dissolução de dióxido de carbono atmosférico pode pôr em risco a sobrevivência de muitos organismos marinhos antes do final do XXI th século.
Características físico-químicas
À pressão atmosférica, ele sublima a -78,5 ° C (mudança do estado sólido para gasoso), mas não derrete (mudança do estado sólido para líquido).
A fase líquida só pode existir a uma pressão mínima de 519 kPa ( ou seja, 5,12 atm ) e em uma faixa de temperatura de -56,6 ° C ( ponto triplo ) a um máximo de 31,1 ° C a 7,38 MPa ( ou seja, 72,8 atm ) ( crítico ponto ).
Pressão de vapor de saturação
|
| Transição | Temperatura | Calor latente |
|---|---|---|
| Vaporização | 0 ° C | 234,5 kJ kg −1 |
| Vaporização | -16,7 ° C | 276,8 kJ kg −1 |
| Vaporização | -28,9 ° C | 301,7 kJ kg −1 |
| Fusão | -56,6 ° C | 199 kJ kg −1 |
Haveria pelo menos cinco fases moleculares sólidas (existindo em pressão "baixa", menos de 30 a 60 GPa) e três fases de polímero sólido (em pressões mais altas) de CO 2. :
- fases moleculares:
- I: “gelo seco”, até 800 K e 11-12 GPa
- II: entre 400 e 5-600 K e uma pressão de 12 a cerca de 50 GPa
- III: além de 12 GPA e menos de 500 K
- IV: além de 11 GPa e mais de 500 K
- VII: de 600 a 900 K (até 1000 K incluindo a parte supercrítica) e 11 a 20 GPa
- fases poliméricas:
- V: mais de 30 GPa e mais de cerca de 1.300 K
- VI: temperatura entre aproximadamente 500 K e 1300 K e pressão maior que 30 (a 1300 K) a 50 GPa (a 500 K)
- amorfo, inferior a 500 K e superior a 50 GPa
Solubilidade aquosa
CO 2dissolve-se em água e forma ácido carbônico H 2 CO 3 : CO 2 (aq)+ H 2 O (l) H 2 CO 3 (aq), com K h = [H 2 CO 3] / [CO 2] ≈ 1,70 x 10 -3 a 25 ° C .
Também é lipossolúvel (solúvel em substâncias gordurosas).
O ácido carbônico é apenas moderadamente estável e facilmente se decompõe em H 2 Oe CO 2. Por outro lado, quando o dióxido de carbono se dissolve em uma solução aquosa básica (soda, potássio, etc.), a base desprotona o ácido carbônico para formar um íon de hidrogenocarbonato HCO-
3, também chamado de íon bicarbonato , então um íon carbonato CO2-
3. Desta forma, a solubilidade do CO 2é consideravelmente aumentado. O carbonato de potássio K 2 CO 3por exemplo, tem uma solubilidade de 1,12 kg / L de água a 20 ° C .
É assim que o calcário se dissolve na água, na faixa de pH em que o hidrogenocarbonato ácido é estável, produzindo uma solução de hidrogenocarbonato (s) (de cálcio e magnésio ...). Portanto, é provável que precipite quando o CO 2dissolvido é desgaseificado, como na formação de estalagmites e estalactites . Calcário, portanto, na presença de CO 2, uma solubilidade que diminui com o aumento da temperatura, como gases e ao contrário da maioria dos sólidos (cuja solubilidade geralmente aumenta com a temperatura).
Sob certas condições (alta pressão + baixa temperatura) CO 2podem ficar presos nas chamadas gaiolas de água de clatrato . É um dos possíveis meios de separação industrial de CO 2contido em um gás de pré ou pós-combustão . É também um dos meios planejados de sequestro de CO 2armazenamento industrial ou geológica estudado, possivelmente correlacionada com a dessalinização de água do mar (teoricamente ele mesmo pode ser substituído por metano hidrato de metano ).
História do conhecimento
O dióxido de carbono é um dos primeiros gases (junto com o vapor d'água ) a ser descrito como uma substância distinta do ar. No XVII th século , o químico e médico Flandres Janeiro Batista van Helmont observado que a queima de carvão num recipiente fechado, a massa da cinza resultante é menor do que o do carvão. Sua interpretação foi que a massa perdida havia se transmutado em uma substância invisível que ele chamou de " gás " ou spiritus sylvestre ("espírito selvagem").
As propriedades do dióxido de carbono foram estudadas em maiores detalhes na década de 1750 pelo químico e físico escocês Joseph Black . Descobriu que, aquecendo ou despejando ácido sobre o calcário (rocha composta de carbonato de cálcio ), o resultado era a emissão de um gás, que chamou de "ar fixo", minando a teoria do flogisto, ainda ensinada na época. Ele observou que é mais denso que o ar e que não pode suportar uma chama, nem a vida de um animal. Black também descobriu que, quando o dióxido de carbono é introduzido em uma solução de calcário ( hidróxido de cálcio ), ocorre um precipitado de carbonato de cálcio. Ele usou esse fenômeno para ilustrar que o dióxido de carbono é produzido pela respiração animal e fermentação microbiana.
Em 1772 , o químico inglês Joseph Priestley publicou um trabalho intitulado Impregnating Water with Fixed Air no qual descreveu um processo de despejar ácido sulfúrico (ou "óleo de vitríolo" como era chamado na época) sobre giz. Para produzir carbono dióxido de carbono, forçando então o gás a se dissolver em uma tigela de água. Ele tinha acabado de "inventar" a água com gás . O processo foi então assumido por Johann Jacob Schweppe que fundou, em 1790 , em Londres, uma fábrica de produção de refrigerantes conhecida como Schweppes .
Em 1781 , o químico francês Antoine Lavoisier destacou o fato desse gás ser produto da combustão do carbono com o oxigênio .
O dióxido de carbono foi liquefeito em 1823 por Humphry Davy e Michael Faraday . A primeira descrição do dióxido de carbono na fase sólida foi escrita por Charles Thilorier (fr) , que em 1834 abriu um recipiente pressurizado de gás dióxido de carbono liquefeito e constatou que o resfriamento produzido pela rápida evaporação do líquido gerado na "neve "CO 2.
Usos
O dióxido de carbono é comercializado em diferentes formas para uma variedade de usos, em um mercado dominado por grandes empresas como a Messer , Air Liquide e Air Products . Para a indústria de alimentos, o padrão de referência na Europa é publicado pela European Industrial Gases Association (de ). Na França, representa 70% do consumo.
A Agência Internacional de Energia publicou um relatório sobre o uso de CO 2 em setembro de 2019, que ele estima em 230 Mt / ano , incluindo 130 Mt / ano para a fabricação de fertilizantes e 80 Mt / ano para a recuperação aprimorada de petróleo e gás natural. O objetivo deste relatório é avaliar seu potencial de contribuição para a compensação de emissões de CO 2 .. Ele conclui que esse potencial é baixo no curto prazo, e permanecerá no longo prazo muito menor do que o da captura e sequestro de dióxido de carbono ; os caminhos mais promissores são os usos em materiais de construção, na fabricação de polímeros e em estufas.
Na forma gasosa
CO 2 tem muitos usos, incluindo:
- extinção de incêndios : muitos centros de dados (salas de servidores de computadores) ou salas de arquivos estão equipados com um sistema que, em caso de incêndio, enche a sala com CO 2 que tem o efeito de extinguir o fogo;
- componente espumante em bebidas gaseificadas ;
- em aquários e cultivo em estufas para melhor crescimento das plantas;
- em embalagens de atmosfera controlada como elemento neutralizante;
- na distribuição de água potável, associada ao carbonato, para elevar a dureza (TH) da água excessivamente agressiva;
- solubilização de calcário em água dura (TH maior que 25 ° F );
- bombas de cerveja: por estar em contato com a superfície da cerveja, evita sua oxidação e prolonga sua conservação, ao contrário de um compressor que utiliza ar (ambiente);
- CO 2 também é usado às vezesem grandes matadouros de porcos, a fim de entorpecê-los antes de sangrá-los; era usado para conservar carne ;
- componente necessário para o fenômeno da fotossíntese que permite que as plantas cresçam transformando matéria inorgânica em matéria orgânica constituindo assim sua madeira;
- fluido de transferência de calor em certos tipos de reatores nucleares, como os do setor UNGG na França;
- é utilizado por sua difusibilidade (capacidade de difusão) para a criação do pneumoperitônio durante as laparoscopias .
Em forma liquida
Na forma líquida, é usado como:
- refrigerante para congelar certos alimentos;
- refrigerante na indústria eletrônica;
- agente extintor nos chamados extintores de "dióxido de carbono", às vezes falamos de neve de dióxido de carbono porque parte do CO 2 o líquido solidifica imediatamente ao sair do extintor, produzindo um pó branco misturado com gás dióxido de carbono;
- propelente (e às vezes também gaseificado) para bebidas servidas na torneira.
Quando usado como refrigerante , o CO 2possui o nome da nomenclatura industrial "R744". Seu uso como refrigerante tende a se tornar mais democrático nos últimos anos: é considerado um “refrigerante natural” e seu potencial de aquecimento global é muito baixo em comparação com os refrigerantes “tradicionais”.
À pressão atmosférica, o dióxido de carbono nunca está na forma líquida. Vai diretamente da forma sólida para a forma gasosa ( sublimação ).
Em forma sólida
O dióxido de carbono na forma sólida tem muitos nomes: "gelo seco", "gelo seco", "gelo seco", "gelo seco". Vem da solidificação do CO 2líquido. Obtém-se gelo seco que é então comprimido para se obter gelo seco.
Em sua fase sólida, este gelo seco sublima sem deixar resíduo, com uma entalpia de sublimação de 573 kJ kg −1 (ou 25,2 kJ mol −1 ), a −78,5 ° C e a 1 atm . Portanto, rapidamente foram encontrados vários usos como refrigerante.
É comercializado em diferentes apresentações dependendo de seu uso:
- em grânulos (do tamanho de um grão de arroz com 3 mm de diâmetro): principalmente para limpeza e decapagem criogênica ;
- em palitos (cerca de 16 mm de comprimento ):
- para a conservação e transporte de produtos sob temperatura controlada (produtos farmacêuticos, transporte de alimentos congelados, transporte de amostras, etc.),
- em eventos: o gelo seco na água forma uma névoa muito densa que desliza ao longo das paredes do recipiente;
- para pesquisa básica ou aplicada, por exemplo:
- em química, como um refrigerante misturado com um solvente orgânico (na maioria das vezes acetona ) para conduzir melhor o calor, mais raramente como um reagente. Neste campo, utilizamos o termo “Carboglace” na França, ou apenas “carbo” na língua falada, e nunca o termo “gelo seco” que, por outro lado, é preferido em Quebec;
- para vinificação : retarda a fermentação e evita a oxidação ;
- em bolhas ou blocos:
- para fornecimento de ar ( catering ), fornecedores, agentes funerários, etc. ;
- em pães:
- para fazer neblina espessa (efeitos especiais, cinema, vídeo).
O dióxido de carbono sólido também está presente na forma de neve de dióxido de carbono nos pólos do planeta Marte , onde cobre as calotas polares (compostas principalmente de água) e suas periferias durante o inverno local , bem como na forma de dióxido de carbono gelo. em latitude mais baixa, tarde da noite nas primeiras fontes locais (fotografias tiradas por sondas Viking , o rover Sojourner , a sondas Phoenix e várias imagens HRSC ). Depósitos importantes são sequestrados geologicamente no pólo sul.
Em fase supercrítica
Além de seu ponto crítico, o dióxido de carbono entra em uma fase chamada supercrítica . A curva de equilíbrio líquido-gás é interrompida no ponto crítico, garantindo à fase supercrítica um continuum de propriedades físico-químicas sem mudança de fase. É uma fase tão densa quanto um líquido, mas que garante propriedades de transporte (viscosidade, difusão) próximas às de um gás. O dióxido de carbono supercrítico é usado como solvente verde, estando os extratos livres de vestígios de solvente.
Neste formulário, ele funciona como:
- extração de agente :
- descafeinação do café ,
- eliminação de 2,4,6-tricloroanisol (TCA) de rolhas tratadas com cloro (ou hipoclorito) para evitar dar um sabor a rolha ao vinho após o engarrafamento,
- extração de compostos químicos ou biológicos,
- purificação de compostos químicos (fase móvel em cromatografia , em particular em SFC );
- agente de transporte e armazenamento no sequestro geológico de dióxido de carbono (em raras aplicações industriais);
- agente de resfriamento para permitir a micronização de ingredientes ativos .
Subproduto de processos industriais
É um subproduto de processos industriais em grande escala. Um exemplo é a produção de ácido acrílico, que chega a ultrapassar cinco milhões de toneladas por ano. O desafio no desenvolvimento desses processos é encontrar um catalisador adequado e condições de processo que maximizem a formação do produto e minimizem a produção de CO 2 ..
Reatividade
O dióxido de carbono é uma molécula muito estável, com uma entalpia de formação padrão de −393,52 kJ mol −1 . O carbono tem uma carga parcial positiva, o que torna a molécula fracamente eletrofílica . Por exemplo, um carbanião será capaz de realizar uma adição nucleofílica em CO 2e formar um ácido carboxílico após hidrólise. Além disso, CO 2pode ser usado para formar carbonatos orgânicos , por adição a epóxis .
Finalmente, CO 2pode ser reduzido, por exemplo, a monóxido de carbono por eletroquímica com um potencial redox de -0,53 V em comparação com o eletrodo de hidrogênio padrão ou por hidrogenação .
Toxicidade
O ar externo contém cerca de 0,04% de CO 2 em 2019 (412 ppm em janeiro de 2019).
A partir de uma certa concentração no ar, este gás é perigoso ou mesmo fatal devido ao risco de asfixia ou acidose , embora o CO 2não é quimicamente tóxico. O valor do limite de exposição é de 3% em um período de quinze minutos. Este valor nunca deve ser excedido. Além disso, os efeitos para a saúde são tanto mais graves quanto o teor de CO 2aumentou. Assim, a 2% de CO 2no ar, a amplitude respiratória aumenta. A 4% (ou 100 vezes a concentração atual na atmosfera), a frequência respiratória acelera. A 10%, podem aparecer distúrbios visuais, tremores e sudorese. Aos 15%, é a perda repentina de consciência . Com 25%, a parada respiratória resulta em morte.
A inalação de dióxido de carbono concentrado causa bloqueio da ventilação, algumas vezes descrito como uma sensação violenta de estrangulamento, falta de ar, dificuldade respiratória ou aperto no peito , que pode levar rapidamente à morte se a exposição for prolongada.
De acordo com a ANSES, estudos relatam “concentrações associadas aos efeitos intrínsecos do CO 2 na saúde(limiar em cerca de 10.000 ppm correspondendo ao aparecimento de acidose respiratória (queda no pH do sangue), o primeiro efeito crítico do CO 2) ” . A acidose respiratória pode ocorrer tão baixo quanto 1% (10.000 ppm ) de CO 2no ar, se respirado por trinta minutos ou mais por um adulto saudável com uma carga física moderada e, possivelmente, mais cedo em indivíduos vulneráveis ou sensíveis. Essas taxas “são superiores aos valores-limite regulatórios e / ou normativos para a qualidade da renovação do ar na França e internacionalmente, que geralmente variam entre 1.000 e 1.500 ppm de CO 2. " Um pequeno estudo experimental (envolvendo 22 adultos) concluiu que o CO 2 teve um efeitona psicomotricidade e função intelectual (tomada de decisão, resolução de problemas) a partir de 1000 ppm (estudo de Satish et al. , 2012), mas este estudo deve ser confirmado por estudos com maior poder estatístico. ANSES observa que, em última análise, existem poucos estudos epidemiológicos sobre este gás comum, incluindo possíveis efeitos CMR (carcinogênicos, mutagênicos e reprotóxicos).
Sendo o dióxido de carbono um gás incolor e pesado que se acumula nas folhas, é difícil de ser detectado por uma pessoa inexperiente.
No ar interno
Os humanos estão passando cada vez mais tempo em uma atmosfera confinada (cerca de 80-90% do tempo em um prédio ou veículo). De acordo com a ANSES e vários atores na França, a taxa de CO 2no ar interno de edifícios (vinculado à ocupação humana ou animal e à presença de usinas de combustão ), ponderado pela renovação do ar, é “normalmente entre 350 e 2.500 ppm aproximadamente” .
Em residências, escolas, creches e escritórios, não existe uma relação sistemática entre os níveis de CO 2e outros poluentes, e CO 2interior não é estatisticamente um bom indicador de poluentes associados ao tráfego rodoviário (ou aéreo ...) exterior. CO 2é o parâmetro que muda mais rapidamente (com a higrometria e a taxa de oxigênio quando humanos ou animais estão reunidos em uma sala fechada ou mal ventilada. Em países pobres, muitas lareiras abertas são fontes de CO 2e CO emitido diretamente no local da vida. Ou fique o dia todo no ar com uma taxa de CO 2alcançar ou exceder 600 ppm degrada nossas habilidades cognitivas (pensar, raciocinar, lembrar, decidir). Pequenas mudanças nos níveis de CO 2 , de acordo com um estudo publicado na Environmental Health Perspectivesno ar afetam fortemente nosso pensamento complexo e habilidades de tomada de decisão. Este nível de 600 ppm é frequentemente alcançado no ar interior, onde frequentemente excede 1000 ppm , várias vezes ao dia com, por exemplo, um teor médio de 3110 mg / m 3 de CO 2nas salas de aula estudadas; em detrimento das capacidades de aprendizagem das crianças).
Um caso especial é o de pavilhões esportivos onde o esforço físico implica uma necessidade adicional de oxigênio e um aumento de CO 2.expirado por jogadores (e espectadores). Por exemplo, durante jogos de hóquei no gelo , CO 2aumenta de 92 para 262 ppm durante um jogo (principalmente jogado por homens adultos). No centro da pista de gelo, o nível de CO 2excede 1000 ppm em cada partida (limite máximo recomendado pelo Instituto Norueguês de Saúde Pública). As medições in situ mostram que um jogador respira ar mais enriquecido em CO 2que os espectadores, e que o CO 2desce durante os tempos de descanso e sobe durante o tempo de jogo. Na noite seguinte a um jogo, em uma sala de hóquei fechada, leva quase uma dúzia de horas para recuperar o nível de CO 2baixo (600-700 ppm ), que ainda está acima do normal. Além disso, em países frios, temperados ou quentes, muitos pavilhões desportivos têm ar condicionado; por razões de economia de energia, eles não têm uma renovação constante ou suficiente do ar externo. Durante um jogo de hóquei no gelo, mulheres e crianças emitem menos CO 2do que os homens, mas na mesma sala, o grau de aumento do nível de CO 2no ar do ginásio é comparável, e em todos os casos estudados o intervalo entre duas partidas não reduz a concentração de CO 2o suficiente para que o início do segundo período seja tão fraco quanto o início do primeiro. Quando o número de espectadores aumenta, o nível de CO 2na sala aumenta ainda mais. O número de aberturas / fechamentos de portas que dão para o exterior também influencia a renovação do ar e, portanto, a taxa de CO 2 .na Academia. Estudos têm mostrado uma diminuição no desempenho cognitivo e na tomada de decisão ou aprendizagem quando o CO 2aumentou. Poucos estudos enfocaram o efeito deste mesmo CO 2 sobre o desempenho esportivo de um indivíduo ou de sua equipe.
Nas acomodaçõesNão é regulamentado no ar doméstico; mas deve ser medido como um “indicador de confinamento e da qualidade de renovação do ar” em certos locais confinados, com base em padrões que a ANSES considera não ter fundamento sanitário.
Em edifícios não residenciaisNa França, as regulamentações departamentais de saúde (RSD) recomendam não ultrapassar o limite de 1000 ppm (parte por milhão) "em condições normais de ocupação", com uma tolerância de 1300 ppm em locais onde é proibido. Fumar ( "sem indicação explícita base de saúde para esses dois valores ", de acordo com a ANSES.
Um decreto de 5 de janeiro de 2012impõe monitoramento da qualidade do ar interno em determinados estabelecimentos que recebem públicos sensíveis, como crianças; propõe o cálculo de um “índice de confinamento” denominado “índice Icone” (proposto pelo Centro Científico e Técnico da Construção (CSTB) com base na frequência de superação dos níveis de CO 2 .em comparação com dois limites de 1000 e 1700 ppm nas salas de aula .
No local de trabalho , a questão da segurança e prevenção ligada ao risco de envenenamento por dióxido de carbono é uma grande preocupação, a fim de limitar o risco de acidentes de trabalho . Devido à falta de dados epidemiológicos, não foi considerado relevante na França como um indicador da qualidade sanitária do ar interno pela ANSES, que não fornece um valor-guia para a qualidade do ar interno (IGAI) para este poluente.
Em altas concentrações que se aproximam de 50 a 100%, como as encontradas em manchas de dióxido de carbono feitas pelo homem no local de trabalho, pode haver um efeito de espanto nervoso e perda imediata de consciência , seguido por morte rápida na ausência de ajuda externa. Estes acidentes apresentam um risco elevado de um segundo acidente , pois as testemunhas podem correr em socorro da vítima sem pensar na sua própria segurança e também se tornarem vítimas de intoxicação.
CO 2 na atmosfera da terra
O dióxido de carbono normalmente só está presente na atmosfera da Terra em pequenas quantidades. É medido por meio de um índice , denominado “ Índice Anual de Gases do Efeito Estufa ” (AGGI), desde 1979 por uma rede de cerca de cem estações terrestres e marítimas, localizadas do Ártico ao Pólo Sul.
Desde a revolução industrial , devido à combustão constante de grandes quantidades de carbono fóssil , enquanto o declínio de incêndios , florestas e áreas de vegetação continua, a taxa de CO 2no ar aumenta regularmente (em janeiro de 2021: 415,13 ppm em volume, ou também 632,96 ppm em massa. Isso corresponde a uma massa total de CO 2atmosférico de cerca de 3,258 × 10 15 kg (cerca de três mil gigatoneladas ) . Esse conteúdo era de 283,4 ppmv em 1839 dos núcleos de gelo retirados da região da calota de Poinsett na Antártica , um aumento geral de cerca de 42% em 177 anos. A taxa de CO 2atmosférico esperado no final de XXI th século é estimada em entre 540 e 970 ppmv por simulações seleccionados (modelo ISAM e modelo Berna-CC). O ano de 1990 (que corresponde a um excedente de cerca de 2,1 W / m 2 em comparação com 1980 ) é o ano de referência usado para o protocolo de Kyoto (portanto, tem um “índice AGGI” de 1). Foi constituído um grupo específico de pesquisa sobre o ciclo do carbono e gases de efeito estufa.
No tempo t , o conteúdo de CO 2difere em cada hemisfério, com variações sazonais regulares em cada hemisfério (cf. padrão “dente de serra” no gráfico à direita, mostrando uma queda no CO 2na estação de vegetação e um aumento no inverno). Existem também variações regionais, em particular ao nível da camada limite atmosférica , ou seja, nas camadas próximas ao solo.
Níveis de CO 2 são geralmente mais elevados em áreas urbanas e em habitações (até dez vezes o nível de fundo).
Pouco depois da formação da Terra (muito antes do surgimento da vida), quando o sol estava quase a metade do “calor”, a pressão inicial de CO 2era cerca de 100.000 vezes maior do que hoje (30 a 60 atmosferas de CO 2( ou seja, 3.000.000 a 6.000.000 pascals), ou seja, 100.000 vezes a quantidade atual de CO 2 cerca de 4,5 bilhões de anos atrás).
Então a vida e a fotossíntese apareceram, levando o CO 2da atmosfera e da água para transformá-lo em rochas carbonáticas e carvão, petróleo e gás natural, grande parte dele enterrado nas profundezas da terra. A taxa de CO 2no entanto, ainda experimentou alguns picos de muito menos importância (vinte vezes mais altos do que hoje cerca de meio bilhão de anos atrás, mas o sol estava menos quente do que hoje (a radiação solar aumenta com o tempo e aumentou cerca de 40% nos últimos quatro bilhões de anos) a taxa de CO. 2caiu mais quatro e cinco vezes durante o Jurássico , depois diminuiu lentamente, exceto, de forma acelerada durante um episódio geologicamente breve, conhecido como o " evento Azolla " (cerca de 49 milhões de anos atrás).
O vulcanismo também emite CO 2(até 40% dos gases emitidos por certos vulcões durante as erupções subaéreas são dióxido de carbono) e certas fontes termais também o emitem (por exemplo, no sítio italiano de Bossoleto perto de Rapolano Terme onde em uma depressão em forma de bacia cerca de 100 m de diâmetro, em uma noite calma, o CO 2pode subir 75% em poucas horas, o suficiente para matar insetos e pequenos animais. Mas a massa de gás aquece rapidamente quando o local está ensolarado e é então dispersa pelas correntes de convecção do ar durante o dia. Concentrações localmente altas de CO 2, produzido pela perturbação da água de um lago profundo saturado com CO 2também pode matar (exemplo: 37 mortes durante uma erupção de CO 2do Lago Monoun em Camarões em 1984 e 1.700 vítimas ao redor do Lago Nyos (também Camarões) em 1986.
Emissões de CO 2por atividades humanas são atualmente mais de 130 vezes maiores que a quantidade emitida por vulcões, totalizando quase 27 bilhões de toneladas por ano em 2007. Em 2012, a China foi o maior emissor mundial de dióxido de carbono com 27% do total, e os Estados Unidos Os estados, em segundo lugar, produzem 14% do total mundial. Em 2016, a agência meteorológica da ONU relata que a concentração de dióxido de carbono atingiu um novo recorde histórico de 403,3 ppm , e um recorde de temperatura foi quebrado para o El Niño de 2017 de acordo com a OMM, enquanto com 405 ppm , o CO 2 o ar nunca esteve tão alto em cerca de 800.000 anos.
Emissões globais de CO 2aumentou 2,7% em 2018, o maior aumento em sete anos. Em um relatório de 2019, as concentrações de CO 2atingiu 407,8 ppm em 2018, um achado também correlacionado com o aumento nas concentrações de metano (CH 4) e óxido nitroso (N 2 O)
Nutriente para plantas
Um nível mais alto de CO 2estimula a fotossíntese e o crescimento das plantas, com benefícios potenciais para a produtividade das safras de cereais, a principal fonte de alimento mundial para humanos e animais de fazenda. O carbono, retirado do dióxido de carbono do ar por plantas autotróficas por meio do processo de fotossíntese, ou retirado do carbono do solo, é de fato um dos principais nutrientes da cadeia alimentar . O aumento na biomassa é um efeito de experimentos simulados que prevêem um aumento de 5-20% no rendimento da colheita a 550 ppm de CO 2. Foi demonstrado que as taxas de fotossíntese foliar aumentam 30-50% em plantas C3 e 10-25% em C4 abaixo dos níveis de CO 2 dobrou.
A partir de 2010, surge um quadro mais completo, com uma diferença significativa nas respostas observadas para as diferentes espécies de plantas, disponibilidade de água e concentração de ozônio . Por exemplo, o projeto de enriquecimento de concentração de ar livre de Horsham ( FACE) 2007-2010 (usando safras de trigo) em Victoria, Austrália, descobriu que "o efeito do CO2 era aumentar a biomassa da safra. Na maturidade de 20% e a biomassa da raiz do antese 49% ". Verificou-se que um aumento no dióxido de carbono atmosférico reduz o consumo de água das plantas e, portanto, a absorção de nitrogênio , o que beneficia particularmente o rendimento das safras em regiões áridas.
Efeitos previstos sobre o valor nutricional das plantas
No entanto, se o aumento do nível de CO 2A atmosfera efetivamente estimula o crescimento (de cereais, por exemplo), por razões ainda pouco conhecidas, reduz então o valor nutricional das principais culturas básicas ( arroz , trigo e batata em particular), ao reduzir sua taxa de proteína , de oligoelementos e vitaminas do complexo B . Em condições experimentais, o nível de CO 2aumentado (mesmo não combinado com um aumento de temperatura) resulta em um maior nível de açúcar nas plantas cultivadas (fonte de álcoois cada vez mais fortes para as uvas), mas também por deficiências de proteínas e minerais. O arroz também costuma conter altas concentrações de arsênico , que a acidificação da mídia pode piorar. Finalmente, maiores concentrações de CO 2agravar a acidificação da água doce e a acidificação dos oceanos , o que pode afetar a produtividade das algas (e, portanto, a cultura de algas ).
Por esse motivo, de acordo com um estudo recente (2018), de 2015-2050, o nível anormalmente alto de CO 2de nossa atmosfera poderia no mundo antes de 2050 levar a doenças induzidas em humanos e certos animais de fazenda (porcos, vacas, aves) por deficiências nutricionais. Em um estudo publicado em uma edição especial da PLOS Medicine sobre mudança climática e saúde, Christopher Weyant e seus colegas da Universidade de Stanford se concentraram em dois micronutrientes essenciais, zinco e ferro. Levando em consideração as mudanças climáticas e os hábitos alimentares, eles mostram que o risco de doenças mudará nos 137 países. Se nada for feito, o aumento da taxa de CO 2diminuirá os níveis de zinco e ferro nos alimentos, custando cerca de 125,8 milhões de anos de vida ajustados por deficiência (intervalo de confiança de 95% [CrI] 113,6–138,9) em todo o mundo para o período de 2015–2050, devido a um aumento nas doenças infecciosas , diarreia e casos de anemia , especialmente no Sudeste Asiático e na África, onde a população já é gravemente afetada por deficiências de zinco e ferro. As crianças seriam particularmente afetadas, com o risco de distúrbios irreversíveis do desenvolvimento ligados a essas deficiências, que podem ser transmitidas ao longo de várias gerações, pelo menos por razões epigenéticas .
O estudo de Weyant também indicaria que a desigualdade nutricional pode aumentar e mostraria que as respostas tradicionais de saúde pública (incluindo suplementação com minerais e vitaminas e controle reforçado de doenças humanas e animais) podem não ser suficientes para conter o fenômeno da doença. Na verdade, essas respostas só iria reduzir 26,6% (95% de CI 23,8-29,6) deste saúde, humana e carga econômica, enquanto uma estratégia eficaz para reduzir as emissões de gases de efeito estufa. Efeito estufa, conforme proposto pelo acordo climático Paris , impediria até 48,2% (95% do índice CIF 47,8–48,5) desta carga.
Embora CO 2nutre o crescimento das plantas, o seu excesso induz uma degradação do seu valor alimentar que terá consequências globais para todos os seres vivos que consomem as plantas, incluindo os humanos. Os autores encorajam um melhor estudo dos efeitos do aumento de CO 2atmosférico em outros compostos de origem vegetal com implicações para a saúde humana (por exemplo, ácidos graxos, vitaminas, compostos farmacológicos, especialmente porque este estudo não levou em consideração outras consequências do aumento de CO 2, sobre os riscos meteorológicos e biológicos (aumento da depredação, etc.) sobre a segurança alimentar, o acesso aos alimentos, seu uso e estabilidade de preços, nem sobre as cadeias de consequências atrasadas no espaço e no tempo (efeitos a longo prazo da desnutrição em particular).
A produção agrícola está estagnada ou se deteriorando em uma parte do mundo, em particular devido ao aquecimento (ondas de calor, etc.) e regimes de precipitação modificados. Culturas vitais (trigo e arroz em particular) já são afetadas em zonas tropicais e temperadas e estudos prospectivos sugerem que as safras de arroz e milho podem diminuir em 20 a 40% apenas por causa dos aumentos de temperatura esperados na zona. Tropical e subtropical em 2100, mesmo levando em consideração os efeitos de eventos climáticos extremos. Este contexto pode fazer com que os preços dos alimentos subam, tornando-os inacessíveis para os mais pobres, enquanto o aumento dos níveis de CO 2 no arpoderia também reduzir a qualidade nutricional, em particular dos cereais, importantes para a saúde humana e, potencialmente, para a dos animais (também fontes de leite e carne (e portanto de proteínas), enquanto no mar a biomassa nos peixes também diminui.
“Ainda não está claro se o declínio no valor nutricional das culturas alimentares induzido pelo CO 2é linear e se a qualidade nutricional já diminuiu devido ao aumento de CO2 desde o início da revolução industrial. "
Além de medidas de adaptação às mudanças climáticas, medidas para reduzir as emissões de CO 2e captura biológica de CO 2são urgentemente necessários. Algumas cultivares menos suscetíveis a déficits nutricionais em um clima mais quente estão buscando concluir o trabalho de Weyant e colegas.
Os efeitos do aumento do CO 2sobre as plantas são mais preocupantes do que o previsto pelos primeiros modelos dos anos 1990 e início dos anos 2000. Morgan et al. , com base em experimentos de laboratório e in situ , confirmou já em 2004 que em ecossistemas emergidos, CO 2, mesmo quando melhora a produtividade em termos de biomassa, pode, no entanto, ter efeitos negativos, modificando a composição das espécies e reduzindo a digestibilidade de gramíneas baixas, por exemplo na vegetação de estepe ).
Gás de efeito estufa e acidificante
CO 2é o segundo gás de efeito estufa mais importante na atmosfera depois do vapor d'água , contribuindo com 26% e 60%, respectivamente, para esse fenômeno. A realidade do aquecimento global observada em escala planetária desde o século passado não é mais contestada do ponto de vista científico, mas a exata parcela de responsabilidade do dióxido de carbono neste processo (em relação ao metano em particular) ainda precisa ser esclarecida, graças a registros fósseis de paleoclimas em particular.
Além disso, a acidificação resultante da dissolução de dióxido de carbono atmosférico pode pôr em risco a sobrevivência de muitos organismos marinhos antes da XXI th século, particularmente aqueles em exoesqueleto calcificada, tais como corais e moluscos , mas também alguns peixes.
A redução das emissões antrópicas é visada pelo Protocolo de Quioto, bem como pela Diretiva 2003/87 / CE ; seu sequestro geológico de longo prazo é objeto de pesquisa, mas é uma solução controversa quando se trata de simplesmente injetar CO 2 em camadas geológicas.
Efeitos do ecossistema do aumento dos níveis de CO 2 na água e no ar
Na águaCO 2tem certo efeito eutrófico (é um nutriente básico, essencial para as plantas), mas também é um fator de acidificação dos oceanos e de certos corpos de água doce , podendo interferir negativamente em muitas espécies (inclusive certas microalgas e outras aquáticas microrganismos protegidos por estruturas calcárias que o ácido carbônico pode dissolver). A acidificação também promove a liberação e a circulação e, portanto, a biodisponibilidade da maioria dos metais pesados , metaloides ou radionuclídeos (naturalmente presentes em sedimentos ou de origem antropogênica principalmente a partir da revolução industrial).
No arO aumento no conteúdo de CO 2 da atmosferatambém pode ter efeitos diferenciados ou mesmo antagônicos dependendo da sua taxa, do contexto ambiental e biogeográfico e de acordo com dados mais recentes dependendo da estação e das variações sazonais da precipitação (acima das florestas em particular);
Há um consenso entre os ecologistas associados ao estudo dos efeitos das mudanças climáticas de que, além de um aumento de 2 ° C em um século, os ecossistemas terrestres e marinhos serão seriamente afetados negativamente.
Em 2013 , a resposta real dos ecossistemas ao CO 2e suas modulações biogeográficas ainda são consideradas complexas e para serem melhor compreendidas, devido aos inúmeros "feedbacks biogeoquímicos " . No entanto, deve ser elucidado se queremos avaliar corretamente ou mesmo prever as capacidades planetárias ou locais dos ecossistemas em termos de armazenamento natural de carbono e amortecimento dos efeitos das mudanças climáticas induzidas pelo homem.
O feedback mediado pelo ciclo hidrológico é particularmente importante e as chuvas desempenham um papel importante. A fisiologia das plantas tem pelo menos um papel bem conhecido; até um determinado estágio (além do qual a planta morre), o aumento no nível de CO 2de ar reduz a condutância estomática e aumenta a eficiência do uso da água pelas plantas (a quantidade de água necessária para produzir uma unidade de matéria seca ), a diminuição do uso da água está resultando em maior disponibilidade de umidade no solo. Foi estimado em 2008 que os efeitos do aumento do CO 2no ar no ecossistema deve ser exacerbado quando a água é um fator limitante (mas as entradas de nitrogênio também devem ser levadas em consideração); isso foi demonstrado por alguns experimentos, mas é um fator que foi "esquecido" por muitos estudos.
Essa relação parece tão forte que torna possível - em zonas temperadas - prever com precisão as variações anuais na estimulação da biomassa aérea após o aumento do nível de CO 2.em uma pastagem mista contendo plantas do tipo C3 e C4 , com base na precipitação sazonal total ; o verão chuvoso tem um efeito positivo, enquanto o outono e a primavera têm efeitos negativos na resposta ao CO 2. O efeito do aumento dos níveis de CO 2 dependerá, portanto, principalmente dos novos equilíbrios ou desequilíbrios que serão estabelecidos entre as precipitações do verão e do outono / primavera.
A ligação com o nitrogênio (outro elemento perturbado pelas atividades humanas, incluindo a agricultura industrial, a indústria e as emissões do tráfego automotivo ) é encontrada aqui: a forte precipitação em estações frias e chuvosas leva a limitar o acesso aos veículos. Plantas terrestres com nitrogênio e, portanto, reduzem ou proíbem a estimulação da biomassa por um nível de CO 2criado. Verificou-se também que esta previsão também realizada para tramas "aquecido" por 2 ° C ou sem aquecimento, e foi semelhante para as plantas em C3 e biomassa total, o que parece permitir que as previsões de fazer robustas previsões. Em respostas a alta CO 2 concentraçõesdo ecossistema . Este é um ativo valioso porque as projeções climáticas dos modelos de alta resolução confirmam a probabilidade muito alta de grandes mudanças na distribuição anual da chuva, mesmo quando a quantidade anual total de chuva que caiu no solo não mudará. Esses dados confirmados cientificamente (em 2013) devem ajudar a explicar algumas das diferenças que apareceram nos resultados de experimentos baseados na exposição de plantas a níveis aumentados de CO 2., e melhorar a eficiência prospectiva de modelos que não levaram suficientemente em consideração os efeitos sazonais da precipitação nas respostas da biodiversidade ao CO 2 14, especialmente em ambientes florestais.
Redução de CO 2 no ar
Diversas maneiras são exploradas ou implementadas para limitar o acúmulo de CO 2no ar. Eles podem envolver processos naturais, como fotossíntese ou processos industriais. Também deve ser feita uma distinção entre captura na fonte e captura na atmosfera.
A startup Indian Carbon Clean Solutions (CCSL) lançou sua primeira instalação, que captura e reutiliza 100% de CO 2(60.000 toneladas por ano) de uma pequena central elétrica movida a carvão na Índia, em Chennai (Madras); este CO 2é purificado e depois vendido a um industrial local, que o usa para fazer refrigerante. A tecnologia CCSL reduz o custo de CO 2vendido a 30 dólares por tonelada na Índia e 40 dólares na Europa ou nos Estados Unidos, muito abaixo do preço de mercado: 70 a 150 dólares por tonelada. A Veolia fechou contrato com o CCSL para comercializar esse processo internacionalmente. Ao mesmo tempo, a empresa Climeworks busca capturar CO 2 filtrando o ar ambiente.
A empresa canadense Carbon Engineering, fundada pelo engenheiro David Keith e financiada por Bill Gates e várias empresas de petróleo e mineração, desenvolveu um reator que extrai CO 2atmosfera a um custo menor do que as tecnologias de captura existentes. Os recursos disponibilizados pelos investidores serão utilizados para combinar esse processo de captura direta com um processo “Air to fuels”, permitindo que o carbono recuperado na atmosfera seja transformado em um combustível semelhante à gasolina. Ela planeja construir uma grande fábrica em Houston em parceria com a Occidental Petroleum . No entanto, reatores sensores de CO 2consomem muita energia e, portanto, devem ser alimentados por fontes de energia renováveis; o Conselho Científico das Academias de Ciências Europeias (EASAC) tem reservas: segundo ele, a eliminação do CO 2 no ar não impedirá as mudanças climáticas e, até o momento, não está de acordo com as recomendações do IPCC.
Rumo à produção de "metano solar" a partir de CO 2 ? .
Em teoria, a transformação do CO 2em combustível ou matérias-primas químicas reduziriam o uso de combustíveis fósseis e reduziriam as emissões de CO 2.
A conversão eletroquímica de fontes renováveis de eletricidade tem sido objeto de muitas pesquisas desde a década de 2010.
Uma esperança, com base na fotoquímica , é que só possamos usar a luz do sol e catalisadores não poluentes que são baratos e abundantes na Terra. Entre os fotocatalisadores e eletrocatalisadores moleculares citados na literatura científica da década de 2010, poucos são estáveis e seletivos para a redução de CO 2 ; além disso, eles produzem principalmente CO ou HCOO, e catalisadores capazes de gerar rendimentos mesmo baixos a moderados de hidrocarbonetos muito reduzidos permanecem raros.
Quatro pesquisadores, incluindo dois franceses (Julien Bonin & Marc Robert) produziram um catalisador que é um complexo de tetrafenilporfirina de ferro funcionalizado com grupos trimetilamônio , que apresentam como sendo (no momento da publicação) o mais eficiente e seletivo para converter CO 2em CO porque pode catalisar a redução de oito elétrons de CO 2em metano sob luz simples, em temperatura e pressão ambiente. O catalisador deve, no entanto, ser usado em uma solução de acetonitrila contendo um fotossensibilizador e um doador de elétrons de sacrifício; ele então opera de forma estável por alguns dias. CO 2é primeiro principalmente transformado em CO por fotorredução e se houver dois reatores CO, em seguida, gera metano com uma seletividade de até 82% e com um rendimento quântico , ou seja, uma eficiência de luz de 0, 18%). Os autores acreditam que outros catalisadores moleculares poderiam ser inspirados por ele.
Também são considerados sistemas de "cocatálise", de catalisadores moleculares, bem como sistemas baseados em perovskita , ou baseados em complexos de metais de transição .
Notas e referências
- DIÓXIDO DE CARBONO , folha de segurança (s) de Programa Internacional de Segurança Química , consultado sobre 9 maio de 2009
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- " dióxido de carbono " , sobre substâncias perigosas Data Bank (acedida 8 de março de 2010 )
- Bernard M. e Busnot F. (1996), Usuel de química geral e mineral , Dunod, Paris, p. 229 .
- (en) Robert H. Perry e Donald W. Green , Perry's Chemical Engineers 'Handbook , Estados Unidos, McGraw-Hill,1997, 7 th ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- (em) WM Haynes, Handbook of Chemistry and Physics , CRC, 2010-2011 91 th ed. , 2610 p. ( ISBN 978-1-4398-2077-3 ) , p. 14-40
- (em) Irvin Glassman e Richard A. Yetter, Combustion , Amsterdam / Boston, Elsevier,2008, 4 th ed. , 773 p. ( ISBN 978-0-12-088573-2 ) , p. 6
- (em) Carl L. Yaws, Handbook of Thermodynamic Diagrams , Vol. 1-3, Huston, Texas, Gulf Pub.,1996( ISBN 0-88415-857-8 , 978-0-88415-858-5 e 978-0-88415-859-2 )
- (em) David R. Lide, Manual de Química e Física , CRC,2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205
- “ dióxido de carbono ” , em www.reciprocalnet.org (acessada 12 de dezembro de 2009 )
- Entrada de número CAS "124-38-9" no banco de dados química GESTIS da IFA (organismo alemão responsável pela segurança e saúde ocupacional) ( alemão , Inglês ), acessado em 06 de dezembro de 2008 (JavaScript obrigatório)
- SIGMA-ALDRICH
- " Dióxido de carbono " no banco de dados de produtos químicos Reptox da CSST (organização de Quebec responsável pela segurança e saúde ocupacional), acessado em 25 de abril de 2009
- (em) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 p. , capa dura ( ISBN 978-1-4200-9084-0 ) , p. 6-107
- Frédéric Datchi, " A molécula de CO 2resiste à pressão melhor do que o esperado. » , No Instituto de Mineralogia e Física de Meios Condensados (IMPMC, Paris) ,abril de 2010(acessado em 28 de janeiro de 2016 ) .
- T. Uchida, S. Mae, J. Kawabata e T. Hondoh, “Physical Data of CO 2Hydrate ” , em N. Handa e T. Ohsumi (dir), Direct Ocean Disposal of Carbon Dioxide , Terra Scientific Publishing Company (TERRAPUB),1995, 45-61 p. ( leia online ).
- HS Chen, A termodinâmica e composição dos hidratos de dióxido de carbono , Tese de MS, Syracuse University, Nova York, 1972.
- H. Lee, C.-S. Lee, W.-M. Sung e S.-P. Kang, equilíbrio da fase hidratada das misturas hóspedes contendo CO 2, N2 e tetra-hidrofurano , Fluid Phase Equilib. , 2001, 185, 101
- P. Englezos, R. Kumar e J. Ripmeester, O processo de hidrato de gás para separação de CO 2da mistura de gás combustível: estudos de nível macro e molecular , Anais da 6ª Conferência Internacional sobre Hidratos de Gás (ICGH) , 2008
- P. Linga, R. Kumar e P. Englezos, The clathrate hydrate process for post and precombustion capture of carbon dioxide , J. Hazard. Mater. , 2007a, 149 (3), 625–629.
- NH Duc, F. Chauvy e J.-M. Herri, CO 2captura por cristalização de hidrato - Uma solução potencial para a emissão de gases da indústria siderúrgica , Energia. Conv. Manag. , 2007, 48, 1313–1322.
- Wassila Bouchafaa, Medição e modelagem das condições de dissociação de hidratos gasosos estabilizados para aplicação na captura de CO 2 (tese de doutorado da École Polytechnique), 22 de novembro de 2011
- YD Kim, HJ Lee, YS Kim e JD Lee, um estudo de dessalinização de CO 2tecnologia de hidratos , Anais da 6ª Conferência Internacional sobre Hidratos de Gás (ICGH) , 2008
- MD Max, K. Sheps, SR Tatro e LB Osegovic, dessalinização da água do mar como fator benéfico de CO 2sequestro , Proceedings of the 6th International Conference on Gas Hydrates (ICGH) , 2008
- cap. I-4.3. Extração de metano simultânea e processo de armazenamento de CO 2, p. 61 (ou p. 67 da versão [PDF] ) da tese de Nadia Mayoufi, Caracterização de coulis de hidrato contendo CO 2aplicada a sistemas de refrigeração , tese de doutorado, École Polytechnique, 8 de dezembro de 2010
- (in) " Dióxido de Carbono: Sylvester Spiritus " Ebbe Almqvist, História dos gases industriais , Springer,2003, 472 p. ( ISBN 978-0-306-47277-0 , leia online ), p.
- Sigaud de La Fond, Ensaio sobre diferentes espécies de ar fixo ou gás… , Paris, Chez P. Fr. Gueffier,1785( leia online )
- (em) Joseph Priestley , " Observations on Different Kinds of Air " , Phil. Trans. , vol. 62,1772, p. 147-264 ( ISSN 0260-7085 , DOI 10.1098 / rstl.1772.0021 , ler online )
- (em) Humphry Davy , " On the Application of the Liquids Formed by Condensation of Gases as Mechanical Agents " , Phil. Trans. , vol. 113,1823, p. 199–205 ( ISSN 0261-0523 , DOI 10.1098 / rstl.1823.0020 , leia online [PDF] )
- (en) Charles Thilorier, " Solidification of carbic acid " , CR Hebd. Sessões Acad. Sci. , vol. 1,1835, p. 194-196 ( ler online )
- (em) HD Roller Duane , " Thilorier First and the solidification of a Permanent Gas (1835) " , Isis , vol. 43, n o 21952, p. 109-113 ( ISSN 0021-1753 , DOI 10.1086 / 349402 )
- Dominique Pialot, “ CO2, um novo mercado? » , Em latribune.fr ,17 de junho de 2019(acessado em 6 de agosto de 2019 ) .
- (em) " Dióxido de carbono para alimentos e bebidas grau fonte qualificação, padrões de qualidade e verificação: EIGA Doc 70/17 " em eiga.eu ,2016(acessado em 12 de julho de 2019 ) .
- (pt) Putting CO2 to Use - Criando Valor a partir das emissões , Agência Internacional de Energia , em setembro de 2019.
- Neil A. Campbell e Jane B. Reece , Biology , Erpi,2007, 1.400 p.
- Carboglace é uma marca registrada na França pela Air Liquide
- von Baczko, K., ed. Gmelins Handbuch der Anorganischen Chemie: Kohlenstoff , 8 th ed. , Chemie GMBH, Weinheim / Bergstr., 1970, Parte C. Seção 1, p. 413–416 .
- Phillips, RJ, Davis, BJ, Tanaka, KL, Byrne, S., Mellon, MT, Putzig, NE, ... & Smith, IB (2011) Enormes depósitos de gelo de CO2 sequestrados nos depósitos de camadas polares sul de Marte . Science, 332 (6031), 838-841.
- (em) " A rede de reação no estágio de oxidação de propano sobre catalisadores de óxido MoVTeNb M1 puro " , Journal of Catalysis , Vol. 311,2014, p. 369-385 ( ler online )
- (em) " Química de superfície da fase de óxido puro M1 MoVTeNb Durante a operação em oxidação seletiva de propano em ácido acrílico " , Journal of Catalysis , Vol. 285,2012, p. 48-60 ( ler online )
- (in) Estudos cinéticos de oxidação de propano em catalisadores à base de óxidos mistos de Mo e V ,2011( leia online )
- (in) " multifuncionalidade de catalisadores de óxido de MoV cristalino (NBPT) M1 na oxidação seletiva de propano e álcool benzílico 3 (6) " , ACS Catalysis , vol. 3, n o 6,2013, p. 1103-1113 ( ler online )
- (em) Colin Finn , Sorcha Schnittger Lesley J. Yellowlees e Jason B. Love , " Molecular aproximações à redução eletroquímica de dióxido de carbono " , Chemical Communications , vol. 48, n o 10,2012, p. 1392-1399 ( PMID 22116300 , DOI 10.1039 / c1cc15393e ).
- (en) CO2. Concentração terrestre de CO 2 na atmosfera da Terra.
- Intoxicação por inalação de dióxido de carbono , arquivo médico-técnico 79, INRS, 1999.
- CO 2 concentrações no ar interior e efeitos na saúde, parecer ANSES, laudo pericial coletivo, ANSES, 2013/07, 294 p.
- Observatório da Qualidade do Ar Interior (Oqai), Ministério da Ecologia, Ademe, CSTB, AirParif, Atmo ...
- (em) Chatzidiakou, L. Mumovic, D., & Summerfield, A. (2015). É CO 2um bom indicador da qualidade do ar interno nas salas de aula? Parte 1: As inter-relações entre as condições térmicas, níveis de CO2, taxas de ventilação e poluentes internos selecionados. Building Services Engineering Research and Technology, 36 (2), 129-161 ( resumo ).
- (em) Cetin Sevik M & H (2016) Análise de qualidade interna de CO2 para a Universidade de Kastamonu . In Conference of the International Journal of Arts & Sciences (Vol. 9, No. 3, p. 71).
- (em) Jaber AR Dejan Marcella M & U (2017) O efeito da temperatura interna e dos níveis de CO2 é o desempenho cognitivo de mulheres adultas em um prédio universitário na Arábia Saudita , Energy Procedia , 122, 451-456.
- (in) Myhrvold AN, Olsen S & Lauridsen O Ambiente interno em escolas, alunos e desempenho de saúde em relação às concentrações de CO2 , Ar interno , 96 (4), 369-371, 1996
- (en) Prestmo LS (2018) As medições de parâmetros de clima interior na zona de exercício por um hall de hóquei no gelo (tese de mestrado, NTNU).
- (in) Prestmo LS (2018) Medições de parâmetros de clima interno na área de exercícios de uma sala de hóquei no gelo (dissertação de mestrado, NTNU) (consulte a Seção 7.2 Aumento de CO 2 concentração durante uma partida)
- (em) Ex: Kenneth W. Rundell (2004) "Decadência da função pulmonar em jogadoras de hóquei no gelo: há uma relação com a qualidade do ar da pista de gelo? " Inhalation Toxicology , 16 (3): 117-123
- Intoxicação por inalação de dióxido de carbono , ficha médico-técnica 79 TC 74, INRS
- D Dr. Pieter Tans (3 de maio de 2008) CO 2 anualaumento da fração molar (ppm) para 1959–2007 , National Oceanic and Atmospheric Administration , Earth System Research Laboratory , Global Monitoring Division ( detalhes adicionais ).
- NOAA / Law Dome
- NOAA / Mauna Loa
- Unidade de Pesquisa Climática (Univ. East Anglia)
- Centro de Análise de Dados de Influências Solares (SIDC)
- http://advances.sciencemag.org/content/3/1/e1601207
- Tendências em dióxido de carbono atmosférico - CO2 médio mensal global , National Oceanic & Atmospheric Administration (NOAA) - Earth System Research Laboratories (ESRL), acessado em 25 de abril de 2021.
- (in) Centro de Análise de Informações de Dióxido de Carbono, em junho de 1998 , " CO 2 Históricoregistro derivado de um ajuste de spline (corte de 20 anos) dos núcleos de gelo Law Dome DE08 e DE08-2 ”, DM Etheridge, LP Steele, RL Langenfelds, RJ Francey (Divisão de Pesquisa Atmosférica, CSIRO, Aspendale, Victoria, Austrália), J.-M. Barnola ( Laboratório de Glaciologia e Geofísica Ambiental , Saint-Martin-d'Hères , França) e VI Morgan (CRC Antártico e Divisão Antártica Australiana, Hobart, Tasmânia, Austrália)
- (in) Programa das Nações Unidas para o Meio Ambiente (PNUMA) - Terceiro Relatório de Avaliação de Mudanças Climáticas 2001 , " Mudanças Climáticas 2001: Grupo de Trabalho I: A Base Científica - Capítulo 3. O Ciclo de Carbono e o Dióxido de Carbono Atmosférico " Resumo Executivo
- Informações sobre o nosso planeta, conteúdo de CO 2aumentou acentuadamente de 1990 a 2004 (acessado em 31 de março de 2012)
- Divisão de Monitoramento Global da ESRL
- Gases de efeito estufa do ciclo de carbono do Grupo de Pesquisa
- Dossiê Atmosfera , Pour la science , junho de 1996
- Guia da Terra / UCSD, Clima e CO 2na atmosfera (acessado em 10 de outubro de 2007)
- Robert A. Berner e Zavareth Kothavala, GEOCARB III: Um modelo revisado de CO 2 atmosféricoover Phanerozoic [PDF] , American Journal of Science , vol. 301, 2001, c. 2, p. 182-204, DOI : 10.2475 / ajs.301.2.182 (acessado em 15 de fevereiro de 2008)
- Sigurdsson, Haraldur and Houghton, BF, Encyclopedia of volcanoes , 2000, Academic Press, San Diego ( ISBN 0-12-643140-X )
- van Gardingen, PR; Grace, J .; Jeffree, CE; Byari, SH; Miglietta, F.; Raschi, A.; Bettarini, I., cap. Efeitos de longo prazo do aumento do CO 2concentrações nas trocas gasosas da folha: oportunidades de pesquisa usando CO 2Springs , editor: Raschi, A .; Miglietta, F.; Tognetti, R.; van Gardingen, PR (ed.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , p. 69-86
- Martini M., cap. CO 2emissões em áreas vulcânicas: histórias de casos e hazaards , em respostas de plantas a CO 2 elevado: Evidência de fontes naturais , editor: Raschi, A.; Miglietta, F.; Tognetti, R.; van Gardingen, PR (ed.), 1997, Cambridge University Press, Cambridge ( ISBN 0-521-58203-2 ) , p. 69-86
- Os gases vulcânicos e seus efeitos (in) , acessado 2007-09-07
- Martin Wolf, " Climate Change Skeptics Are Losing Ground " , no The New Economist ,17 de julho de 2014(acessado em 26 de julho de 2014 ) .
- " Sempre mais CO 2na atmosfera ”, La Croix ,30 de outubro de 2017( ISSN 0242-6056 , ler online , acessado em 31 de outubro de 2017 )
- Gamilloaug E., carbono atmosférico no ano passado atingiu níveis não vistos em 800.000 anos , Science News , 2 de agosto de 2018
- " Emissões globais de CO 2“Escorregou” em 2018, em + 2,7% ” , em Liberation.fr (consultado em 6 de dezembro de 2018 )
- " CO2 " .
- Lobell DB & Field CB (2008) Estimativa do dióxido de carbono (CO 2) efeito de fertilização usando anomalias da taxa de crescimento de CO 2e safras desde 1961 . Glob Chang Biol. ; 14 (1): 39–45.
- FN Tubiello , JF Soussana e SM Howden , “ Respostas de culturas e pastagens às mudanças climáticas ”,2007( PMID 18077401 , PMCID 2148358 , DOI 10.1073 / pnas.0701728104 , Bibcode 2007PNAS..10419686T ) ,p. 19686–19690
- (em) Rob Norton et al. O efeito do dióxido de carbono elevado no crescimento e rendimento do trigo no experimento de Enriquecimento com Dióxido de Carbono no Ar Livre de Grãos Australianos (AGFACE) , regional.org.au 2008
- (in) Daniel R. Taub, Effects of Rising Atmospheric Carbon Dioxide Concentrations of one Plants , Nature , Education Knowledge 3 (10): 21, 2010
- (in) Taub DR, Miller B, Allen H. Efeitos de CO2 elevado na concentração de proteína de culturas alimentares: uma meta-análise , Global Change Biology 1 de março; 14 (3): 565-75, 27 de novembro de 2007
- (pt) Myers SS Zanobetti A, Kloog I, P Huybers, Leakey AD, Bloom AJ, et al. (2014), O aumento do CO2 ameaça a nutrição humana. Nature . Jun; 510 (7503): 139.
- (em) Zhu C, Kobayashi K, Loladze I, Zhu J, Jiang Q, Xu, et al. (2018), os níveis de dióxido de carbono (CO2) neste século irão alterar o conteúdo de proteínas, micronutrientes e vitaminas dos grãos de arroz com consequências potenciais para a saúde dos países mais pobres dependentes do arroz , Sci Adv. 2018: 4: eaaq1012.
- (in) Loladze I (2014) Mudança oculta do ionoma de plantas expostas a elevados minerais com empobrecimento de CO2 na base da nutrição humana , Elifa . ; 3: e02245.
- (em) Andrew A. Meharg, Jeanette Hartley-Whitaker (2002) Absorção e metabolismo de arsênio em espécies de plantas resistentes e não resistentes ao arsênio, publicado em 4 de abril de 2002 DOI: 10.1046 / j.1469-8137.2002.00363.x Edição Novo fitologista , Volume 154, Edição 1, páginas 29-43, abril de 2002
- (pt) Ebi KL, Ziska LH (2018) Aumentos no dióxido de carbono atmosférico: efeitos negativos previstos na qualidade dos alimentos. PLoS Med 15 (7): e1002600. https://doi.org/10.1371/journal.pmed.1002600 ; Estudo publicado sob a licença de domínio público CC0 da Creative Commons
- (em) Helena Bottemiller evich, " O grande colapso dos nutrientes " , Politico ,13 de setembro de 2017( leia online , consultado em 13 de setembro de 2017 ).
- (in) Weyant C Brandeau ML, Burke M, DB Lobell, Bendavid S & S Basu (2018), Carga antecipada e mitigação de deficiências nutricionais induzidas por dióxido de carbono e doenças relacionadas: um estudo de modelagem de simulação, PLoS Med. ; 15 (7): e1002586
- Vickers MH (2014) Nutrição na primeira infância, epigenética e programação de doenças na velhice . Nutrientes. 2 de junho; 6 (6): 2165–78.
- Zhu C, Zeng Q, McMichael A., Ebi KL, Ni K, Khan AS, et al. (2015) Evidências históricas e experimentais para a concentração aumentada de artemesinina, um tratamento antimalárico global, com aumentos recentes e projetados no dióxido de carbono atmosférico . Das Alterações Climáticas. 1 de setembro; 132 (2): 295–306
- Porter JR, Xie L, Challinor AJ, Cochrane K, Howden SM, Iqbal MM, et al. (2014) Segurança alimentar e sistemas de produção de alimentos . In: Mudanças Climáticas 2014: Impactos, Adaptação e Vulnerabilidade. Parte A: Aspectos globais e setoriais. Contribuição do Grupo de Trabalho II para o Quinto Relatório de Avaliação do Painel Intergovernamental sobre Mudanças Climáticas [Field CB, Barros VR, Dokken DJ, Mach KJ, Mastrandrea MD, et al. (eds.)]. Cambridge University Press, Cambridge, Reino Unido e Nova York, NY, EUA, pp. 485-533
- Battisti DS & Naylor RL (2009) Avisos históricos de insegurança alimentar futura com calor sazonal sem precedentes . Science 323, 240–244.
- (em) Nowak RS, SD Ellsworth DS e Smith (2004), Respostas funcionais de plantas para CO atmosférica elevada dois- os dados fotossintéticos e de produtividade dos experimentos do FACE dão suporte às previsões iniciais? , New Phytol. , 162, 253-280 ( resumo )
- (em) Morgan JA et al. (2004), CO 2aumenta a produtividade, altera a composição das espécies e reduz a digestibilidade da vegetação de estepe de gramíneas baixas , Ecol. Appl. , 14, 208-219
- (em) JT Kiehl e Kevin E. Trenberth, " Earth's Annual Global Mean Energy Budget " , Bulletin of the American Meteorological Society , vol. 78, n o 2Fevereiro de 1997, p. 197-208 ( DOI 10.1175 / 2008BAMS2634.1 , leia online )
- (in) Mudanças climáticas: como sabemos? , NASA, sem data
- (en) Emmanuel Quiroz, Temperatura e CO 2Correlações encontradas nos registros do Ice Core , sem data
- (em) Bärbel Hönisch Andy Ridgwe Daniela N. Schmidt, Ellen Thomas, Samantha J. Gibbs, Appy Sluijs, Richard Zeebe, Lee Kump, Rowan C. Martindale, Sarah E. Greene, Wolfgang Kiessling, Justin Ries, James C. Zachos , Dana L. Royer, Stephen Barker, Thomas M. Marchitto Jr. , Ryan Moyer, Carles Pelejero Patrizia Ziveri, Gavin L. Foster e Branwen Williams, " The Geological Record of Ocean Acidification " , Science , vol. 335, n o 6072, 2 de março de 2012, p. 1058-1063 ( DOI 10.1126 / science.1208277 , ler online )
- (em) Joe Romm, Sociedade Geológica: Acidificação dos oceanos significa derretimento biológico marinho "até o final do século" , Progresso do Clima , 31 de agosto de 2010
- (en) C. Langdon e J. Atkinson, " Effect of Elevated p CO 2na fotossíntese e calcificação de corais e interações com mudança sazonal na temperatura / irradiância e enriquecimento de nutrientes ” , Journal of Geophysical Research , vol. 110,7 de setembro de 2005, C09S07 ( DOI 10.1029 / 2004JC002576 , ler online )
- (em) Katharina E. Fabricius, Chris Langdon, Sven Uthicke Craig Humphrey, Sam Noonan, Glenn De'ath, Remy Okazaki, Nancy Muehllehner, Martin S. Glas e Janice M. Lough, " Perdedores e vencedores em recifes de coral aclimatados a elevadas concentrações de dióxido de carbono ” , Nature Climate Change , vol. 1,29 de maio de 2011, p. 165-169 ( DOI 10.1038 / nclimate1122 , ler online )
- (em) Joe Romm, Dióxido de Carbono Is "Driving Fish Crazy" and Threatening their Survival, Study Finds , Climate Progress , 23 de janeiro de 2012.
- Sebastian Leuzinger e Christian Korner, “ A distribuição das chuvas é o principal motor do escoamento sob o futuro CO 2-concentração em uma floresta decídua temperada ”, Glob. Change Biol. , vol. 16,2010, p. 246-254 ( resumo )
- Peters, GP et al. , O desafio para manter o aquecimento global abaixo de 2 ° C , Nature Clim. Mudança , 3, 4-6, 2013
- Reich PB e Hobbie SE (2013), Década longa restrição de nitrogênio do solo no CO 2fertilização da biomassa vegetal , Nature Clim. Mudança , 3, 278-282 ( resumo )
- Mark J. Hovenden, Paul CD Newton e Karen E. Wills, “ A chuva sazonal e não anual determina a resposta da biomassa das pastagens ao dióxido de carbono ”, Nature , vol. 511,2014( DOI 10.1038 / nature13281 , resumo )
- Sokolov AP et al. (2008), Consequências de considerar as interações carbono-nitrogênio nos feedbacks entre o clima e o ciclo do carbono terrestre , J. Clim. , 21, 3776-3796 ( resumo e bibliografia )
- Morgan J. et al. (2011), gramíneas C4 prosperam à medida que o dióxido de carbono elimina a dessecação em pastagens semi-áridas aquecidas , Nature , 476, 202-205 ( resumo )
- (en) Leakey A. et al. (2009), CO 2 elevadoefeitos no carbono, nitrogênio e relações hídricas das plantas: seis lições importantes de FACE , J. Exp. Robô. , 60, 2859-2876 ( resumo )
- (em) McMurtrie, RE et al. (2008), Por que a resposta do crescimento da planta ao CO 2 elevadoamplificado quando a água é limitante, mas reduzido quando o nitrogênio é limitante? Uma hipótese de otimização de crescimento , Funct. Plant Biol. , 35, 521-534
- PB Reich, SE Hobbie, T. Lee et al. , " A limitação de nitrogênio restringe a sustentabilidade da resposta do ecossistema ao CO 2 », Nature , vol. 440,2006, p. 922-925 ( resumo )
- PB Reich, BA Hungate e Y. Luo, “ Interações de carbono-nitrogênio em ecossistemas terrestres em resposta ao aumento do dióxido de carbono atmosférico ”, Annu. Rev. Escola. Evol. Syst. , vol. 37,2006, p. 611-636 ( resumo )
- J. A. Morgan, DE Pataki, C. Körner et al. , " Relações hídricas em ecossistemas de pastagens e desertos expostos a elevado CO 2 atmosférico », Oecologia , vol. 140,2004, p. 11-25 ( leia online [PDF] )
- (en) Derner JD et al. , Respostas acima e abaixo do solo de misturas de espécies C3 - C4 ao CO 2 elevadoe disponibilidade de água no solo , Glob. Change Biol. , 9, 452-460, 2003
- (en) Dukes JS et al. (2005), Respostas da produção de pastagens a mudanças ambientais globais únicas e múltiplas , PLoS Biol. , 3, 1829-1837 ( resumo
- Grunzweig JM e Korner C. (2001), Crescimento, relações de água e nitrogênio em ecossistemas modelo de pastagens do semi-árido Negev de Israel exposto a elevado CO 2, Oecologia , 128, 251-262 ( resumo )
- (en) Marissink M., Pettersson A. e Sindhoj E. (2002) Produção de plantas acima do solo sob elevado dióxido de carbono em uma pastagem semi-natural sueca , Agric. Ecossistema. Cerca de. , 93, 107-120 ( resumo )
- (em) Singh D., Tsiang M., B. e Rajaratnam Diffenbaugh NS (2013) Extremos de precipitação sobre o território continental dos Estados Unidos em um experimento de modelo climático total transiente, de alta resolução , J. Geophys. Res. , D 118, 7063-7086 ( resumo )
- (em) Piao S. et al. (2013), Avaliação de modelos de ciclo de carbono terrestre para sua resposta à variabilidade climática e ao CO 2tendências , Glob. Change Biol. , 19, 2117-2132 ( resumo )
- (em) De Kauwe MG et al. (2013), Uso da água da floresta e eficiência do uso da água em elevado CO 2: a intercomparison model-data in two contrastate forest temperate FACE sites , Glob. Change Biol. , 19, 1759-1779 ( resumo )
- " O CCSL inicial e a Veolia irão capturar e revender o CO 2em grande escala " ,30 de março de 2017.
- Empresa canadense apoiada por Bill Gates quer capturar CO 2no ar , Le Figaro , 29 de junho de 2019.
- (em) Richard Littlemore, "Essa empresa pode ser parte da solução para mudanças climáticas do BC?" , The Globe and Mail , Report on business magazine , outubro de 2019
- Bonin J, Maurin A & Robert M (2017) Catálise molecular da redução eletroquímica e fotoquímica de CO 2com complexos à base de metais Fe e Co. Avanços recentes . Coord. Chem. Rev. 334, 184-198 | URL: https://www.researchgate.net/profile/Julien_Bonin/publication/308271980_Molecular_Catalysis_of_the_Electrochemical_and_Photochemical_Reduction_of_CO2_with_Fe_and_Co_Metal_Based_Complexes_Recent_Advances/links/5c0639fb299bf169ae3078e9/Molecular-Catalysis-of-the-Electrochemical-and-Photochemical-Reduction-of-CO2- with-Fe-and-Co-Metal-Based-Complexes-Recent-Advances.pdf
- Jhong HR.M, Ma S & Kenis PJA (2013) Conversão eletroquímica de CO 2a produtos químicos úteis: status atual, desafios restantes e oportunidades futuras . Curr. Opin. Chem. Eng. 2, 191-199 ( resumo )
- Aresta M, Dibenedetto A & Angelini A (2014) Catálise para a valorização do carbono de exaustão: do CO 2a produtos químicos, materiais e combustíveis . Uso tecnológico do CO2. Chem. Rev. 114, 1709-1742 ( resumo )
- Qiao J, Liu Y, Hong F e Zhang J (2014) Uma revisão dos catalisadores para a eletrredução de dióxido de carbono para produzir combustíveis de baixo carbono . Chem. Soc. Rev. 43, 631-675
- Parajuli R et al. (2015) Integração de catalisadores anódicos e catódicos de materiais abundantes na Terra para CO 2 eficiente e escalonávelredução . Topo. Catal. 58, 57-66
- Tatin A et al. (2016) Eletrolisador eficiente para CO 2divisão em água neutra usando materiais abundantes na Terra . Proc. Natl Acad. Sci. EUA 113, 5526–5529 | URL: https://www.pnas.org/content/pnas/113/20/5526.full.pdf
- Sahara G & Ishitani O (2015) Fotocatalisadores eficientes para CO 2redução . Inorg. Chem. 54, 5096–5104 | URL: https://pubs.acs.org/doi/full/10.1021/ic502675a
- Takeda H, Cometto C, Ishitani O & Robert M (2017) Elétrons, fótons, prótons e complexos de metais abundantes na Terra para catálise molecular de CO 2redução . ACS Catal. 7, 70-88 ( resumo )
- Shen, J. et al. (2015) Redução eletrocatalítica de dióxido de carbono em monóxido de carbono e metano em uma protoporfirina de cobalto imobilizada . Nat. Comum. 6, 8177 | URL: https://www.nature.com/articles/ncomms9177
- Weng Z et al. (2016) CO 2 eletroquímicoredução a hidrocarbonetos em um catalisador de Cu molecular heterogêneo em solução aquosa . J. Am. Chem. Soc. 138, 8076–8079 | URL: https://pdfs.semanticscholar.org/a69e/11c9a8e97716bdbd4a24aa5e687f447616fa.pdf .
- Manthiram K, Beberwyck BJ & Alivisatos AP (2014) Metanação eletroquímica aprimorada de dióxido de carbono com um catalisador de cobre em nanoescala dispersível . J. Am. Chem. Soc. 136, 13319-13325
- Xie MS et al. (URL: https://cloudfront.escholarship.org/dist/prd/content/qt4882v99t/qt4882v99t.pdf ) Eletrodos de cobre modificados com aminoácidos para a eletrorredução seletiva aprimorada de dióxido de carbono em hidrocarbonetos . Energia aprox. Sci. 9, 1687-1695 (2016)
- Wu T et al. (2014) Um fotocatalisador à base de carbono converte de maneira eficiente o CO 2para CH4 e C2H2 sob luz visível . Green Chem. 16, 2142-2146
- AlOtaibi B, Fan S, Wang D, Ye J & Mi Z (2016) Fotossíntese artificial de nível de wafer para CO 2redução em CH4 e CO usando nanofios de GaN . ACS Catal. 5, 5342-5348 ( resumo )
- Liu X, Inagaki S & Gong J (2016) Sistemas moleculares heterogêneos para CO 2 fotocatalíticoredução com oxidação da água . Angew. Chem. Int. Ed. 55, 14924-14950 ( resumo )
- Wang Y et al. (2016) Síntese fácil de uma etapa de nitreto de carbono grafítico híbrido e compostos de carbono como catalisadores de alto desempenho para CO 2conversão fotocatalítica . ACS Appl. Mater. Interf. 8, 17212-17219 ( resumo )
- Zhu, S. et al. (2016) Redução fotocatalítica de CO 2com H2O a CH4 sobre nanofolhas ultrafinas de SnNb2O6 2D sob irradiação de luz visível . Green Chem. 18, 1355–1363 | URL: https://www.researchgate.net/profile/Ling_Wu10/publication/283244219_Photocatalytic_reduction_of_CO_2_with_H_2_O_to_CH_4_over_ultrathin_SnNb_2_O_6_2D_nanosheets_under_visible_light_irradiation/links/569dcad408ae950bd7a6b275.pdf )
- Yu L et al. (2016) Aumento da atividade e estabilidade de nanobastões mesoporosos de óxido cuproso decorado com carbono para CO 2redução na fotossíntese artificial . ACS Catal. 6, 6444-6454 ( resumo )
- Azcarate I, Costentin C, Robert M & Savéant J.-M (2016) Um estudo de efeitos substitutos de interação de carga através do espaço na catálise molecular levando ao projeto do catalisador mais eficiente de conversão eletroquímica de CO2 em CO . J. Am. Chem. Soc. 138, 16639-16644
- Costentin C, Robert M, Savéant JM. & Tatin A (2015) Catalisador molecular eficiente e seletivo para a conversão eletroquímica de CO2 em CO em água . Proc. Natl Acad. Sci. USA 112, 6882-6886
- Heng Rao, Luciana C. Schmidt, Julien Bonin e Marc Robert (2018) “ Visible-light-driven methane training from CO 2com um catalisador molecular de ferro ”; Carta | 17 de julho de 2017 Nature volume 548, páginas 74–77 (03 de agosto de 2017) | URL: https://www.nature.com/articles/nature23016#ref2
- Li, X., Yu, J., Jaroniec, M., & Chen, X. (2019). Cocatalisadores para fotorredução seletiva de CO 2em combustíveis solares. Chemical reviews, 119 (6), 3962-4179. ( resumo )
- Zhang, B., & Sun, L. (2019). Fotossíntese artificial: oportunidades e desafios dos catalisadores moleculares . Chemical Society Reviews, 48 (7), 2216-2264.
- Andrei V, Reuillard B & Reisner E (2019) Produção de gás de síntese solar livre de polarização por meio da integração de um catalisador de cobalto molecular com perovskita - tandens BiVO 4 . Materiais da natureza, 1-6 ( resumo )
- Dalle KE, Warnan J, Leung JJ, Reuillard B, Karmel IS e Reisner E (2019) Síntese de combustível movida a energia elétrica e solar com complexos de metais de transição de primeira linha . Revisões químicas, 119 (4), 2752-2875 | URL: https://pubs.acs.org/doi/full/10.1021/acs.chemrev.8b00392 ( versão PDF )
Veja também
Bibliografia
- Gérard Borvon, História do carbono e CO 2. Da origem da vida às mudanças climáticas , Vuibert, 2013, 256 p.