ciclo de Krebs
O ciclo de Krebs , também chamado de ciclo do ácido cítrico pelo anglicismo é uma via metabólica presente em todos os organismos aeróbicos e cuja função primária é oxidar os grupos acetila , em particular a partir da degradação dos carboidratos , das gorduras e das proteínas , para recuperar energia em. a forma de oito elétrons de alto potencial e transferência de uma molécula de GTP ou ATP ; elétrons com alto potencial de transferência, recuperados de NADH e ubiquinol (CoQ 10 H 2ou coenzima Q 10 reduzido ), pode então circular através da cadeia respiratória para, por sua vez, permitir a formação de moléculas de ATP adicionais por fosforilação oxidativa .
Este ciclo foi descoberto em etapas na década de 1930 , vários de seus elementos foram identificados pelo biólogo molecular húngaro Albert Szent-Györgyi, enquanto seu funcionamento cíclico foi evidenciado pelo bioquímico alemão Hans Adolf Krebs em 1937. Ele se desdobra no citoplasma de procariotos e na mitocôndria de eucariotos . É um ciclo porque o último metabólito , o oxaloacetato , também está envolvido na primeira reação. O primeiro passo é transferir o grupo acetil do acetil-CoA para o oxaloacetato para formar o citrato , que deu ao anel seu nome nas línguas inglesa e germânica. As etapas a seguir formam uma sequência de reações, cada uma catalisada por uma enzima específica, que leva à oxidação gradual do grupo acetila em duas moléculas de dióxido de carbono (CO 2) Ao fazer isso, esse ciclo também produz precursores para a biossíntese de certos aminoácidos proteinogênicos , enquanto o NADH pode ser usado em um grande número de reações bioquímicas .
O ciclo de Krebs é o ponto final comum da degradação de poliolosídeos ( glicólise , via da pentose fosfato ), lipídeos ( β-oxidação ) e aminoácidos , que resultam na formação de acetil-CoA; o último é uma forma de transporte de grupos acetila do piruvato . Existem também reações de escape no ciclo que permitem várias biossínteses; o ciclo do glioxilato , ausente nos animais, mas presente em particular nas plantas , é um exemplo entre outros de tais vias metabólicas usando o ciclo de Krebs.
O fato de o ciclo de Krebs ser essencial para muitas vias metabólicas, tanto anabólicas quanto catabólicas , sugere que foi provavelmente um dos primeiros blocos de construção do metabolismo celular a ocorrer durante a evolução , possivelmente por abiogênese . Está relacionado a reações que ocorrem em bactérias anaeróbias e diz-se que evoluiu em vários estágios; Existem teoricamente várias alternativas para o ciclo de Krebs, mas o último parece ser o mais eficiente: se várias alternativas evoluíram independentemente, todas devem ter convergido para o ciclo de Krebs.
Etapas do ciclo de Krebs
A tabela abaixo resume os dez estágios do ciclo de Krebs, catalisados por oito enzimas diferentes. Essas etapas são notavelmente conservadas dependendo da espécie , mas as enzimas podem, por outro lado, diferir significativamente de um organismo para outro. As reações e enzimas mostradas nesta tabela são aquelas prevalentes em mamíferos .
| Substratos | Produtos | Enzima | Tipo de reação | Observações | |
|---|---|---|---|---|---|
| 1 |
Oxaloacetato + Acetil-CoA + H 2 O |
Citrato + CoA-SH |
Citrato sintase ( EC ) |
Crotonização | Irreversível, estende o oxaloacetato (4C) em uma molécula para seis átomos de carbono |
| 2 | Citrato |
cis -Aconitate + H 2 S |
Aconitase ( EC ) |
Desidratação | Isomerização reversível |
| 3 |
cis -Aconitate + H 2 S |
Isocitrato | Hidratação | ||
| 4 |
Isocitrato + NAD + |
Oxalosuccinato + NADH + H + |
Isocitrato desidrogenase ( EC ) |
Oxidação | Produto de NADH (equivalente a 2,5 ATP ) |
| 5 | Oxalosuccinato |
α-cetoglutarato + CO 2 |
Descarboxilação | Reação limitante, etapa irreversível, produzindo uma molécula com cinco átomos de carbono. |
|
| 6 |
α-cetoglutarato + NAD + + CoA-SH |
Succinil-CoA + NADH + H + + CO 2 |
Complexo de Α-cetoglutarato desidrogenase ( EC ) |
Descarboxilação oxidativa |
Etapa irreversível, produzindo NADH (equivalente a 2,5 ATP ), levando a uma molécula com quatro átomos de carbono (excluindo a coenzima A ) |
| 7 |
Succinil-CoA + GDP + P i |
Succinato + CoA-SH + GTP |
Succinil-CoA sintetase ( EC ) |
Fosforilação | ou ADP → ATP em vez de GDP → GTP, produz uma molécula de ATP ou equivalente A reação de condensação do GDP com o P i e a hidrólise do succinil-CoA envolve a molécula de H 2 O necessário para o equilíbrio da reação. |
| 8 |
Succinato + CoQ 10 |
Fumarato + CoQ 10 H 2 (ubiquinol) |
Succinato desidrogenase ( EC ) |
Oxidação | Usa FAD como um grupo protético (FAD → FADH 2na primeira fase da reação), equivalente a 1,5 ATP |
| 9 |
Fumarato + H 2 S |
L -Malato |
Fumarase ( EC ) |
Hidratação | |
| 10 |
L -Malato + NAD + |
Oxaloacetato + NADH + H + |
Malato desidrogenase ( EC ) |
Oxidação | Reversível (na realidade, o equilíbrio promove a formação de L- malato ), produto do NADH (equivalente a 2,5 ATP ) |
Síntese de citrato
A citrato sintase condensa o oxaloacetato e acetil CoA em citrato com liberação de CoA . Um intermediário transitório, citroil-CoA, é formado . A ligação tioéster da acetil-CoA é uma ligação com alto potencial de hidrólise . O acoplamento das atividades de hidrolase e sintase torna a reação de síntese termodinamicamente possível. Essa reação é uma etapa regulatória do ciclo, tendo succinil-CoA , NADH , acetil-CoA , citrato e ATP como efetores negativos na velocidade da reação .
|
|
+ Acetil-CoA + H 2 S → CoA + |

|
| Oxaloacetato | Citrato | |
| Citrato sintase - EC | ||
Desidratação de citrato
A aconitase , uma liase , catalisa a desidratação do citrato em cis- aconitado . Embora a molécula de citrato pareça ser simétrica, foi demonstrado que a saída da água ocorre entre os átomos de carbono derivados do oxaloacetato :

|
H 2 O + |
|
| Citrato | cis -Aconitate | |
| Aconitase - EC | ||
Hidratação de cis- aconitado
A aconitase também catalisa a hidratação do cis- aconitado em isocitrato :
|
|
+ H 2 S |

|
| cis -Aconitate | Isocitrato | |
| Aconitase - EC | ||
As duas etapas anteriores, catalisadas pela aconitase , levam à isomerização de citrato em isocitrato :

|
H 2 O + |
|

|
|
| Citrato | cis -Aconitate | Isocitrato | ||
| Aconitase - EC | ||||
Oxidação de isocitrato
A isocitrato desidrogenase , uma oxidorredutase , catalisa a oxidação do isocitrato em oxalosuccinato :

|
+ NAD + NADH + H + + |
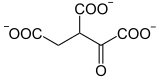
|
| Isocitrato | Oxalosuccinato | |
| Isocitrato desidrogenase - EC | ||
Os eucarióticos usam uma isocitrato desidrogenase NAD + -dependente ( EC ), que requer como cofator íons Mn 2+ ou Mg 2+ . Os próprios procariotos usam uma isocitrato desidrogenase NADP + -dependente ( EC ).
Descarboxilação de oxalosuccinato
A isocitrato desidrogenase catalisa também a descarboxilação do oxalosuccinato , volátil, α-cetoglutarato com evolução de CO 2, em uma reação irreversível:

|
→ CO 2 + |

|
| Oxalosuccinato | α-cetoglutarato | |
| Isocitrato desidrogenase - EC | ||
É também uma etapa regulatória do ciclo, com NADH e ATP como efetores negativos . A presença de ADP, ao contrário, promove a atividade da isocitrato desidrogenase e, portanto, a velocidade dessa reação.
Descarboxilação oxidativa de α-cetoglutarato
O complexo α-cetoglutarato desidrogenase catalisa a descarboxilação oxidativa do α-cetoglutarato em succinil-CoA com produção de NADH + H + e liberação de CO 2. É uma reação semelhante à conversão do piruvato em acetil-CoA , catalisada pelo complexo piruvato desidrogenase . Este complexo enzimático envolve sucessivamente três enzimas - α-cetoglutarato desidrogenase , diidrolipoamida S-succiniltransferase e diidrolipoil desidrogenase - e cinco cofatores : TPP , lipoamida , coenzima A , FAD e NAD + . Essa reação é irreversível.

|
+ CoA-SH + NAD + → NADH + H + + CO 2 + |
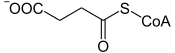
|
| α-cetoglutarato | Succinil-CoA | |
| Complexo de Α-cetoglutarato desidrogenase - EC | ||
O NADH , o GTP e a succinil-CoA são efetores negativos na atividade do complexo enzimático.
Formação de succinato
A sintetase succinil CoA ou succinato tioquinase , converte succinil CoA em succinato e coenzima A , formando uma molécula de GTP em animal ou ATP em plantas e bactérias . Esta reação é reversível.

|
+ GDP / ADP + Pi GTP / ATP + CoA + |
|
| Succinil-CoA | Succinato | |
| succinil-CoA sintetase (formando GTP / ATP) - EC / EC | ||
Oxidação de succinato
A succinato desidrogenase , uma oxidorredutase , catalisa a oxidação de succinato em fumarato com redução concomitante de ubiquinona ( coenzima Q 10) em ubiquinol (CoQ 10 H 2) Esta enzima flavoprotéique ao ADF é o complexo II da cadeia respiratória . É inibido pelo malonato . Como o FAD é um grupo protético covalentemente ligado à enzima, ele apenas transmite elétrons e prótons para o substrato CoQ 10 “real”..
|
|
+ FAD FADH 2 + |
|
| Succinato | Fumarate | |
| Succinato desidrogenase - EC | ||
Essa reação é a quarta e última reação regulatória do ciclo. Malonate é o inibidor competitivo aqui.
Hidratação de fumarato
A fumarase , uma liase, catalisa a hidratação do fumarato a L- malato .
|
|
+ H 2 S |

|
| Fumarate | L -Malato | |
| Fumarase - EC | ||
Oxidação do malato: fechando o ciclo
A malato desidrogenase , uma oxidorredutase , converte o L- malato em oxaloacetato com formação de NADH + H + .

|
+ NAD + NADH + H + + |
|
| L -Malato | Oxaloacetato | |
| Malato desidrogenase - EC | ||
Esta reação é catalisada por uma malato desidrogenase dependente de NAD + ( EC ) em eucariotos e dependente de quinona ( EC ) em procariotos .
Revisão do ciclo de Krebs
O ciclo de Krebs é composto de 10 etapas catalisadas por oito enzimas diferentes. Durante o ciclo são produzidos, de um mol de acetato até o estágio de CO 2e H 2 O :
- 2 moles de CO 2
- 3 moles de NADH + H +
- 1 mole de CoQ 10 H 2
- 1 mole de GTP
Pode-se observar que o ciclo de Krebs produz apenas um equivalente de ATP (um GTP ), ou seja, menos do que a glicólise (quatro moléculas de ATP para uma molécula de glicose , duas das quais são utilizadas durante a fase de "ativação" da glicólise. - etapas 1 e 3, que correspondem às fosforilações ). A maior parte da energia química potencial é produzida na forma de poder redutor ( NADH + H + e CoQ 10 H 2) Esse poder redutor é subsequentemente usado na cadeia respiratória da mitocôndria para produzir 11 outras moléculas de ATP por meio de um gradiente de prótons e ATP sintase, que às vezes é erroneamente atribuído ao ciclo de Krebs.
| Descrição | Substratos | Produtos |
| A soma de todas as reações de oxidação da acetil-CoA pelo ciclo de Krebs (excluindo a cadeia respiratória ) corresponde a: | Acetil-CoA + 3 NAD + + CoQ 10 + PIB + P i + 2 H 2 O | → CoA-SH + 3 (NADH + H + ) + CoQ 10 H 2 + GTP + 2 CO 2 |
| Voltando à descarboxilação do piruvato , os resultados são: | Piruvato + 4 NAD + + CoQ 10 + PIB + P i + 2 H 2 O | → 4 (NADH + H + ) + CoQ 10 H 2 + GTP + 3 CO 2 |
| Voltando à oxidação da glicose pela glicólise , os resultados são: | Glicose + 10 NAD + + 2 CoQ 10+ 2 ADP + 2 PIB + 4 P i + 2 H 2 O | → 10 (NADH + H + ) + 2 CoQ 10 H 2 + 2 ATP + 2 GTP + 6 CO 2 |
Isso corresponde, no total, para toda a respiração aeróbica ( glicólise , ciclo de Krebs, redução das coenzimas NAD + e CoQ 10pela cadeia respiratória ) entre 30 e 38 ATP para uma molécula de glicose estimada, dependendo em parte da lançadeira mitocondrial dependente de ATP usada para transportar NAD + da glicólise.
O uso de glicose por meio da respiração aeróbica é mais enérgico do que a fermentação .
Na presença de uma grande quantidade de acetil-CoA , o ciclo de Krebs pode ser sobrecarregado, especialmente em diabéticos com deficiência grave de insulina ou após jejum prolongado (ver cetoacidose diabética para mais detalhes).
Variações
Embora o ciclo de Krebs seja geralmente muito conservado entre as espécies, existem variações significativas nas enzimas presentes nos diferentes taxa . Em particular, existem diferenças entre procariotos e eucariotos . Assim, a conversão de D - treo- isocitrato em α-cetoglutarato é catalisada por uma isocitrato desidrogenase dependente de NAD + ( EC ) em eucariotos, mas dependente de NADP + ( EC ) em procariotos. O mesmo é verdadeiro para a conversão de L- malato em oxaloacetato , catalisada por uma malato desidrogenase dependente de NAD + ( EC ) em eucariotos e quinona dependente ( EC ) em procariotos.
A conversão de succinil-CoA em succinato pela succinil-CoA sintetase exibe uma variabilidade significativa. A maioria dos seres vivos usar um ADP- dependente enzima ( EC ), enquanto mamíferos também usam o GDP dependente isoforma ( CE ) desta enzima. A taxa de uso de cada uma dessas duas formas da enzima depende dos tecidos considerados. Em certas bactérias produtoras de acetato , como Acetobacter aceti (en) , é uma enzima totalmente diferente que catalisa esta reação, neste caso succinil-CoA: acetato de CoA-transferase ( EC ): esta enzima realiza a junção do ácido acético metabolismo ácido com o ciclo de Krebs nesses organismos. Algumas bactérias, como o Helicobacter pylori, usam uma enzima ainda diferente para essa reação, neste caso a 3-oxoácido CoA-transferase ( EC ).
Também existe alguma variabilidade na etapa anterior, ou seja, na conversão de α-cetoglutarato em succinly-CoA . A maioria dos seres vivos usa o complexo α-cetoglutarato desidrogenase , mas algumas bactérias usam α-cetoglutarato sintase ( EC ). Outros organismos, incluindo bactérias e arquéias autotróficas e metanotróficas obrigatórias contornam completamente o succinil-CoA e convertem α-cetoglutarato em succinato por meio do semialdeído succínico pela ação sucessiva da α-cetoglutarato descarboxilase ( EC ) e succinato-semialdeído desidrogenase ( EC ).
Regulamento
Os estágios irreversíveis do ciclo de Krebs podem ser regulados: estágio da citrato sintase , isocitrato desidrogenase e complexo α-cetoglutarato desidrogenase :
- a citrato sintase é ativada pelo ADP, mas inibida pelo NADH , o ATP e o citrato . Portanto, é inibido respectivamente pelo poder redutor, pela carga de energia e pelo produto de reação que catalisa.
- a isocitrato desidrogenase é ativada por cálcio e ADP , e é inibida por NADH e ATP .
- o complexo α-cetoglutarato desidrogenase é ativado pelo cálcio e inibido pelo NADH , ATP e seu produto de reação, a succinil-CoA .
A regulação do ciclo de Krebs depende principalmente da disponibilidade do substrato e da inibição pelos produtos da reação. Se essas reações não fossem reguladas, o ciclo de Krebs desperdiçaria grandes quantidades de energia metabólica, produzindo ATP em excesso e coenzimas reduzidas como o NADH .
- O NADH é produzido por todas as desidrogenases do ciclo, exceto a succinato desidrogenase e tem o efeito de inibir o complexo piruvato desidrogenase , isocitrato desidrogenase , o complexo α-cetoglutarato desidrogenase, bem como citrato sintase .
- O acetil-CoA inibe o complexo piruvato desidrogenase, enquanto o succinil-CoA inibe o complexo α-cetoglutarato desidrogenase e citrato sintase . Os testes in vitro das enzimas do ciclo de Krebs mostram que o ATP inibe a citrato sintase e o complexo α-cetoglutarato desidrogenase; no entanto, o nível de ATP in vivo não varia em mais de 10% entre os períodos de repouso e atividade sustentada, e nenhum mecanismo alostérico conhecido permite modular significativamente a atividade de uma enzima com uma variação de no máximo 10% da concentração de um efetor alostérico.
- O cátion de cálcio Ca 2+ atua como regulador. O nível de cálcio na matriz mitocondrial pode atingir algumas dezenas de micromoles por litro . Ativa a piruvato desidrogenase fosfatase , que por sua vez ativa o componente piruvato desidrogenase (E1) do complexo piruvato desidrogenase. Também ativa a isocitrato desidrogenase e o complexo α-cetoglutarato desidrogenase. Isso aumenta a taxa de reação de vários estágios do ciclo e, portanto, aumenta o fluxo de compostos por essa via metabólica .
- O Citrato actua inibindo a fosfofrutoquinase , a qual está envolvida na glicólise e, assim, contribui para a formação de piruvato via da frutose-1,6-bisfosfato . Isso forma um ciclo de feedback entre as duas vias metabólicas.
Trabalho publicado em 2007 mostrou uma ligação importante entre os intermediários do ciclo de Krebs e a regulação de fatores induzidos por hipóxia ( HIF ). Desempenham um papel na homeostase do oxigênio como fatores de transcrição envolvidos na angiogênese , remodelação vascular, mobilização de glicose , transporte de íons e apoptose . Os HIF são sintetizados constitutivamente e a hidroxilação de pelo menos um dos dois resíduos de prolina está envolvida em sua interação com a ubiquitina ligase complexa , que os designa como um alvo para degradação rápida. Essa reação é catalisada por dioxigenases pró-colágeno-prolina . Tanto o fumarato quanto o succinato são inibidores eficazes dessas enzimas, que podem estabilizar os HIFs.
Integração com as principais vias metabólicas
Vias anaplerótica e cataplerótica
Várias vias metabólicas convergem no ciclo de Krebs. A maioria dessas reações produz metabólitos que participam do ciclo e, portanto, são reações anapleróticas ; processos que, por outro lado, consomem metabólitos do ciclo de Krebs são considerados catapleróticos.
Todos os intermediários no ciclo de Krebs - como citrato , isocitrato , α-cetoglutarato , succinato , fumarato , L- malato e oxaloacetato - são regenerados a cada volta do ciclo. O aumento da quantidade disponível de um desses metabólitos aumenta a quantidade total de todos os metabólitos do ciclo, pois cada intermediário é gradualmente convertido em todos os outros intermediários do ciclo. Esta é a razão pela qual a produção de qualquer um dos metabólitos do ciclo de Krebs tem um efeito anaplerótico geral naquele ciclo, enquanto o consumo de qualquer um dos metabólitos tem um efeito cataplerótico em todo o ciclo.
As moléculas de piruvato resultantes da glicólise são transportadas ativamente do citosol para a matriz mitocondrial através da membrana mitocondrial interna . Uma vez na matriz, eles podem ser oxidados e reagir com a coenzima A para formar CO 2, acetil-CoA e NADH , ou podem ser carboxilados pela piruvato carboxilase para formar oxaloacetato . Esta é uma reação anaplerótica que aumenta o fluxo e, portanto, o fluxo através do ciclo de Krebs quando a célula se depara com um aumento da necessidade de energia metabólica, por exemplo nos miócitos .
Alimentando o ciclo com acetil-CoA
A acetil-CoA , entretanto, derivada da oxidação do piruvato ou da β-oxidação dos ácidos graxos , nunca é regenerada pelo ciclo de Krebs: ao contrário, cada volta do ciclo consome uma molécula de acetil-CoA por molécula de oxaloacetato da matriz mitocondrial, enquanto o acetil resíduo de acetil-CoA é totalmente oxidado para CO 2e em H 2 Oatravés da cadeia respiratória , permitindo que a energia metabólica seja recuperada na forma de ATP por fosforilação oxidativa .
As vias metabólicas que produzem ou consomem acetil-CoA, portanto, não são anapleróticas ou catapleróticas para o ciclo de Krebs.
Gliconeogênese
No fígado, a carboxilação do piruvato citosólico em oxaloacetato mitocondrial é uma etapa avançada na gliconeogênese , que converte lactato e alanina desaminada em glicose sob o efeito de um nível elevado de glucagon e / ou adrenalina no sangue . Nessas condições, a formação de oxaloacetato na mitocôndria não apresenta efeito anaplerótico porque o L -malato mitocondrial é consumido para formar oxaloacetato citosólico, que é convertido em glicose.
Degradação de proteínas
No processo de degradação de proteínas , as cadeias polipeptídicas são clivadas por peptidases nos aminoácidos que as constituem. Sua cadeia de carbono pode então:
- introduzir o ciclo de Krebs - como é por exemplo o caso de glutamato e glutamina que entram na forma de α-cetoglutarato - que apresenta uma anaplerótica efeito - falamos de glucoforming amino ácidos , porque eles podem ser orientadas para a gluconeogénese via o G -malato ;
- ser convertido em acetil-CoA para ser oxidado e produzir energia, como é o caso da leucina , isoleucina , lisina , fenilalanina , triptofano e tirosina ;
- podem ser convertidos em corpos cetônicos , capazes de ser oxidados por tecidos diferentes do fígado onde são produzidos, ou excretados pela urina ou pela respiração - são chamados de aminoácidos cetoformadores .
Degradação de lipídios
No processo de lipólise , os triglicerídeos são hidrolisados em glicerol e ácidos graxos . No fígado , o glicerol pode ser convertido em glicose através da di-hidroxiacetona fosfato e gliceraldeído-3-fosfato no contexto da gluconeogénese . Em muitos tecidos , especialmente no coração e nos músculos esqueléticos , os ácidos graxos são degradados por meio da β-oxidação , que produz acetil-CoA mitocondrial capaz de ingressar no ciclo de Krebs. Ácidos graxos com um número ímpar de átomos de carbono produzem propionil-CoA , que é convertido em succinil-CoA e se junta ao intermediário do ciclo de Krebs como anaplerótico.
Metabólitos usados como substratos para biossíntese
Vários metabólitos do ciclo de Krebs estão envolvidos na biossíntese de compostos importantes, apresentando um efeito cataplerótico significativo no ciclo.
Produção de carboidratos e lipídios
Como o acetil-CoA não pode deixar a mitocôndria como está , é o citrato que é transportado através da membrana mitocondrial interna da matriz mitocondrial para o citosol , onde é clivado em acetil-CoA e oxaloacetato pela ATP citrato liase . O oxaloacetato pode ser usado para a gliconeogênese no fígado ou pode ser convertido em L- malato e se juntar à mitocôndria. O acetil-CoA citosólico é usado para a biossíntese de ácidos graxos e colesterol . Este último pode, por sua vez, ser usadas para produzir hormonas esteróides , os ácidos biliares e vitamina D .
Durante a gliconeogênese , o oxaloacetato mitocondrial é reduzido a malato , que é subsequentemente transportado para fora da mitocôndria para ser novamente oxidado a oxaloacetato no citosol . Este último é então descarboxilado em fosfoenolpiruvato pela fosfoenolpiruvato carboxicinase , que é a etapa cineticamente determinante na conversão em glicose de praticamente todos os precursores da glucoformação - como os aminoácidos glucoformadores e lactato - pelo fígado e rins .
Produção de aminoácidos
A cadeia de carbono de muitos aminoácidos não essenciais se origina de metabólitos do ciclo de Krebs. O aspartato e a asparagina são derivados do oxaloacetato , enquanto a glutamina , a prolina e a arginina derivam do α-cetoglutarato . O grupo amina vem do glutamato por transaminação em um α-cetoácido usando enzimas usando fosfato de piridoxal como cofator ; durante essas reações, o glutamato é convertido em α-cetoglutarato, que é um metabólito do ciclo de Krebs.
Produção de bases de ácido nucleico
O aspartato e a glutamina estão envolvidos também na biossíntese de nucleobases purinas que entram na composição do ácido nucléico - DNA e RNA - bem como de nucleotídeos como o ATP , o AMP cíclico , o NAD , o ADF e CoA . As bases nucleicas da pirimidina , por sua vez, são derivadas do aspartato , ele próprio derivado do oxaloacetato .
Produção de porfirinas
A maioria dos átomos de carbono nas porfirinas vem do succinil-CoA , um metabólito do ciclo de Krebs. Porfirinas são os grupos prostéticos de hemoproteínas , como hemoglobina , mioglobina e citocromos .
Notas e referências
- (em) " O Prêmio Nobel de Fisiologia ou Medicina 1937: Albert Szent-Györgyi " , 1937(acessado em 7 de novembro de 2015 ) : " O Prêmio Nobel de Fisiologia ou Medicina de 1937 foi concedido a Albert Szent-Györgyi" por suas descobertas relacionadas aos processos de combustão biológica, com especial referência à vitamina C e à catálise do ácido fumárico ". " .
- (em) " O Prêmio Nobel de Fisiologia ou Medicina 1953: Hans Krebs, Fritz Lipmann " (acessado em 7 de novembro de 2015 ) : " O Prêmio Nobel de Fisiologia ou Medicina de 1953 foi dividido igualmente entre Hans Adolf Krebs" Por sua descoberta do cítrico ciclo do ácido "e Fritz Albert Lipmann" por sua descoberta da coenzima A e sua importância para o metabolismo intermediário ". " .
- (em) H. Gest , " raízes evolutivas do ciclo do ácido cítrico em procariotos " , Biochemical Society Symposium , vol. 54, 1987, p. 3-16 ( PMID 3332996 )
- (in) Enrique Meléndez-Hevia, Thomas G. Waddell e Marta Cascante , " O quebra-cabeça do ciclo do ácido cítrico de Krebs: Montando as peças de reações quimicamente viáveis e oportunismo no projeto de vias metabólicas durante a evolução " , Journal of Molecular Evolution , vol. 43, n o 1, Setembro de 1996, p. 293-303 ( PMID 8703096 , DOI 10.1007 / BF02338838 , ler online )
- (em) Oliver Ebenhöh e Reinhart Heinrich , " Evolutionary Optimization of Metabolic Pathways. Reconstrução Teórica da Estequiometria dos Sistemas de Produção de ATP e NADH ” , Bulletin of Mathematical Biology , vol. 63, n o 1, Janeiro de 2001, p. 21-55 ( PMID 11146883 , DOI 10.1006 / bulm.2000.0197 , ler online )
- (em) Takehiko SARA, Yasuhiro Takada, Yoji Takeuchi Naoto Yamaoka e Noriyuki Fukunaga , " Cloning, A sequenciação e expressão de um gene que codifica a monomérico Isocitrato Desidrogenase do Bactéria Azoto-fixa, Azotobacter vinelandii " , Bioscience, Biotechnology e Biochemistry , vol. 66, n o 3, Março de 2002, p. 489-500 ( PMID 12005040 , DOI 10.1271 / bbb.66.489 , ler online )
- (en) Michel E. van der Rest, Christian Frank e Douwe Molenaar , “ Functions of the Membrane-Associated and Cytoplasmic Malate Dehydrogenases in the Citric Acid Cycle of Escherichia coli ” , Journal of bacteriology , vol. 182, n o 24, dezembro de 2000, p. 6892-6899 ( PMID 11092847 , PMCID 94812 , DOI 10.1128 / JB.182.24.6892-6899.2000 , ler online )
- (in) RK Porter e MD Brand , " condutância Mitocondrial próton e H + / O proporções são independentes da taxa de transporte de elétrons em hepatócitos isolados " , Biochemical Journal , vol. 310, 1995, p. 379-382 ( ler online )
- (em) David O. Lambeth, Kristin N. Tews, Steven Adkins, Dean Frohlich e Barry I. Milavetz , " Expression of Two succinyl-CoA Synthetases with Different Specificities Nucleotide in Mammalian Tissues " , Journal of Biological Chemistry , vol. 279, n o 35, 27 de agosto de 2004, p. 36621-36624 ( PMID 15234968 , DOI 10.1074 / jbc.M406884200 , leia online )
- (em) Elwood A. Mullins, Julie A. Francois e Joseph T. Kappock , " A Specialized Citric Acid Cycle Requiring succinyl-coenzyme A (CoA): Acetate CoA transferase (AARC) Confers Resistance Acid Acid on the acidophilus Acetobacter aceti " , Journal of Bacteriology , vol. 190, n o 14, julho de 2008, p. 4933-4940 ( PMID 18502856 , PMCID 2447011 , DOI 10.1128 / JB.00405-08 , ler online )
- (em) Irene E. Corthésy-Theulaz Gabriela E. Bergonzelli, Henry Hughes, Daniel Bachmann Daniel F. Schorderet Andre L. Blum e Nicholas L. Ornston , " Cloning and Characterization of Helicobacter pylori succinyl CoA: acetoacetato CoA transferase, a Novel Prokaryotic Member of the CoA-transferase Family ” , Journal of Biological Chemistry , vol. 272, n o 41, 10 de outubro de 1997, p. 25659-25667 ( PMID 9325289 , DOI 10.1074 / jbc.272.41.25659 , ler online )
- (em) Anthony D. Baughn, Scott J. Garforth, Vilchèze Catherine e William R. Jacobs Jr. , " An Anaerobic-type α-Ketoglutarate ferredoxin oxidoreductase Completes the Oxidative tricarboxylic Acid Cycle of Mycobacterium tuberculosis " , PLoS Pathogens , vol. 5, n o 11, novembro de 2009, e1000662 ( PMID 19936047 , PMCID 2773412 , DOI 10.1371 / journal.ppat.1000662 , ler online )
- (em) Shuyi Zhang e Donald A. Bryant , " The tricarboxylic Acid Cycle in Cyanobacteria " , Science , vol. 334, n o 6062, 16 de dezembro de 2011, p. 1551-1553 ( PMID 22174252 , DOI 10.1126 / science.1210858 , ler online )
- (em) Maxim V. Ivannikov e Gregory T. Macleod , " Mitocondrial Free Ca2 + Levels and their Effects on Energy Metabolism in Drosophila Motor Nerve Terminals " , Biophysical Journal , Vol. 104, n o 11, 4 de junho de 2013, p. 2353-2361 ( PMID 23746507 , PMCID 3672877 , DOI 10.1016 / j.bpj.2013.03.064 , ler online )
- (em) Richard Denton, Philip J. Randle, Barbara J. Bridges, Ronald H. Cooper, Alan L. Kerbey Helen T. Pask, David L. Severson, David e Susan Whitehouse Stansbie , " Regulamento da piruvato desidrogenase de mamíferos " , Molecular and Cellular Biochemistry , vol. 9, n o 1, Outubro de 1975, p. 27-53 ( PMID 171557 , DOI 10.1007 / BF01731731 , leia online )
- (en) Inibição do fator indutível por hipóxia (HIF) hidroxilases por intermediários do ciclo do ácido cítrico. POSSÍVEIS LINKS ENTRE METABOLISMO CELULAR E ESTABILIZAÇÃO DE HIF , “ Peppi Koivunen, Maija Hirsilä, Anne M. Remes, Ilmo E. Hassinen, Kari I. Kivirikko e Johanna Myllyharju ” , Journal of Biological Chemistry , vol. 282, n o 7, 16 de fevereiro de 2007, p. 4524-4532 ( PMID 17182618 , DOI 10.1074 / jbc.M610415200 , leia online )
- (em) Premjit P. Halarnkar e Gary J. Blomquist , " Comparative aspect of propionate metabolism " , Comparative Biochemistry and Physiology Part B: Comparative Biochemistry , vol. 92, n o 2 1989, p. 227-231 ( PMID 2647392 , DOI 10.1016 / 0305-0491 (89) 90270-8 , ler online )
Veja também
Artigos relacionados
- Cadeia respiratória : o futuro do NADH, H +
- Respiração celular
- Glicolise
- As principais vias do metabolismo (em wikibooks)
- Hans Adolf Krebs
- Ciclo de Calvin , cloroplasto : reações bioquímicas da fotossíntese
