Organomagnésio
Um organomagnésio é um composto orgânico com uma ligação carbono - magnésio . Esta é uma importante família de compostos organometálicos em síntese orgânica porque inclui os reagentes de Grignard , que são organomagnésio mistos da forma R - Mg X , onde R é uma cadeia de carbono e X é um halogênio , geralmente bromo. Ou cloro , às vezes iodo - flúor geralmente não é usado devido à polarizabilidade muito baixa do difluor F 2. Estes reagentes são amplamente utilizados na indústria e sua descoberta no final do XIX ° século pelo químico francês Victor Grignard lhe permitiu obter o Prêmio Nobel de Química em 1912, porque eles podem se ligar uma grande variedade de blocos de construção para de moléculas orgânicas.
Além dos reagentes de Grignard, os compostos de organomagnésio incluem moléculas como dimetilmagnésio (CH 3 ) 2 Mg, dibutilmagnésio (CH 3 CH 2 CH 2 CH 2 ) 2 Mgou antraceno-magnésio .
Caráter organometálico de R - Mg - X
O carbono tem uma electronegatividade forte: . E também notamos isso . Portanto, este fato físico impõe a polarização do C - M: C -M ligação . Notamos uma inversão da polaridade das ligações clássicas de carbono: em um organometálico, o carbono carrega uma carga (este carbono é chamado de carbanião), além disso esta ligação é 35% iônica, o que permitirá por reação, por exemplo, um haleto alquil ( R —X ) criando uma ligação carbono-carbono .
Os organomagnésio são uma das bases de Brönsted mais fortes na química orgânica, com um pKa da ordem de 40 a 60. R-Mg-X é um nucleófilo poderoso.
Síntese de organomagnésio
Devido à sua extrema basicidade, o organomagnésio não existe naturalmente. Os resultados gerais da síntese são os seguintes:
Modo operacional
A síntese do organomagnésio é delicada: o meio de reação deve ser anidro, devido às propriedades do produto desejado; a reação é fortemente exotérmica e o solvente é volátil e inflamável. O manuseio inadequado também resulta na criação de um produto parasita - chamado “ Wurtz Coupling ”.
Materiais necessários :
- Bola tricolor;
- Funil de fundição isobárico;
- Condensador de refluxo;
- Mantém CaCl 2 (ou trabalha sob uma atmosfera inerte);
- Agitador magnético com aquecimento;
- Lascas de magnésio;
- Éter dietílico ou THF anidro;
- Derivado halogenado;
- Banho-maria e depois água fria.
Modo operacional
- Realizar uma montagem de adição com refluxo, com proteção do meio reacional contra a umidade atmosférica, e colocando uma barra magnética ovóide no frasco de três gargalos.
- Deite no tricol as aparas de magnésio previamente activadas no forno. Cubra-os com alguns cm 3 de éter etílico anidro. Adicione um pequeno cristal de diodo.
- Condicionar o funil de vazamento com a solução do derivado halogenado em éter etílico anidro e tapar com uma rolha de vidro.
- Despeje algumas gotas da solução de haleto nas aparas de magnésio, espere alguns minutos para a observação de uma descoloração ocorrendo no meio de reação.
- Quando a cor do iodo tiver desaparecido no meio reacional, aqueça em banho-maria para estabelecer o refluxo e despeje o halogeneto lentamente e gota a gota agitando magneticamente.
- Uma vez que a adição esteja completa, aqueça o meio de reação ao refluxo para obter uma reação completa.
Comentários
Para evitar que ocorra um acoplamento de Würtz entre o organomagnésio sintetizado e o haleto. Desde o início da reação, o éter ferve: o refluxo serve para condensar os vapores de éter que fluem no frasco; o refluxo também deve ser mantido muito baixo, para não criar a reação parasitária mencionada acima. Não é necessário aquecer durante a manipulação porque a reação é muito exotérmica .
A solução finalmente obtida é de uma cor acinzentada bastante clara, em geral.
Solvente
O éter desempenha um papel duplo aqui, ele solvata o organomagnésio formado e o estabiliza, o organomagnésio aqui é um ácido de Lewis, o solvente aqui desempenha o papel de base de Lewis , portanto, os dupletos não-ligantes de oxigênio vão para estabilizar o centro reativo de magnésio . É possível, por exemplo, usar éter dietílico , ou então THF - tetrahidrofurano , cf. figura abaixo.

O ambiente em que o organomagnésio é banhado deve ser completamente anidro: a reação água / RMgX é viva.
Reatividade do organomagnésio
Reações em compostos orgânicos usuais
Na águaA reação dos organomagnésio na água é muito viva (é uma reação ácido-base : p K a (RH / R-) = 50) e exotérmica. É por isso que o modo de operação requer desidratação total do ar na vidraria, bem como das superfícies e solventes. Exceto em casos especiais, essa reação é considerada parasitária e leva à destruição do organomagnésio.
A reação do organomagnésio na água é a seguinte:
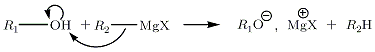 Com ácidos carboxílicos
Com ácidos carboxílicos
 Com aminas
Com aminas
 Com alcinos terminais
Com alcinos terminais

Reações de substituição nucleofílica
Substituição nucleofílica, exemplo de I 2Propomos a substituição nucleofílica de RMgX em I 2 (a polaridade desta molécula é induzida).
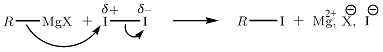 Substituição nucleofílica com derivados halogenados
Substituição nucleofílica com derivados halogenados
Derivado halogenado: mecanismo R'-X: SN2
R-MgX + R'-X -> RR '+ MgX2
Nota: funciona bem com RI e Ar-CH2X, pois são estabilizados por efeito indutivo para RI e mesômero para Ar-CH2X
Reação em epóxisMecanismo: SN2
No éter:
R ---- Mg ---- X + O (CH2) 2 (ciclo) → R-CH2-CH2-O-Mg-X
Então H3O + hidrólise ácida:
R-CH2-CH2-O-Mg-X + H + → R-CH2-CH2-OH + MgX +
Reações de adição nucleofílica ...
... em aldeídos e cetonas- Em aldeídos :

A reação entre o organomagnésio e os aldeídos leva à formação de um álcool secundário, se as cadeias R 1 e R 2 contiverem pelo menos um carbono. Se o carbono de suporte do grupo álcool final for assimétrico, isto é, se as duas cadeias R forem diferentes, o produto será composto pelos dois isômeros de configuração R e S.
- Em cetonas :

Essa reação leva à criação de um álcool terciário. Quanto aos aldeídos, se o carbono formado for assimétrico, obtém-se uma mistura R / S 50/50; portanto, não há estereosseletividade. Um estudo do mecanismo de reação mostra que de fato existe um intermediário cíclico:

- Caso especial da síntese de um álcool primário :
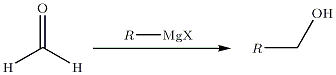 ... em ésteres
... em ésteres
A reação é semelhante à reação em uma cetona. Após a hidrólise, obtemos o hemiacetal de forma intermediária ;
Este é instável, ele sofre eliminação levando a uma cetona. O organomagnésio presente reagirá quimiosseletivamente com a cetona antes do éster, que é menos reativo porque o núcleo de carbono de sua carbonila é um tanto mascarado pelos elétrons não ligados do oxigênio ligados por uma única ligação. A avaliação geral da reação leva, portanto, à formação de um álcool terciário, sem a possibilidade de isolar a cetona intermediária.
... em cloretos de acilaA reação é semelhante à reação em uma cetona, mas mais rápida porque o núcleo de carbono ligado ao cloro mostra uma carga positiva mais atraente para o radical organomagnésio.
R ---- Mg ---- X + R'-CO-Cl → R'-CO-R + Cl-Mg-X
A reação, portanto, leva à formação de uma cetona isolável se não houver muito organomagnésio. Esta cetona instável irá reagir com o agente organomagnésio que está no meio reacional de acordo com a seguinte reação: R'-CO-R + RMgX → R-R'COMgX-R e então sob a ação de H2O obtemos um álcool terciário. Se quisermos parar no estágio de cetona, devemos operar a −65 ° C
... em CO 2
Usando o dióxido de carbono na forma de gelo seco . A reação a -40 ° C leva à formação de um ácido carboxílico R-COOH.
Notas e referências
- Victor Grignard , " Sobre algumas novas combinações organometálicas de magnésio e sua aplicação às sínteses de álcoois e hidrocarbonetos ", Relatórios semanais das sessões da Académie des sciences , vol. 130, 1900, p. 1322-1325 ( ler online )
- (em) " O Prêmio Nobel de Química em 1912 " (acessado em 27 de outubro de 2018 ) .




