Lactato desidrogenase
lactato desidrogenase Estrutura da lactato desidrogenase muscular mostrando as quatro subunidades
Estrutura da lactato desidrogenase muscular mostrando as quatro subunidades
| EC No. | EC |
|---|---|
| Número CAS |
| IUBMB | Entrada IUBMB |
|---|---|
| IntEnz | Vista IntEnz |
| BRENDA | Entrada BRENDA |
| KEGG | Entrada KEGG |
| MetaCyc | Via metabólica |
| PRIAM | Perfil |
| PDB | Estruturas |
| VAI | AmiGO / EGO |
A lactato desidrogenase ( LDH ) ou desidrogenases lácticas são enzimas encontradas em uma ampla diversidade de organismos, tanto plantas quanto animais. Eles catalisam a conversão de piruvato em lactato e vice-versa. Existem vários tipos dessas enzimas, que diferem de acordo com a natureza do cofator da reação e do estereoisômero do lactato formado. O lactato de fato possui dois isômeros D e L e existem lactato desidrogenases capazes de formar um ou outro dos produtos.
O cofator mais comum das lactato desidrogenases é o NADH, que é convertido em NAD + . Esta conversão é a reação básica da fermentação láctica que possibilita a regeneração do NAD + no final da glicólise. Está envolvida em um grande número de biotransformações por microrganismos e bactérias lácticas. Certas lactato desidrogenases também podem usar NADPH , ou mesmo outros cofatores, como o citocromo c .
Em mamíferos, apenas a NADH lactato desidrogenase é encontrada, que produz L-lactato ( EC 1.1.1.27 ). Também é capaz de catalisar a oxidação de 2-hidroxibutirato e, portanto, ocasionalmente também é referido como Hidroxibutirato desidrogenase ( HBD ).
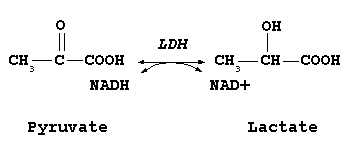
Este artigo enfoca as lactato desidrogenases da última família (EC 1.1.1.27)
Iso-enzimas
A NADH L-lactato desidrogenase é uma enzima tetramérica. Em mamíferos, cada subunidade pode ser Tipo H (inglês h eart = heart ) ou M ( m uscle ) (com base em seu comportamento eletroforético ). Dependendo do tipo de junta formada devem, portanto, cinco isotipos de LDH:
- LDH-1 (4H) - principalmente no coração
- LDH-2 (3H1M) - principalmente no sistema reticuloendotelial
- LDH-3 (2H2M) - principalmente nos pulmões
- LDH-4 (1H3M) - principalmente nos rins
- LDH-5 (4M) - principalmente no fígado e músculos esqueléticos
Em geral, a forma predominante no soro é a LDH-2. Um nível mais alto de LDH-1 do que LDH-2 sugere um infarto do miocárdio (dano ao tecido cardíaco que libera LDH cardíaco, que é rico em LDH-1, na corrente sanguínea). No entanto, o diagnóstico de infarto com base nesse fenômeno foi amplamente substituído pela medição dos níveis de troponina I ou T.
Genética humana
As subunidades H e M são codificadas por dois genes diferentes:
- A subunidade é codificada por M LDHA , localizada no cromossomo 11p15.4 ( (in) 150000 )
- A subunidade H é codificada por LDHB , localizada no cromossomo 12p12.2-p12.1 ( (en) 150100 )
Mutações
- Mutações na subunidade M foram correlacionadas a uma doença rara, mioglobinúria de estresse (ver artigo OMIM )
- Algumas mutações da subunidade H foram descritas, mas não parecem causar doença.
Aspectos médicos
Hemólise
Na medicina , o LDH é freqüentemente usado como um marcador de danos aos tecidos. Como o LDH é abundante nas células vermelhas do sangue , ele pode servir como um marcador de hemólise . Uma amostra de sangue que foi processada incorretamente pode ter atividades de LDH elevadas falso-positivas devido a danos nos eritrócitos .
Rotatividade de tecidos
Outras aplicações do ensaio de atividade de LDH referem - se à destruição de tecidos em geral; isso é possível se não houver outros sinais de hemólise . É usado para monitorar pacientes com câncer (especialmente em casos de linfoma ou câncer testicular ): como as células cancerosas são renovadas rapidamente, sua destruição leva a um alto nível de LDH.
Valor normal
- Valor normal da concentração plasmática de LDH: 190-390 IU / L
- 125-220 U / L em teste de sangue (teste ABBOTT de piruvato 37 ° C)