Transplante de medula óssea
O transplante de medula óssea é um transplante de transferência de medula óssea de um indivíduo para outro que sofre de uma patologia em seu cordão. Às vezes, é a única maneira de se recuperar.
Permite o uso de quimioterapia e / ou radioterapia em doses massivas que resulta na melhora da sobrevida ou mesmo considerando a cura em alguns casos e aproveitando o enxerto contra efeito tumoral (pelos linfócitos T do doador). Estes tratamentos são de facto muito tóxicos para as células sanguíneas e o transplante permite a reconstrução e regeneração da medula óssea e a manutenção da produção normal dessas células.
Esse transplante, como o de rim ou sangue, é possível graças a um doador vivo que doa seu órgão na maioria dos casos. Em alguns países, o doador recebe compensação; isso é ilegal na França devido ao princípio da não patrimonialidade do corpo humano .
Existem dois tipos de enxertos:
- o aloenxerto da medula óssea, medular usa um enxerto obtido de um doador saudável para ser HLA idêntico ao do receptor.
- a medula óssea autóloga , usa medula própria do paciente.
Histórico
Os primeiros experimentos com animais ocorreram no início dos anos 1950.
Os primeiros transplantes de medula óssea foram feitos em humanos em 1957 por E. Donnall Thomas em Nova York, resultando na morte de seis receptores em menos de três meses. Eles foram feitos em uma época em que não existia a noção de histocompatibilidade .
Os primeiros transplantes de medula óssea bem-sucedidos foram realizados em 1958 por Georges Mathé , então assistente de Jean Bernard no hospital Saint-Louis em Paris, em cinco físicos iugoslavos acidentalmente irradiados em um reator nuclear. Quatro sobreviveram ao transplante. Em 1963, Georges Mathé transplantou com sucesso um paciente leucêmico após irradiação total. O paciente permaneceu em remissão completa por mais de dezoito meses antes de morrer de encefalite.
O primeiro sucesso prolongado remonta à década de 1970. Os primeiros transplantes HLA idênticos foram realizados para crianças com deficiências imunológicas graves por Robert Good em Minneapolis nos Estados Unidos em 1958 e Claude Griscelli em 1971 no hospital Necker (Nouv presse Med, maio de 1973 Jan1 : 2n220-7 e Clin .exp immunol1974 jun17: 2 245-52).
A primeira descrição de sucesso no caso de doador não aparentado é feita logo em seguida.
Nos anos 1980, Éliane Gluckman foi encarregada por Jean Bernard da responsabilidade pelo serviço de transplante de medula óssea do hospital Saint-Louis. Ela deu origem ao primeiro transplante de sangue do cordão umbilical em uma criança americana com doença de Fanconi (anemia aplástica de origem autossômica recessiva).
Em 1990, E. Donnall Thomas recebeu o Prêmio Nobel de Medicina por seus avanços na área.
Medula óssea
Sua operação
A medula óssea é um tecido que se encontra dentro de todos os ossos principais (tíbia, pelve, etc.) e não tem nada a ver com a medula espinhal . Na verdade, existem dois tipos de medula, a medula branca localizada na diáfise dos ossos longos (fêmur, tíbia, úmero ...) e a medula hematopoiética vermelha, localizada nos ossos curtos (cubóide, astrágalo, escafoide. ..) ou plana (osso ilíaco, escápula, esterno, etc.) e na epífise de ossos longos (cabeça do fêmur, planalto tibial, maléolos, etc.) onde são feitos os elementos figurativos do sangue. Este último constitui o sistema hematopoiético: produz glóbulos vermelhos , glóbulos brancos e plaquetas .
Doenças
A questão do transplante surge quando as células da medula óssea de um paciente não desempenham mais sua função. Diferentes doenças do sangue (doenças do sangue) podem ser causadas por disfunção da medula óssea:
- A anemia aplástica é uma doença que se caracteriza pela interrupção do funcionamento do cordão umbilical que afeta principalmente as crianças.
- Na leucemia ( câncer do sangue ), a medula continua a funcionar, mas as células produzidas não funcionam.
- As crianças-bolha sofrem de deficiência do sistema imunológico, geralmente desde o nascimento.
- No linfoma , o câncer afeta a produção de células brancas do sangue.
A deficiência de cada um dos tipos de células produzidas pela medula pode causar diversos distúrbios:
- que nas células vermelhas do sangue leva à anemia ,
- que nos glóbulos brancos leva à neutropenia , ou seja, a uma fraqueza nas defesas imunológicas e a infecções,
- e que nas plaquetas para trombocitopenia , portanto, para um risco aumentado de sangramento, ou mesmo problemas hemorrágicos
Em algumas dessas doenças, um transplante de medula óssea pode ser considerado para alcançar a cura. O transplante não é necessariamente o principal tratamento para todas essas doenças. Assim, no caso da leucemia mieloide crônica, novos tratamentos têm sido desenvolvidos.
Problemas de compatibilidade
Se for escolhido o tratamento com transplante de medula óssea, deve-se encontrar um doador compatível com o paciente.
Como acontece com todos os aloenxertos , a compatibilidade entre o doador e o receptor é um problema importante a ser resolvido: para maximizar as chances de sucesso do transplante, é necessário que a compatibilidade HLA (ou histocompatibilidade ) entre o doador e o receptor seja tão alto quanto possível.
Compatibilidade HLAO sistema HLA é o sistema que permite que o corpo e seu sistema imunológico reconheçam o eu (todos os tecidos, etc.), o não-eu (vírus, bactérias e ... transplantes). Cada corpo humano tem seu próprio código HLA, que se encontra na superfície de suas células. Assim, qualquer corpo estranho ou célula que não possua os marcadores HLA “corretos” em sua superfície é atacado pelo sistema imunológico.
O código HLA de um indivíduo é determinado pelos diferentes alelos que representam os 6 genes (A, B, C, DR, DQ e DP) que governam a histocompatibilidade. Estes genes estão presentes no cromossoma n o 6 e têm muitos alelos:
| Desconfortável | Número de alelos identificados |
| NO | 268 |
| B | 517 |
| VS | 129 |
| DR | 333 |
| DQ | 53 |
| DP | 109 |
O grande número de alelos para cada um dos genes leva a um número ainda maior de combinações possíveis que são todos códigos HLA. Estima-se que 10-30% das pessoas vivas têm um código HLA próprio que nenhum outro ser humano no mundo compartilha.
Apesar dessa dificuldade, os códigos HLA do doador e do receptor devem ser o mais próximos possível para permitir que as células do doador ocorram no corpo do receptor sem desencadear uma reação de rejeição. Em um transplante de medula óssea, o sistema imunológico do receptor está gravemente enfraquecido ou inexistente. Não é ele quem está na origem da reação de rejeição. São as células transplantadas do doador, que terão que produzir o novo sistema imunológico do paciente, que atacará os tecidos do receptor, percebidos como hostis, como alheios. Esta é a doença do enxerto contra o hospedeiro (doença de GvH, doença do enxerto contra o hospedeiro).
Encontre um doador compatívelEm busca de um doador, o médico irá primeiro recorrer aos diferentes membros dos irmãos do paciente (irmãos e irmãs) para encontrar os mesmos marcadores HLA. Gêmeos idênticos costumam ser os mais compatíveis entre si.
Na verdade, há uma chance de 4 que dois irmãos têm o mesmo código de HLA: a criança recebe um cromossomo n o 6 do seu pai e um de sua mãe, que também cada um tem duas cópias. A criança, portanto, herdará uma das quatro combinações possíveis de cromossomos:
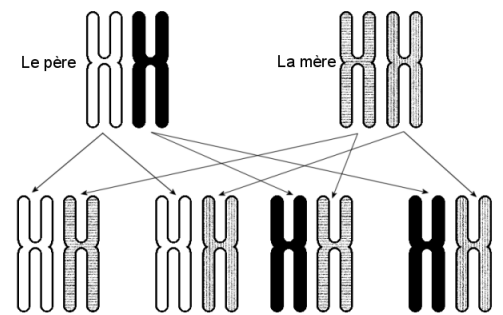
Se, no entanto, nenhum dos irmãos tiver o mesmo código HLA do paciente, o médico pesquisará o banco de dados global de doadores, que lista 31 milhões de voluntários com suas informações HLA.
Se essa pesquisa falhar porque nenhum dos voluntários cadastrados é compatível, então resta a solução de sangue do cordão umbilical (veja abaixo) ou um transplante de um membro da família com histocompatibilidade imperfeita, denominado haplo-idêntico.
Processo de doação
Assim que um doador adequado for encontrado, o processo de transplante pode começar. Consiste na transferência de um determinado número de células que constituem a medula óssea (células-tronco hematopoiéticas, ou HSC) para o paciente. Essas células irão reconstituir toda a medula óssea do receptor após o transplante.
vestir
Existem várias formas de doação:
- amostragem intraóssea,
- a aférese ,
- coleta de sangue do cordão umbilical
As células removidas podem ser enxertadas por 24 horas. Isso permite que sejam transportados por grandes distâncias. Se, entretanto, surgissem problemas logísticos, seria o doador que abordaria o paciente, que estava frágil demais para se mover.
Amostragem intraósseaEsta amostra é coletada sob anestesia geral e requer hospitalização do doador por um período de dois dias. O procedimento em si dura de uma a duas horas. Consiste em tirar por punções nos ossos da pelve uma quantidade de medula óssea calculada de acordo com o peso do doador. Essa amostra permite coletar tanto as células-tronco hematopoéticas quanto o tecido celular que as circunda.
Às vezes, uma bolsa de sangue de um doador pode ser retirada antes do procedimento. Foi devolvido a ele no processo de promover sua recuperação.
CitafereseEssa técnica permite que as células-tronco periféricas sejam coletadas por centrifugação do sangue do doador. Os constituintes do sangue não coletados são devolvidos ao doador. A quantidade de células-tronco hematopoéticas tomadas é maior em comparação com a via intraóssea. Poucos dias antes da medula óssea do doador ser estimulada por injeção subcutânea de um medicamento análogo ao G-CSF (Fator Estimulador de Colônias de Granulócitos), como as moléculas filgrastim ou lenograstim, que causa a passagem de células-tronco hematopoiéticas da medula óssea para o sangue . A amostra é coletada uma ou duas vezes por 3 a 4 horas, sem internação.
A escolha entre aférese ou via intraóssea é feita pelo médico levando em consideração diversos critérios vinculados tanto ao receptor quanto ao doador.
Coleta de sangue do cordão umbilicalO sangue com virtudes terapêuticas também pode ser colhido após o nascimento de uma criança. Este é o sangue retirado da placenta (não do recém-nascido) do cordão. O sangue da placenta também contém HSCs. Apresentam a vantagem de serem jovens e imaturos, o que permite reduzir os riscos de rejeição imunológica e de reação enxerto versus hospedeiro. Uma doação até mesmo para um paciente com o qual a compatibilidade HLA não é perfeita é então possível.
Esse sangue costuma ser destinado a crianças, pois a quantidade limitada de células-tronco ali encontradas nem sempre permite o tratamento de um paciente com peso superior a 50 kg . Alguns estudos mostram que é possível combinar dois cordões sanguíneos (próximos do ponto de vista de seu HLA) para tratar adultos.
O transplante
Antes de fazer o transplante, o paciente está preparado: sua medula, doente, está completamente destruída. Para isso, ele receberá quimioterapia, chamada de "condicionamento", por dez dias. A hospitalização é feita em sala esterilizada porque a quimioterapia terá colocado o paciente em aplasia profunda ao destruir seu sistema imunológico.
O próprio transplante é realizado na forma de uma infusão, por meio da qual a medula preparada é recebida pelo paciente.
As células transplantadas ocorrerão então nos ossos para reconstituir gradualmente todo o tecido da medula óssea e retomar a produção das várias células sanguíneas. Isso não ocorre até 10 a 30 dias após o transplante, tempo durante o qual é necessário continuar a proteger o paciente de agentes infecciosos. Ao final de 3 meses, as defesas imunológicas podem ser reconstituídas. No entanto, este cenário pode escurecer se ocorrer uma reação de rejeição, se a doença enxerto versus hospedeiro se desenvolver (ver abaixo). Em alguns casos, por exemplo, linfoma, doença do enxerto contra hospedeiro moderada é um fator crítico na cura da doença subjacente porque o enxerto, uma vez desenvolvido, ataca as células cancerosas.
Complicações
Reação enxerto versus hospedeiro
A "doença do enxerto contra o hospedeiro" ( doença enxerto-versus-hospedeiro , ou GVHD GVHD) é uma complicação grave e comum de transplantes de medula óssea alogénicos. É causada por células imunocompetentes da medula óssea do doador que irão atacar o organismo do receptor, incapaz de rejeitá-las devido à imunossupressão induzida antes do transplante (condicionamento do receptor pela supressão de sua medula e de sua memória imunológica.). Certos órgãos são o alvo preferencial da DECH aguda: pele , trato digestivo e dutos biliares, mas também envolvimento pulmonar. Por definição, a GVHD é considerada aguda quando ocorre antes do centésimo dia pós-transplante e crônica após. Os surtos crônicos de GVHD não têm necessariamente um caráter recorrente e regular, ao contrário do significado primário e enganoso do termo usado para qualificá-lo. Em vez disso, eles ocorrem esporadicamente e de forma imprevisível. O GVHD crônico pode se desenvolver sem um GVHD agudo prévio.
Para limitar ou até eliminar completamente qualquer risco de rejeição, os médicos usam drogas: imunossupressores. Seu objetivo é diminuir a resposta imunológica do corpo, limitando o nível de anticorpos criados pelos linfócitos B e o número de linfócitos T2. Corticosteroides, inibidores da síntese de DNA e soros monoclonais serão mencionados como imunossupressores. No entanto, a atividade dos imunossupressores, embora benéfica para o paciente, resulta em fraqueza do paciente em relação aos ataques de doenças, e seus efeitos colaterais não são desprezíveis. É por isso que todos os pacientes que recebem imunossupressores têm acompanhamento médico muito regular.
Torne-se um doador
Dadas as restrições de compatibilidade, a estratégia de doação de medula óssea é diferente daquela de doação de sangue. Na verdade, não se trata de armazenar doações nos bancos enquanto se espera por uma possível necessidade.
O processo é inverso: as pessoas que se voluntariam para doar medula óssea são listadas em um registro nacional, no qual sua tipagem HLA é indicada. Isso é feito a partir de um simples exame de sangue. A doação de medula óssea só será feita se um paciente compatível realmente precisar e não encontrar um irmão ou irmã compatível em sua família. Na França, o registro de doadores voluntários é mantido pela Agência de Biomedicina .
Entre o registro no arquivo e a efetiva doação, pode decorrer um período de tempo bastante variável (de alguns meses a muitos anos). Também é possível que a doação nunca ocorra se nenhum paciente for compatível.
Durante a doação, os dois princípios principais a seguir são aplicados:
- o anonimato : o doador e o receptor nunca se encontrarão e a identidade de um não será comunicada ao outro
- a gratuidade : o traficante não será pago por seu gesto. No entanto, todos os custos de hospitalização serão cobertos.
Cadastro
Para ser voluntário, você deve atender a cinco condições:
- ser maior de idade
- estar com boa saúde, e
- ter um índice de massa corporal inferior a 30 e
- ter menos de 35 anos ao se registrar (doação é possível até 60), e
- aceitar uma entrevista médica sobre seu histórico médico e estilo de vida.
É durante a entrevista médica que uma amostra de saliva ou um exame de sangue é coletado para determinar a tipagem HLA e detectar certas doenças. Essa análise pode ser parcial e outro exame de sangue pode ser feito se houver início de compatibilidade com o paciente.
Durante o registro, o novo código HLA é comparado com todos os dos pacientes listados.
As pré-inscrições são feitas online no site dondemoelleosseuse.fr .
A situação na França
O France Marrow Registry é credenciado pela World Marrow Donor Association (WMDA), que reúne 73 registros em 52 países, que em abril de 2021 representavam 38,7 milhões de doadores potenciais em todo o mundo. O registo France Greffe de Moelle (FGM) é gerido pela Agência de Biomedicina. No final de 2019, havia 311.555 doadores registrados no arquivo francês. Em 2014, houve 1.943 aloenxertos de células-tronco hematopoéticas (HSCs) e 927 transplantes não relacionados com doadores voluntários, incluindo 187 com unidades de sangue placentário. Em 2016, 205 doadores do registro francês doaram sua medula óssea. Dessas doações, 75% são por aférese e 25% por amostragem intraóssea. A compatibilidade entre um paciente e um doador fora da família é em média de 1 em 1 milhão, é de 1 em 4 entre irmãos e irmãs da mesma família.
A doação de medula óssea era como a doação de sangue e órgãos, a “Grande Causa Nacional de 2009” na França. Uma semana nacional anual é dedicada a ele. Desde 2012, os potenciais doadores cadastrados no arquivo reúnem-se na comunidade e são chamados de “vigilantes da vida”.
Notas e referências
- " Tudo sobre doação | Don de Moelle Osseuse ” , em www.dondemoelleosseuse.fr (acessado em 11 de novembro de 2018 )
- (em) Thomas ED, Lochte HL Jr, Lu toalete, Ferrebee JW, "Infusão intravenosa de medula óssea em pacientes recebendo radiação e quimioterapia", N Engl J Med. 1957; 257: 491-496
- Biografia de Georges mathé
- Mathé L, Jammet H, Pendic B, G Schwarzenberg, Duplan JF, Maupin B, Latarjet R, Larrieu MJ, Kalic D, Djukic Z. "transfusões e transplante de medula óssea homólogas em humanos irradiados acidentalmente em dose elevada" Rev Fr Estudo Clin Biol. Março de 1959; 4 (3): 226-38.
- (em) G. Mathe, JL Amiel L. Schwarzenberg Cattan A. e M. Schneider "Haematopoietic Chimera in Man After allogenic (Homologous) Bone-medula transplantation", Br Med J. 1963, 28 de dezembro; 2 (5373): 1633–1635.
- (em) Jansen, Jan, " The first successful alogeneic bone-medrow transplant Georges Mathe " , Transfusion Medicine Reviews , n o Vol 19, No 3,Julho de 2005
- (in) Appelbaum FR, o primeiro transplante de medula de uma criança com imunodeficiência hereditária foi conduzido por Robert Good em Minneapolis nos EUA em 1968. Na França, um primeiro filho com a mesma imunodeficiência grave foi transplantado em 1971 por Claude Griscelli e sua equipe em 1971. Morreu com sequelas de meningite contraída antes do transplante e apesar de uma reconstituição imunológica completa. O segundo transplante realizado pela mesma equipe no Hospital Necker em 1972 foi um sucesso total. A menina que receberam medula de seu irmão tem linfócitos do sexo masculino, enquanto todas as outras células são do sexo masculino, o que mostra que apenas as populações de células que faltam são permanentemente transplantado (Nouv Presse Med 13, 1:20 1364 e Clin Exp. Imunologia 19742,245-52) hematopoiéticas transplante de células em 50 , N Eng J Med, 2007; 357: 1472-1475
- " Biomedicine Agency - The medical and Scientific Annual report 2016 " , em www.agence-biomedecine.fr (acessado em 11 de novembro de 2018 )
- "A doação de sangue do cordão umbilical pode salvar vidas " , em www.dondesangdecordon.fr (acessado em 11 de novembro de 2018 )
- Bouaziz JD., Bagot M., Rybojad M., “ Graft versus host disease ” , em http://www.therapeutique-dermatologique.org/ , dezembro de 2011(acessado em 20 de julho de 2012 )
- " France Greffe de Moelle Register (RFGM) - Biomedicine Agency " , em www.agence-biomedecine.fr (acessado em 11 de novembro de 2018 )
- Boletim Nacional de Ligação - Registro de Medula da França, fevereiro de 2017
- Associação Mundial de Doadores de Medula Óssea
- http://www.agence-biomedecine.fr/
- RESUMO DA ATIVIDADE DO REGISTRO DE FRANÇA GRAFFE DE MOELLE EM 2019 [1]
- http://asp.zone-secure.net/v2/index.jsp?id=324/9403/59616&lng=fr
- Relatório anual 2015 Biomedicine Agency , em " http://www.agence-biomedecine.fr/ ". Acessado em 03 de março de 2017
Veja também
Artigos relacionados
links externos
- Associação de transplante de medula francesa encomendada pelo Ministério da Saúde para gerenciar o arquivo de doadores franceses
- Fundação Suíça de Células-Tronco de Sangue
- Agence de la Biomédecine (antigo estabelecimento francês de transplantes) As informações estão disponíveis na secção "Sites para o público em geral" sob o título "Os nossos sites temáticos", "Osso da medula óssea de Don"
- Site oficial para doação de medula óssea na França
- (pt) O número de doadores por país