Hidrazina
| Hidrazina | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 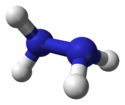 Dimensões e modelo 3D da hidrazina |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identificação | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nome IUPAC | hidrazina | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Sinônimos |
diazano, diamina |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o CAS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o ECHA | 100.005.560 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| N o EC | 206-114-9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PubChem | 8058 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SORRISOS |
NN , |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| InChI |
InChI: InChI = 1 / H4N2 / c1-2 / h1-2H2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Aparência | líquido higroscópico, incolor, esfumaçado com um odor pungente. | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades quimicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fórmula bruta | N 2 H 4 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa molar | 32,0452 ± 0,0007 g / mol H 12,58%, N 87,42%, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Momento dipolar | 1,75 D | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Diâmetro molecular | 0,390 nm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades físicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Fusão T ° | 2 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T ° fervendo | 114 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilidade | miscível com água e solventes orgânicos polares |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Parâmetro de solubilidade δ |
37,3 MPa 1/2 ( 25 ° C ) 36,2 J 1/2 · cm -3/2 ( 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Massa volumica |
1010 kg · m -3
equação:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto de inflamação | 38 ° C ( cf ) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limites explosivos no ar | 1,8 - 100 % vol | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Pressão de vapor de saturação | anidro: 21 mbar ( 20 ° C ), solução a 64 % m : equação:
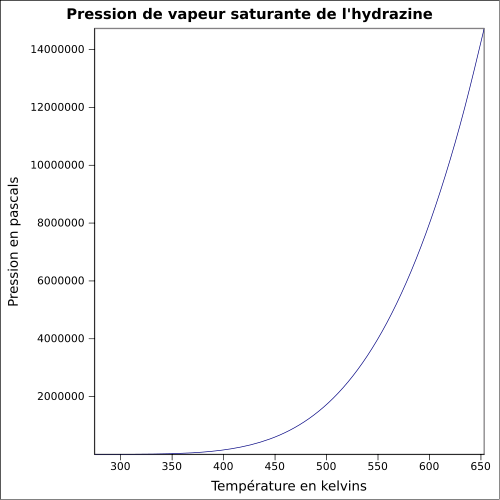
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Viscosidade dinamica | 0,9 mPa · s a 25 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ponto crítico | 147,0 bar , 379,85 ° C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Termoquímica | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 gás, 1 bar | 238,68 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| S 0 líquido, 1 bar | 121,52 J · K -1 · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 gás | 95,35 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ f H 0 líquido | 50,63 kJ · mol -1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Δ vap H ° |
41,8 kJ · mol -1 ( 1 atm , 113,55 ° C ); 44,7 kJ · mol -1 ( 1 atm , 25 ° C ) |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| C p |
equação:
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCS | 667,1 kJ · mol -1 ( 25 ° C , gás) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| PCI | -622,08 kJ · mol -1 (gás) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades eletrônicas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1 energia de re ionização | 8,1 ± 0,15 eV (gás) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriedades ópticas | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Índice de refração | 1.469 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Precauções | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
     Perigo H226, H301, H311, H314, H317, H331, H350, H410, P201, P261, P273, P280, P301 + P310, P305 + P351 + P338, H226 : Líquido e vapor inflamáveis H301 : Tóxico por ingestão H311 : Tóxico em contato com a pele H314 : Provoca queimaduras na pele e lesões oculares graves H317 : Pode causar uma reação alérgica na pele H331 : Tóxico por inalação H350 : Pode causar câncer (indicar via de exposição se for conclusivamente provado que nenhuma outra via de exposição causa o perigo) H410 : Muito tóxico para os organismos aquáticos com efeitos duradouros P201 : Obtenha instruções especiais antes da utilização. P261 : Evite respirar poeira / fumaça / gás / névoa / vapores / spray. P273 : Evite a liberação para o meio ambiente. P280 : Use luvas de proteção / roupas de proteção / proteção ocular / proteção facial. P301 + P310 : Em caso de ingestão: contacte imediatamente um CENTRO DE INFORMAÇÃO ANTIVENENOS ou médico / médico. P305 + P351 + P338 : Se entrar em contato com os olhos: enxágue cuidadosamente com água por vários minutos. Remova as lentes de contato se a vítima as estiver usando e elas podem ser removidas facilmente. Continue a enxaguar. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| WHMIS | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   B3, D1A, D2A, E, B3 : Líquido combustível D1A : Material muito tóxico causando efeitos sérios imediatos D2A : Material muito tóxico causando outros efeitos tóxicos E : Material corrosivo 0,1% de divulgação de acordo com a lista de divulgação de ingredientes |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3 3 3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Outro | Pode atacar o sistema nervoso. Fatal em altas doses. |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transporte | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
0113 : GUANYL NITROSAMINOGUANYLIDENE HIDRAZINA HUMIDIFICADA com pelo menos 30 por cento (massa) de água Classe: 1 Código de classificação: 1.1A : Substâncias e artigos com risco de explosão em massa (uma explosão em massa é uma explosão que afeta quase instantaneamente carga inteira). Material explosivo primário. Etiqueta: 1 : Substâncias e artigos explosivos 
663 : material muito tóxico e inflamável (ponto de inflamação igual ou inferior a 60 ° C ) Número ONU : 1163 : DIMETILHIDRAZINA ASSIMÉTRICA Classe: 6.1 Código de classificação: TFC : Substâncias tóxicas corrosivas inflamáveis. ; Rótulos: 6.1 : Materiais tóxicos 3 : Líquidos inflamáveis 8 : Materiais corrosivos   
663 : material muito tóxico e inflamável (ponto de inflamação igual ou inferior a 60 ° C ) Número ONU : 1244 : METILHIDRAZINA Classe: 6.1 Código de classificação: TFC : Substâncias tóxicas corrosivas inflamáveis. ; Rótulos: 6.1 : Materiais tóxicos 3 : Líquidos inflamáveis 8 : Materiais corrosivos   
886 : material muito corrosivo e tóxico Número UN : 2029 : HIDRAZINA ANIDRÁSTICA Classe: 8 Código de classificação: CFT : Substâncias corrosivas líquidas, inflamáveis, tóxicas; Rótulos: 8 : Materiais corrosivos 3 : Líquidos inflamáveis 6.1 : Materiais tóxicos Embalagem: Grupo de embalagem I : materiais muito perigosos;   
86 : corrosivo ou apresentando um grau menor de corrosividade e toxicidade Número ONU : 2030 : HIDRAZINA HIDRATO contendo mais de 37 por cento, mas não mais de 64 por cento (massa) de hidrazina; ou SOLUÇÃO AQUOSA DE HIDRAZINA contendo mais de 37 por cento, mas não mais de 64 por cento (em massa) de hidrazina Classe: 8 Código de classificação: CT1 : Corrosivos tóxicos: Líquidos; Etiquetas: 8 : Substâncias corrosivas 6.1 : Substâncias tóxicas Embalagem: Grupo de embalagem I / II : substâncias muito / moderadamente perigosas;  
86 : corrosivo ou apresentando menor grau de corrosividade e toxicidade Número ONU : 2030 : HIDRAZINA HIDRATO contendo mais de 37 por cento, mas não mais de 64 por cento (massa) de hidrazina; ou SOLUÇÃO AQUOSA DE HIDRAZINA contendo mais de 37 por cento, mas não mais de 64 por cento (em massa) de hidrazina Classe: 8 Código de classificação: CT1 : Tóxicos corrosivos: Líquidos; Etiquetas: 8 : Substâncias corrosivas 6.1 : Substâncias tóxicas Embalagem: Grupo de embalagem III : substâncias de baixo perigo.  
663 : material muito tóxico e inflamável (ponto de inflamação menor ou igual a 60 ° C ) Número ONU : 2382 : DIMETILHIDRAZINA SIMÉTRICA Classe: 6.1 Código de classificação: TF1 : Materiais tóxicos inflamáveis: Líquidos; Rótulos: 6.1 : Materiais tóxicos 3 : Líquidos inflamáveis Embalagem: Grupo de embalagem I : materiais muito perigosos;  
60 : material tóxico ou com menor grau de toxicidade Número ONU : 2572 : FENILHIDRAZINA Classe: 6.1 Código de classificação: T1 : Substâncias tóxicas sem risco subsidiário: Orgânico, líquidos; Etiqueta: 6.1 : Substâncias tóxicas Embalagem: Grupo de embalagem II : substâncias moderadamente perigosas; 
3165 : TANQUE DE COMBUSTÍVEL PARA MOTOR HIDRÁULICO DE AERONAVES contendo uma mistura de hidrazina anidra e monometilhidrazina (combustível M86) Classe: 3 Código de classificação: FTC : Líquidos inflamáveis , tóxicos, corrosivos Etiquetas: 3 : Líquidos inflamáveis 6.1 : Substâncias tóxicas 8 : Substâncias corrosivas Embalagem: Grupo de embalagem I : substâncias muito perigosas;   
60 : material tóxico ou com menor grau de toxicidade Número ONU : 3293 : SOLUÇÃO AQUOSA DE HIDRAZINA contendo não mais de 37 por cento (em massa) de hidrazina Classe: 6.1 Código de classificação: T4 : Substâncias tóxicas sem risco subsidiário: Inorgânico, líquido; Etiqueta: 6.1 : Substâncias tóxicas Embalagem: Grupo de embalagem III : substâncias de baixo perigo.  |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classificação IARC | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Grupo 2B: Possivelmente cancerígeno para humanos | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Ecotoxicologia | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| LogP | -3,1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Limiar de odor | baixo: 3 ppm alto: 4 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unidades de SI e STP, salvo indicação em contrário. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
A hidrazina , de nome oficial diazano , de fórmula química N 2 H 4 e fórmula de estrutura H 2 N-NH 2 , é um composto químico líquido incolor com um odor que lembra amônia . É miscível com água em todas as proporções.
Hidrazinas também constituem uma família de compostos químicos derivados de hidrazina (H 2 N-NH 2 por substituição de um ou mais átomos de H por radicais de hidrocarbonetos (por exemplo, 2,4-dinitrofenil-hidrazina ).
A produção anual de hidrazina é de 260.000 toneladas. A maior parte dessa produção é usada como agente espumante para a produção de polímeros espumados. O restante dessa produção é dividido em vários setores, como a química orgânica para a síntese de medicamentos ou a química inorgânica para a produção de azida sódica , o agente explosivo para inflar " airbags " (airbags). A hidrazina também pode ser usada como combustível para motores de foguete .
Estrutura molecular e propriedades
A estrutura da hidrazina é apresentada como duas moléculas de amônia acopladas uma à outra removendo um hidrogênio para cada uma das duas moléculas. Cada subunidade -NH 2 tem uma forma piramidal. A distância entre os dois átomos de nitrogênio é de 145 µm e a molécula adota uma conformação anticlinal. O torque é o dobro do etano . Suas propriedades estruturais se assemelham às do gás peróxido de hidrogênio , que adota uma conformação "assimétrica" semelhante a uma estrutura alcana linear, com alto torque.
Tem as propriedades de uma base comparável à amônia , mas 15 vezes mais fraca.
O substituinte em cada amina torna o dupleto eletrônico menos disponível para pegar um próton e, portanto, menos básico. A hidrazina é um nucleófilo melhor do que a amônia por causa da repulsão entre os dupletos não vinculantes dos átomos de nitrogênio adjacentes.
A segunda protonação é mais difícil:
[N 2 H 5 ] ++ H + → [N 2 H 6 ] 2+ ; K = 8,4 × 10 -16A hidrazina é um agente redutor muito mais forte em um ambiente básico do que em um ambiente ácido. (E = -0,23 V a pH = 0 e E = -1,16 V a pH = 14). Quando a hidrazina reage com os oxidantes, vários produtos nitrogenados podem ser formados, mas geralmente é o dinitrogênio. A reação da hidrazina com o dioxigênio forma dinitrogênio e água, enquanto libera uma grande quantidade de calor.
Hidrazina N 2 H 4degrada-se sob a ação do calor e dos raios ultravioleta em nitrogênio N 2, hidrogênio H 2e amônia NH 3.
Alguns sais de hidrazina são explosivos : nitrato hidrazina , clorato hidrazina perclorato hidrazina e azida hidrazônio.
Propriedades físico-químicas
A hidrazina anidra é um líquido incolor, fumegante, com odor de amina. O limite de odor é de 3 ppm .
Síntese
Theodor Curtius sintetizou a hidrazina simples pela primeira vez em 1889 pela porta dos fundos.
A hidrazina é produzida pelo processo de Olin Raschig a partir do hipoclorito de sódio e da amônia , um método inventado em 1907. Esse processo depende da reação das cloraminas com a amônia.
NH 2 Cl+ NH 3→ H 2 N - NH 2+ HCl .A monocloramina necessária sendo produzida de antemão pela reação: NH 3 + HOCl → NH 2 Cl + H 2 OUma variante do processo de Olin Raschig é a oxidação da ureia por hipoclorito de sódio :
(H 2 N) 2 C = O+ NaOCl + 2 NaOH → N 2 H 4+ H 2 S+ NaCl + Na 2 CO 3.No ciclo Atofina-PCUK, a hidrazina é produzida em várias etapas a partir da acetona , amônia e peróxido de hidrogênio. A acetona e a amônia reagem primeiro para dar uma imina , seguida pela oxidação da reação com peróxido de hidrogênio em oxaziridina , um heterociclo de três átomos compreendendo um átomo de carbono, um átomo de nitrogênio e um átomo de oxigênio, seguido por amoniólise que resulta em hidrazona , um processo que reúne dois átomos de nitrogênio. A hidrazona reage com o excesso de acetona, e a acetona azina produzida é hidrolisada para formar a hidrazina, regenerando a acetona. Ao contrário do processo Raschig, este método não gera sal. A PCUK está associada à Ugine Kuhlmann , fabricante francesa de produtos químicos.
A hidrazina também pode ser produzida por um método conhecido como processo de cetazina e peróxido .
Em 2001, Marc Strous, microbiologista da Universidade de Nijmegen, na Holanda, descobriu que a hidrazina é produzida por leveduras e uma bactéria oceânica, Brocadia anammoxidans , por meio de uma reação anammox realizada em organelas especializadas chamadas anammoxossomos . Eles são os únicos organismos vivos atualmente conhecidos capazes de produzir hidrazina naturalmente.
Derivados
Muitos derivados de substituição da hidrazina são conhecidos, e vários deles são produzidos naturalmente. Alguns exemplos :
- a giromitrina (in) e a agaritina (in) são fenil-hidrazinas encontradas em uma espécie de cogumelos cultivados e comercializados o Agaricus bisporus . A giromitrina é metabolizada em monometilhidrazina ;
- a iproniazida , a hidralazina e a fenelzina (en) são drogas feitas a partir da hidrazina;
- a 1,1-dimetil-hidrazina (UDMH) e 1,2-dimetil-hidrazina (en) são hidrazinas onde dois átomos de hidrogênio são substituídos por grupos metil ;
- a 2,4-dinitrofenilhidrazina (2,4-DNPH) é comumente usada para testes de cetonas e aldeídos em química orgânica ;
- a fenil-hidrazina , C 6 H 5 NHNH 2 , hidrazina é o primeiro a ser descoberto.
Use em química
As hidrazinas são utilizadas na síntese de muitas moléculas orgânicas e muitas delas são de importância prática na indústria farmacêutica , como medicamento anti-tuberculose , bem como em têxteis como corante e na fotografia.
Também é encontrado na indústria em geral e mais particularmente misturado com água de alimentação para caldeiras a vapor. Seu objetivo é destruir as últimas moléculas de oxigênio e, assim, evitar a corrosão das linhas de vapor de aço.
Reação com carbonilas
Para ilustrar a condensação da hidrazina com um radical carbonila, vamos citar a reação com acetona que resulta na formação de diisopropilideno hidrazina. Este reage novamente com a hidrazina para formar uma hidrazona:
2 (CH 3 ) 2 CO+ N 2 H 4→ 2 H 2 O+ [(CH 3 ) 2 C = N] 2. [(CH 3 ) 2 C = N] 2+ N 2 H 4→ 2 (CH 3 ) 2 C = N - NH 2.A acetona e a diisopropilideno hidrazina são intermediários na síntese de PCUK-Atofina. A alquilação dirige as hidrazinas com halogenetos de alquila na presença de uma forma básica dos derivados alquilados das hidrazinas, mas a reação é geralmente ineficaz devido ao fraco controle do grau de substituição (como para as aminas comuns). Reduzir a hidrazona a hidrazina é uma maneira elegante de produzir 1,1 hidrazinas dialquiladas.
Em outra reação, 2-ciano piridina reage com hidrazina para formar hidrazidas amidadas que podem ser convertidas em triazinas usando 1,2-dicetonas.
Reação Wolff-Kishner
A hidrazina é usada na química orgânica na redução de Wolff-Kishner , uma reação que converte o grupo carbonila de uma cetona ou aldeído em uma ponte de metileno (ou grupo metil ) por meio de uma molécula de hidrazona . A produção de dinitrogênio muito estável a partir da hidrazina promove a reação.
Síntese de moléculas policíclicas
Tendo duas funções amina, a hidrazina é uma peça chave para a preparação de muitos compostos heterocíclicos por condensação, com uma parte tendo duas funções eletrofílicas . Com acetilacetona , ele condensa para dar 3,5-dimetilpirazol . Na reação de Einhorn-Brunner, as hidrazinas reagem com as imidas para dar triazóis .
Sulfonação
Por ser um bom nucleófilo, o N 2 H 4 é vulnerável ao ataque por haletos de sulfonila e haletos de acila. A tosil hidrazina também forma hidrazonas após o tratamento com carbonilas.
Repartição de ftalimidas
A hidrazina é usada para dividir a N- ftalimida em derivados de alquil. Esta reação de clivagem permite que o ânion ftalimida seja usado como um precursor de amina na síntese de Gabriel.
Agente redutor
A hidrazina é um agente redutor popular porque seus subprodutos da decomposição são geralmente nitrogênio gasoso e água. Assim, é usado como um antioxidante , eliminador de oxigênio e inibidor de corrosão na água de caldeiras e circuitos de aquecimento (neste papel, N, N-dietilhidroxilamina é agora preferido , de menor toxicidade, mas ainda é amplamente utilizado contra corrosão em grandes centrais térmicas e nucleares em particular). Também é usado para reduzir sais de metais e óxidos metálicos ao estado metálico na eletrólise do níquel, bem como na extração de plutônio de combustíveis nucleares usados .
Sais de hidrazina
A hidrazina é convertida em sais sólidos por tratamento com ácidos minerais. O sal mais comum é o hidrogenossulfato de hidrazina, N 2 H 5 HSO 4 , que provavelmente deveria ser chamado de bissulfato de hidrazina. O bissulfato de hidrazina é usado como um tratamento alternativo para a caquexia induzida pelo câncer. O sal de hidrazina e ácido N 5 H 5 azotídrico foi de interesse científico, devido ao seu alto teor de nitrogênio e propriedades explosivas.
Usos industriais
A hidrazina é utilizada em muitos processos, por exemplo na produção de fibras de spandex , como catalisador de polimerização , agente de expansão, para células a combustível , como fluxo de solda para soldagem , para revelação de fotografias, como cadeia extensora para polimerização de poliuretano , como um composto redutor para o condicionamento de água em centrais térmicas e circuitos secundários em centrais nucleares e como estabilizador de calor. Além disso, uma técnica que usa depósitos de hidrazina em semicondutores foi recentemente testada, com possível aplicação na fabricação de transistores de película fina usados para telas de cristal líquido . Hidrazina em solução 70% com 30% de água é usada para alimentar a EPU (unidade de energia de emergência), em aviões de combate F-16 ( General Dynamics F-16 Fighting Falcon ).
No uso militar, um derivado da hidrazina, a dimetil hidrazina assimétrica (UDMH) , combinada com nitrato de amônio é o ingrediente básico do astrólito (in) , um explosivo extremamente poderoso inventado na década de 1960.
Combustível de foguete
A hidrazina foi usada pela primeira vez como combustível de foguete na Segunda Guerra Mundial para os aviões Messerschmitt Me 163 (o primeiro avião-foguete), sob o nome de B-Stoff (na verdade, hidrato de hidrazina ). Este B-Stoff foi misturado com metanol ( M-Stoff ) para dar C-Stoff , que foi usado como combustível com T-Stoff , um concentrado de peróxido de hidrogênio , usado como um oxidante em contato com o qual se inflamou. Espontaneamente em um reação muito enérgica.
Hoje, a hidrazina é geralmente usada sozinha como monopropelente em motores de baixo empuxo (mas de alta precisão), permitindo o posicionamento de satélites e sondas espaciais em órbita ; neste caso, o impulso é fornecido pela decomposição catalítica da hidrazina e não por combustão. Esta decomposição é de fato uma reação muito exotérmica . É obtido passando a hidrazina sobre um catalisador cujo componente ativo é irídio metálico depositado em uma grande superfície de alumina (óxido de alumínio), ou nanofibras de carbono, ou mais recentemente nitreto de molibdênio em alumina, ou mesmo nitrato de molibdênio . Sua decomposição em amônia , nitrogênio e hidrogênio resulta das seguintes reações:
Essa decomposição é disparada em alguns milissegundos e permite que o impulso seja medido com muita precisão. Essas reações são muito exotérmicas (o catalisador na câmara pode chegar a 800 ° C em alguns milissegundos) e produzem um grande volume de gases quentes a partir de um pequeno volume de hidrazina líquida, o que a torna um bom propelente para a propulsão espacial .
Certos derivados de hidrazina são também usados como líquidos propulsores : metil-hidrazina H 2 N - NHCH 3(ou MMH), e dimetilhidrazina assimétrica , H 2 N - N (CH 3 ) 2(ou UDMH). Eles são geralmente usados com peróxido de nitrogênio N 2 O 4como um oxidante, com o qual eles formam um propelente líquido hipergólico armazenável .
Células de combustível
O fabricante italiano de catalisadores Acta propôs o uso de hidrazina como uma solução alternativa ao hidrogênio em células a combustível . A principal vantagem deste produto é sua capacidade de produzir mais de 200 mW / cm 2 , mais do que uma célula de combustível de hidrogênio semelhante, sem a necessidade de catalisadores caros contendo platina . Como o combustível é líquido à temperatura ambiente, ele pode ser manuseado e armazenado com mais facilidade do que o hidrogênio. Ao armazenar hidrazina em um tanque contendo uma carbonila com uma ligação dupla carbono- oxigênio , o combustível reage e forma um material sólido e seguro chamado hidrazona . Depois é só encher o tanque com água quente para liberar o hidrato de hidrazina na forma líquida. O manuseio do combustível líquido é na prática muito mais seguro do que o gás hidrogênio, e o líquido tem um potencial redox maior (1,56 V ) em comparação com 1,23 V do hidrogênio. A molécula de hidrazina é quebrada na bateria para formar átomos de dinitrogênio e hidrogênio que se ligam a um átomo de oxigênio para formar água.
segurança
Toxicidade, ecotoxicidade
A hidrazina é altamente tóxica e perigosamente instável, especialmente em sua forma anidra . Geralmente é usado como um monohidrato estável.
Os sintomas de exposição aguda a níveis elevados de hidrazina podem se manifestar em humanos como irritação dos olhos , nariz e garganta , tontura, dor de cabeça , náusea , edema pulmonar , convulsões , coma . A exposição aguda também pode causar danos ao fígado , rins e sistema nervoso central em humanos. O líquido é corrosivo e pode produzir eczema de contato em humanos e animais. Efeitos nocivos nos pulmões , fígado, baço e tireoide foram relatados em animais cronicamente expostos à hidrazina por inalação. Um aumento no número de pulmão, cavidade nasal, e do fígado tumores tem sido observada em roedores expostos a hidrazina.
Sua toxicidade é objeto de reavaliações periódicas, à medida que o conhecimento evolui.
Referências
- de hidrazina (anidra) , folha de segurança (s) de Programa Internacional de Segurança Química , consultado em 9 de maio de 2009
- (en) Yitzhak Marcus, The Properties of Solvents , vol. 4, Inglaterra, John Wiley & Sons Ltd,1999, 239 p. ( ISBN 0-471-98369-1 )
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (em) James E. Mark, Physical Properties of Polymer Handbook , Springer,2007, 2 nd ed. , 1076 p. ( ISBN 978-0-387-69002-5 e 0-387-69002-6 , leia online ) , p. 294
- (en) Robert H. Perry e Donald W. Green , Perry's Chemical Engineers 'Handbook , EUA, McGraw-Hill,1997, 7 th ed. , 2400 p. ( ISBN 0-07-049841-5 ) , p. 2-50
- Entry "hidrazina" no banco de dados química GESTIS da IFA (organismo alemão responsável pela segurança e saúde ocupacional) ( alemão , Inglês ), acessado 11 fev 2010 (JavaScript obrigatório)
- " Propriedades de vários gases, " em flexwareinc.com (acessado em 12 de abril de 2010 )
- (en) "Hydrazine" , no NIST / WebBook , acessado em 11 de fevereiro de 2010
- (em) David R. Lide, CRC Handbook of Chemistry and Physics , CRC Press,2009, 90 th ed. , 2804 p. , Capa dura ( ISBN 978-1-4200-9084-0 )
- (em) David R. Lide , CRC Handbook of Chemistry and Physics , Boca Raton, CRC Press,18 de junho de 2002, 83 th ed. , 2664 p. ( ISBN 0849304830 , apresentação online ) , p. 5-89
- (em) David R. Lide, Handbook of Chemistry and Physics , Boca Raton, CRC,2008, 89 th ed. , 2736 p. ( ISBN 978-1-4200-6679-1 ) , p. 10-205
- Grupo de Trabalho IARC sobre a Avaliação de Riscos Carcinogênicos para Humanos, “ Evaluations Globales de la Carcinogenicité pour l'Homme, Groupe 2B: Possibly carcinogenic to humanos ” , em http://monographs.iarc.fr , IARC,16 de janeiro de 2009(acessado em 22 de agosto de 2009 )
- Número de índice na tabela 3.1 do apêndice VI do regulamento CE nº 1272/2008 (16 de dezembro de 2008)
- SIGMA-ALDRICH
- " Hidrazina " no banco de dados de produtos químicos Reptox da CSST (Organização de Quebec responsável pela segurança e saúde ocupacional), acessado em 24 de abril de 2009
- " hidrazina, " em hazmap.nlm.nih.gov (acessada 14 de novembro de 2009 )
- “hidrazina” , em ESIS , acessado em 17 de fevereiro de 2009
- Miessler, Gary L. e Tarr, Donald A. Inorganic Chemistry, Terceira Edição . Pearson Prentice Hall (2004). ( ISBN 978-0-13-035471-6 ) .
- Química Inorgânica, DF Shriver, Peter William Atkins
- Foundations of Organic Chemistry, Michael Hornby, Josephine Peach
- (in) Holleman, AF, Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ( ISBN 978-0-12-352651-9 ) .
- Folha de segurança INRS
- Curtius, Journal für praktische Chemie , 39, 1889, p. 107-39
- Adams, R.; Brown, BK, sulfato de hidrazina, 1, 309, 1941, cv1p0309
- " Hydrazine: Chemical product info, chemindustry.ru, 2007-01-08 " ( Arquivo • Wikiwix • Archive.is • Google • O que fazer? ) (Acessado em 25 de março de 2013 )
- Riegel, Emil Raymond. "Hydrazine" Riegel's Handbook of Industrial Chemistry p. 192 (1992).
- (em) Brian Handwerk , " Bacteria Eat Human Sewage, Produce Rocket Fuel " , National Geographic Society ,9 de novembro de 2005( leia online , consultado em 12 de novembro de 2007 )
- National Geographic http://news.nationalgeographic.com/news/2005/11/1109_051109_rocketfuel.html
- [Dia, AC; Whiting, MC; Acetona hidrazona; vol 6 | página 10; cv6p0010;]
- [Wiley, RH; Hexner, PE; 3,5-Dimetilpirazol, vol 4, página 351; cv4p0351]
- [Friedman, L; Litle, RL; Reichle, WR; p- toluenossulfonil hidrazida; vol 5; página 1055, cv5p1055]
- [Weinshenker, NM; Shen, CM; Wong, JY; Carbodiimida polimérica; vol 6, páginas 951; (1988); cv6p0951]
- 2013 Usina nuclear derrama produtos químicos em Bay of Fundy Nova Brunswick relata vazamento de produto químico em Bay of Fundy (Canadian Press in Energy and Resources ) 3013-11-05, acessado 3013-11-06
- (en) R. Vieira , " Novo compósito de feltro de nanofibra de carbono / grafite para uso como suporte de catalisador para decomposição catalítica de hidrazina " , Chemical Communications , n o 9,2002, p. 954-955 ( DOI 10.1039 / b202032g )
- (en) Xiaowei Chen , “ Catalytic Decomposition of Hydrazine over Supported Molybdenum Nitride Catalysts in a Monopropellant Thruster ” , Catalysis Letters , vol. 79,Abril de 2002, p. 21-25 ( DOI 10.1023 / A: 1015343922044 )
- " Ativos líquidos - Notícias - O engenheiro - Notícias: notícias de engenharia, informações de engenharia, tecnologia de ponta, notícias de fabricação, informações de fabricação, notícias automotivas, notícias aeroespaciais, notícias de materiais, pesquisa e desenvolvimento " ( Arquivo • Wikiwix • Archive.is • Google • O que fazer? )
- ARC, Monografia, volume 71 (1999) Reavaliação de Alguns Produtos Químicos Orgânicos, Hidrazina e Peróxido de Hidrogênio .
- Sylvie Tissot, Annick Pichard, " Acute toxicity thresholds hydrazine (NH 2 NH 2 ) - Final report " [PDF] , em ineris.fr , Instituto Nacional para o ambiente industrial e riscos ,agosto de 2003(acessado em 29 de outubro de 2015 ) .
Artigos relacionados
links externos
- O último show com Rob! Convidado especial desta noite: Hidrazina (PDF) - Robert Matunas
- xMSDS-Hidrazina-9924279 (PDF) - MSDS para hidrazina
- (fr) Folha toxicológica INRS
- (en) Folha de Dados de Segurança Internacional








