Acetil-coenzima A
| Acetil-coenzima A | |
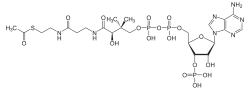  Estrutura da acetil-coenzima A |
|
| Identificação | |
|---|---|
| N o CAS | |
| N o ECHA | 100.000.719 |
| N o EC | 200-790-9 |
| PubChem | 444493 |
| ChEBI | 15351 |
| SORRISOS |
CC (= O) SCCNC (= O) CCNC (= O) C (C (C) (C) COP (= O) (O) OP (= O) (O) OCC1C (C (C (O1) N2C = NC3 = C2N = CN = C3N) O) OP (= O) (O) O) O , |
| InChI |
InChI: InChI = 1 / C23H38N7O17P3S / c1-12 (31) 51-7-6-25-14 (32) 4-5-26-21 (35) 18 (34) 23 (2,3) 9- 44-50 (41,42) 47-49 (39,40) 43-8-13-17 (46-48 (36,37) 38) 16 (33) 22 (45-13) 30-11-29- 15-19 (24) 27-10-28-20 (15) 30 / h 10-11,13,16-18,22,33-34H, 4-9H2,1-3H3, (H, 25,32) (H, 26,35) (H, 39,40) (H, 41,42) (H2,24,27,28) (H2,36,37,38) / t13-, 16-, 17-, 18 +, 22- / m1 / s1 / f / h25-26,36-37 , 39,41H, 24H2 InChIKey: ZSLZBFCDCINBPY-XZFIVJFQDF Std. InChI: InChI = 1S / C23H38N7O17P3S / c1-12 (31) 51-7-6-25-14 (32) 4-5-26-21 (35) 18 (34) 23 (2,3) 9- 44-50 (41,42) 47-49 (39,40) 43-8-13-17 (46-48 (36,37) 38) 16 (33) 22 (45-13) 30-11-29- 15-19 (24) 27-10-28-20 (15) 30 / h 10-11,13,16-18,22,33-34H, 4-9H2,1-3H3, (H, 25,32) (H, 26,35) (H, 39,40) (H, 41,42) (H2,24,27,28) (H2,36,37,38) / t13-, 16-, 17-, 18 +, 22- / m1 / s1 Std. InChIKey: ZSLZBFCDCINBPY-ZSJPKINUSA-N |
| Propriedades quimicas | |
| Fórmula bruta |
C 23 H 38 N 7 O 17 P 3 S [Isômeros] |
| Massa molar | 809,571 ± 0,033 g / mol C 34,12%, H 4,73%, N 12,11%, O 33,6%, P 11,48%, S 3,96%, |
| Unidades de SI e STP, salvo indicação em contrário. | |
A acetil-coenzima A , normalmente escrita acetil-CoA , é a forma "ativada" do ácido acético , ou seja, o tioéster formado por este com o CoA . É uma molécula com alto potencial de hidrólise localizada no cruzamento de várias vias metabólicas importantes. Acetil-CoA pode, portanto, resultar, sob a ação do complexo piruvato desidrogenase , da descarboxilação oxidativa do piruvato , resultante, por exemplo, da glicólise , ou da degradação de ácidos graxos por β-oxidação ( hélice de Lynen ) no quadro da lipólise ( degradação de lipídios ). Ele atua principalmente como um substrato para o ciclo de Krebs ser oxidado a CO 2e coenzimas reduzidas, tais como NADH + H + e ubiquinol ( CoQ 10 H 2), bem como um substrato para vias anabólicas , como a biossíntese de ácidos graxos , após uma série de reações semelhantes ao recíproco da β-oxidação. Durante o jejum prolongado, quando a gliconeogênese reduziu a concentração de oxaloacetato disponível para permitir que o acetil-CoA entre no ciclo de Krebs, o acetil-CoA leva à formação de corpos cetônicos - acetilacetato (H 3 C - CO - CH 2 - COO -), β- D- hidroxibutirato (H 3 C - CHOH - CH 2 -COO -) e acetona (H 3 C - CO - CH 3) - que são usados como fontes de energia metabólica pelos músculos , coração e cérebro . A acetil-CoA também está envolvida na biossíntese da acetilcolina , um neurotransmissor , pela acetilação da colina sob o efeito da colina acetiltransferase .
Funções bioquímicas
Conversão de piruvato em acetil-CoA
A descarboxilação oxidativa do piruvato em acetil-CoA é catalisada pelo complexo piruvato desidrogenase . Existem outras reações que permitem a formação de acetil-CoA a partir do piruvato, como a dismutação do piruvato em acetil-CoA e formato pela piruvato formato liase .
Síntese direta
A acetil-CoA pode ser formada por acetilação direta da coenzima A sob a ação da acetil-CoA sintase do metano CH 4e dióxido de carbono CO 2. Essa reação ocorre, por exemplo, na modulação da expressão gênica pela formação de histonas acetiltransferases que permitem a acetilação de histonas, bem como na via de Wood-Ljungdahl de fixação de carbono em condições anaeróbias utilizando uma enzima cujo sítio ativo contém níquel .
Entrada no ciclo de Krebs
O acetil CoA é produzido tanto pela degradação dos carboidratos por meio da glicólise quanto pela degradação dos ácidos graxos que constituem o lipídio por meio da β-oxidação . Ele entra no ciclo de Krebs com as mitocôndrias através da reacção com o oxaloacetato para formar citrato , com a libertação de um livre coenzima A. A unidade de acetil vendida é oxidada lá em CO 2e coenzimas reduzidas, tais como NADH + H + e ubiquinol ( CoQ 10 H 2) que, por sua vez, são totalmente oxidados a H 2 Oatravés da cadeia respiratória ; a energia liberada por essas oxidações gera um gradiente eletroquímico através da membrana mitocondrial interna que permite a fosforilação de ADP em ATP sob a ação da ATP sintase por acoplamento quimiosmótico .
Formação de cetonas
No fígado , o oxaloacetato pode ser usado para a biossíntese de glicose por gliconeogênese quando em jejum estendido para dieta pobre em carboidratos, esforço físico intenso e prolongado, e diabetes tipo 1 não controlado. Nessas condições, marcadas por alto teor de glucagon e baixíssimo nível de insulina no sangue , o oxaloacetato é reduzido a malato , que deixa a mitocôndria para ser convertida em glicose no citoplasma dos hepatócitos , de onde é produzido. ganha circulação sanguínea . Consequentemente, o oxaloacetato deixa de estar disponível no fígado para condensação com acetil-CoA, de modo que este último condensa consigo mesmo para formar acetoacetil-CoA H 3 C - CO - CH. 2 - COS - CoAe β- D- hidroxibutirato H 3 C - CHOH - CH 2 -COO -, que originam espontaneamente acetona H 3 C - CO - CH 3 : esses três compostos são geralmente chamados de corpos cetônicos . Eles são liberados na corrente sanguínea de onde podem ser absorvidos por qualquer célula do corpo com mitocôndrias : essas células reformam a acetil-CoA desses corpos cetônicos e decompõem essa acetil-CoA em suas mitocôndrias para extrair energia metabólica.
Ao contrário dos ácidos graxos , as cetonas podem cruzar a barreira hematoencefálica e, portanto, também estão disponíveis como compostos energéticos para uso pelo cérebro e pelo sistema nervoso central no lugar da glicose.
A produção de cetonas em resposta ao estresse fisiológico (jejum, dieta pobre em carboidratos, esforço intenso prolongado) é chamada de cetose ; o excesso de cetonas resultante do diabetes tipo 1 é denominado cetoacidose .
Biossíntese de ácidos graxos
Quando a taxa sanguínea da insulina é alta e a do glucagon é baixa (normalmente após as refeições), o acetil-CoA derivado do glicolítico e do oxaloacetato se condensa para formar citrato , que em vez de ser degradado, o ciclo de Krebs deixa a mitocôndria para se juntar ao citoplasma onde é clivado em oxaloacetato e acetil-CoA pela ATP citrato liase . O oxaloacetato retorna às mitocôndrias como malato . A acetil-CoA citosólica pode então ser usada para a biossíntese de ácidos graxos por carboxilação de acetil-CoA em malonil-CoA pela acetil-CoA carboxilase . Essa reação ocorre principalmente no fígado , tecido adiposo e glândulas mamárias , onde os ácidos graxos se ligam ao glicerol para formar triglicerídeos , os principais compostos de armazenamento de energia metabólica na maioria dos animais. Os ácidos graxos também são constituintes dos fosfolipídios , a maior parte das bicamadas lipídicas das membranas biológicas .
Nas plantas , a síntese de novo dos ácidos graxos ocorre nos plastídios . Muitas sementes acumulam grandes reservas de óleos vegetais para promover a germinação e o desenvolvimento da planta até que a planta possa se sustentar por meio da fotossíntese .
Produção de colesterol
O acetil-CoA citosólico também pode condensar com o acetoacetil-CoA para formar 3-hidroxi-3-metilglutaril-CoA (HMG-CoA) pela ação da HMG-CoA sintase , que é a etapa limitante na biossíntese do colesterol via mevalonato . O colesterol age como constituindo membranas biológicas , na biossíntese de hormonas esteróides , os ácidos biliares e vitamina D .
Outros usos
O acetil-CoA também está envolvido em várias outras vias metabólicas :
- como grupo doador de acetil durante a acetilação de certos resíduos de lisina por acetiltransferases durante as modificações pós - tradução de histonas e proteínas não histonas;
- como um precursor de malonil-CoA por carboxilação no citosol sob o efeito da acetil-CoA carboxilase , que abre caminho para a produção de flavonóides e policetídeos relacionados, o alongamento de ácidos graxos para produzir ceras , cutícula e óleo em Brassicaceae , e para a malonização de proteínas e outros fitoquímicos, como sesquiterpenos , brassinosteróides e esteróis de membrana.
Notas e referências
- massa molecular calculada de " pesos atômicos dos elementos 2007 " em www.chem.qmul.ac.uk .
- (em) Hidekazu Takahashi, J. Michael McCaffery, Rafael A. Irizarry e Jef D. Boeke , " Nucleocytosolic acetyl-coenzyme a synthetase is required for histone acetylation and global transcription " , Molecular Cell , Vol. 23, n o 2 21 de julho de 2006, p. 207-217 ( PMID 16857587 , DOI 10.1016 / j.molcel.2006.05.040 , leia online )
- (em) Javier Seravalli, Manoj Kumar e Stephen W. Ragsdale , " Rapid Kinetic Studies of Acetyl-CoA Synthesis: Evidence Supporting the Catalytic Intermediacy of a NiFeC Paramagnetic Species in the Wood-Ljungdahl Pathway autotrophic " , 41 , vol. 6, 12 de fevereiro de 2002, p. 1807-1819 ( PMID 11827525 , DOI 10.1021 / bi011687i , leia online )
- (em) Eric L. Hegg , " Unraveling the Structure and Mechanism of Acetyl-Coenzyme A Synthase " , Accounts of Chemical Research , Vol. 37, n o 10, Outubro de 2004, p. 775-783 ( PMID 15491124 , DOI 10.1021 / ar040002e , leia online )
- (en) P. Ferré e F. Foufelle , “ SREBP-1c transcription factor and lipid homeostasis: Clinic perspective ” , Hormone Research , vol. 68, n o 2 2007, p. 78-82 ( PMID 17344645 , DOI 10.1159 / 000100426 , ler online )
- (em) Beth L. Fatland, Basil J. Nikolau e Eve Syrkin Wurtele , " Reverse Genetic Characterization of Cytosolic Acetyl-CoA Generation by ATP-citrate lyase in Arabidopsis " , The Plant Cell , Vol. 17, n o 1, janeiro de 2005, p. 182-203 ( PMID 15608338 , PMCID 544498 , DOI 10.1105 / tpc.104.026211 , JSTOR 4130763 , ler online )