Desconforto respiratório
Desconforto respiratório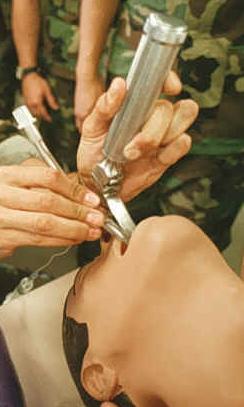 A intubação orotraqueal (mostrada aqui em um manequim) é um tratamento para o desconforto respiratório.
A intubação orotraqueal (mostrada aqui em um manequim) é um tratamento para o desconforto respiratório.
| Especialidade | Medicina de emergência, pneumologia e reanimação. |
|---|
| CISP - 2 | R99 |
|---|---|
| ICD - 10 | J96.0 |
| DiseasesDB | 6623 |
| eMedicine | 167981 |
| eMedicine | med / 2011 |
| Malha | D012131 |
| Sintomas | Dispneia , cianose . |
| Causas | Doença pulmonar , insuficiência cardíaca , síndrome do desconforto respiratório agudo , descompensação da DPOC . |
| Tratamento | Oxigenoterapia e tratamento da causa. |
O desconforto respiratório é uma insuficiência respiratória que ocorre de forma abrupta e se manifesta como dispneia importante (falta de ar). O sistema respiratório não pode mais garantir a troca gasosa normal de oxigênio e dióxido de carbono . É uma emergência médica que pode ser fatal para o paciente e causa cerca de um terço das hospitalizações em unidades de terapia intensiva.
Existem dois tipos principais de desconforto respiratório: hipoxêmico , quando apenas a pressão parcial de oxigênio no sangue arterial é diminuída, e hipercápnico , quando é adicionado um aumento na pressão parcial de dióxido de carbono .
O diagnóstico da dificuldade respiratória é acima de tudo clínico: poucos exames adicionais são necessários, e estes são dominados pela medição do conteúdo de oxigênio do sangue por um saturômetro , o estudo dos gases do sangue por uma amostra arterial e do tórax x -ray . Outros exames permitirão, no entanto, refinar o diagnóstico etiológico e identificar o processo causador da falha.
Adultos e crianças podem sofrer de dificuldade respiratória. Em adultos, infecções pulmonares , descompensações de bronquite crônica , síndrome do desconforto respiratório agudo (SDRA) e insuficiência cardíaca estão entre as causas mais comuns. Em crianças pequenas, a bronquiolite e as infecções pulmonares bacterianas são as mais envolvidas. Em neonatos, a SDRA e a inalação de mecônio estão principalmente envolvidas.
O tratamento do desconforto respiratório é baseado principalmente no suprimento adicional de oxigênio inalado. Isso pode ser realizado em primeiro lugar com óculos de oxigênio , uma máscara de alta concentração ou um sistema de terapia de oxigênio nasal de alto fluxo . Se este tratamento for insuficiente, a assistência ventilatória é configurada. Pode ser não invasivo , por meio de máscara nasolabial que fornece ar pressurizado ao paciente, ou invasivo, por intubação traqueal . Como último recurso, em alguns casos, a oxigenação por membrana extracorpórea (ECMO) pode ser iniciada. A causa da dificuldade respiratória é tratada em paralelo.
O tratamento é seguido principalmente por sintomas, oxímetro de pulso e gasometria arterial.
O prognóstico do desconforto respiratório é muito variável, dependendo da causa. A letalidade geral é de aproximadamente 30% e maior para pacientes em idades extremas de vida, aqueles com comorbidades significativas e aqueles com maior gravidade inicial. Em pacientes sobreviventes, a recuperação da função pulmonar é longa, mas as sequelas respiratórias são geralmente moderadas. A qualidade de vida pode, entretanto, permanecer prejudicada por vários anos.
Epidemiologia
A incidência de dificuldade respiratória é, na Europa Ocidental, entre 78 e 150 por 100.000 habitantes.
Um estudo realizado em 2002 com aproximadamente 1.500 pacientes adultos internados em unidades de terapia intensiva em 16 países descobriu que 32% foram internados por dificuldade respiratória. Entre os pacientes internados por outros motivos, 35% apresentaram dificuldade respiratória durante o curso de sua patologia inicial.
Em relação às crianças, esse é um motivo frequente de admissão em terapia intensiva pediátrica, afetando até dois terços dos pacientes. Em um estudo britânico sobre os motivos de admissão em unidades de terapia intensiva pediátrica, as causas respiratórias afetaram 20% das crianças em 1982, 19% em 1995 e 27% em 2006.
Definição e fisiopatologia
Em geral
A insuficiência respiratória aguda ocorre quando o sistema respiratório falha repentinamente em fornecer a troca gasosa de oxigênio e dióxido de carbono . Geralmente é definido pela análise dos gases dissolvidos no sangue arterial . Uma pressão parcial de oxigênio arterial ( PaO 2 ) inferior a 60 mmHg (ou seja, 8,0 kPa ) é o valor limite usado para definir o estado de hipoxemia . Isso se reflete em uma diminuição da oximetria de pulso , com saturação periférica de oxigênio (SpO 2 ) entre 80 e 94%.
Tipos de dificuldade respiratória
Geralmente distinguimos:
- insuficiência respiratória hipoxêmica , conhecida como "tipo 1",
- insuficiência respiratória hipercápnica , conhecida como "tipo 2".
- Alguns médicos também distinguem entre insuficiência respiratória aguda, conhecida como “tipo 3” (no contexto perioperatório) e “tipo 4” (que ocorre durante um estado de choque hemodinâmico ).
Insuficiência respiratória hipoxêmica
A insuficiência respiratória hipoxêmica pode ocorrer em várias circunstâncias, levando à insuficiência pulmonar: relação ventilação / perfusão inadequada, aparecimento de um efeito de shunt , difusão alveolar-capilar prejudicada ou hipoventilação alveolar.
Insuficiência respiratória hipercápnica
A insuficiência respiratória hipercápnica ocorre durante anormalidades na mecânica ventilatória, impedindo a eliminação de CO 2 . A hipoxemia é então acompanhada por hipercapnia, definida por uma PaCO 2 maior que 45 mmHg (ou seja, 6,0 kPa ). O acúmulo de CO 2 reduz o pH do sangue; uma acidose respiratória se instalou quando se tornou menor que 7,35 .
Caso especial de crianças
As crianças, especialmente as mais jovens, têm maior probabilidade de apresentar problemas respiratórios do que os adultos. Na verdade, as seções menores de suas vias aéreas aumentam a resistência ao fluxo de ar e facilitam a obstrução brônquica por secreções ou edema. A menor rigidez da parede torácica também contribui para o aumento do trabalho ventilatório. O diafragma e os músculos respiratórios acessórios também contêm fibras musculares menos lentas do que as do adulto, o que facilita a exaustão respiratória. Finalmente, crianças muito pequenas têm um sistema nervoso imaturo que as predispõe à apnéia e bradipnéia .
Sinais clínicos
O diagnóstico de dificuldade respiratória é principalmente clínico e pode ser estabelecido diretamente à beira do leito do paciente. O quadro clínico combina as consequências diretas do ataque ao sistema respiratório e as medidas compensatórias implementadas pelo organismo.
Os sinais de esforço são dominados por um aumento da frequência respiratória ( polipneia ), que pode estar associado à tensão dos músculos respiratórios.
Os sinais de gravidade, também chamados de falência, variam de acordo com os órgãos afetados. Eles refletem o impacto global do desconforto respiratório e na maioria das vezes indicam a necessidade de assistência ventilatória. No nível respiratório, respiração abdominal paradoxal e cianose são os principais sinais. Este último pode estar ausente na anemia grave, se o nível de hemoglobina for inferior a 5 g · dl -1 . Neurologicamente, a hipercapnia, quando presente, causa asterixia e distúrbios do estado de alerta e do comportamento (agitação ou coma). Finalmente, no plano circulatório, o cor pulmonale agudo é uma insuficiência cardíaca direita. É acompanhado por pulso paradoxal e pode estar associado a insuficiência cardiovascular até choque .
Quando há hipercapnia , o quadro pode ser complementado por sudorese profusa.
Pacientes, adultos e crianças, portadores de doenças neuromusculares, podem apresentar poucos sinais clínicos; nessas populações, o desconforto respiratório deve ser facilmente evocado e a medição dos gases arteriais realizada. Em idosos, sinais clínicos menos claros podem levar a divagações diagnósticas.
Testes adicionais
As medições das constantes fisiológicas ( frequência cardíaca e respiratória , pressão arterial , saturação de oxigênio ) completam o exame clínico e permitem uma avaliação rápida da gravidade da situação. Poucos exames adicionais são necessários para estabelecer o diagnóstico de dificuldade respiratória. Em situações de emergência, a radiografia de tórax e a gasometria arterial são os únicos exames necessários para o diagnóstico. De acordo com os primeiros elementos de orientação, outros exames podem, no entanto, ser realizados para especificar a causa da dificuldade respiratória. No entanto, eles não devem atrasar o início do tratamento.
O exame de sangue padrão pode apontar para uma causa: hiperleucocitose no caso de infecção bacteriana, aumento da PCR no caso de inflamação, aumento do dímero D no caso de embolia pulmonar , BNP no caso de insuficiência cardíaca.
O ecocardiograma e o pleural podem ser úteis na diferenciação das causas da insuficiência respiratória hipoxêmica. A tomografia computadorizada (TC) de tórax pode observar embolia pulmonar, sinais de fibrose ou especificar lesões mais finas visualizadas na radiografia de tórax. Em um contexto infeccioso (febre ou escarro purulento), a análise do escarro , assim como as hemoculturas podem possibilitar a busca dos germes responsáveis. A gripe é sistematicamente procurada durante epidemias no paciente febril.
A broncoscopia pode ser indicada quando a causa do desconforto respiratório não for óbvia. Permite colher amostras para fins bacteriológicos, mas também para explorar a morfologia da árvore brônquica através da realização de biópsias, se necessário, e da lavagem broncoalveolar .
Procedimento de diagnóstico
Existem muitas causas de dificuldade respiratória. O diagnóstico etiológico é baseado no exame clínico, complementado por radiografia de tórax e análise de gases arteriais.
A primeira etapa do diagnóstico é verificar a liberdade das vias aéreas superiores. Este diagnóstico é clínico. A inalação de um corpo estranho é a causa mais comum em crianças e idosos com distúrbios de deglutição, mas qualquer doença que resulte em obstrução otorrinolaringológica ou laríngea pode estar envolvida. Tumor laríngeo , estenose traqueal rígida, epiglotite ou angioedema podem, portanto, estar envolvidos. Quando as vias aéreas estão livres, as radiografias de tórax e a ausculta podem diagnosticar danos à pleura e ao parênquima pulmonar . No nível pleural, qualquer derrame de grande abundância ( pneumotórax ou derrame de fluido ) pode causar dificuldade respiratória. Em nível pulmonar, uma atelectasia é a ausência de ventilação de um território mais ou menos importante, muitas vezes por obstrução mecânica. As doenças pulmonares , particularmente bacterianas, que afetam um volume pulmonar significativo, são causa comum de dificuldade respiratória, assim como edema pulmonar, seja cardíaco ( edema agudo de pulmão ) ou lesão ( síndrome da dificuldade respiratória aguda ou SDRA). Neste último caso, é importante observar que a pneumonia, seja bacteriana ou viral (por exemplo, Covid-19 ), é provavelmente a causa da SDRA. Finalmente, os ataques de doença pulmonar intersticial podem ser a causa de dificuldade respiratória. Em pacientes em tratamento para doença cancerosa, é importante especificar a data da última quimioterapia e, se for o caso, do transplante de medula óssea . Na verdade, é provável que esses tratamentos levem à imunossupressão e, então, infecções oportunistas devem ser procuradas.
Quando a radiografia e o exame clínico são pouco úteis, a medida do gás arterial permite orientar o diagnóstico. A normalidade da capnia (pressão de CO 2 ) e do pH aponta para uma embolia pulmonar ou asma aguda grave . A embolia será pesquisada por uma tomografia computadorizada de tórax; o exame físico pode ser muito áspero, mas também inclui sinais de insuficiência cardíaca direita e cor pulmonale agudo, especialmente em casos de embolia maciça e proximal. Quando as medições de gases indicam acidose respiratória, que se manifesta como aumento de capnia e bicarbonatos, o desconforto respiratório geralmente resulta da descompensação de uma patologia crônica. Na maioria das vezes, é a exacerbação da doença pulmonar obstrutiva crônica (DPOC). Danos neuromusculares, como miastenia gravis ou síndrome de Guillain-Barré, podem estar envolvidos. A poliomielite era uma causa comum até a introdução da vacina; a ventilação pulmonar dos pacientes era então assegurada, após a fase aguda, por um pulmão de aço . Finalmente, o dano parietal também pode ser responsável pelo desconforto respiratório. As múltiplas fraturas de costelas podem estar envolvidas, principalmente em pacientes cujo estado ventilatório básico é precário. As miopatias , sejam congênitas ou adquiridas, às vezes também estão envolvidas, por uma infração dos músculos inspiratórios. No caso dessas doenças crônicas, é necessário procurar o elemento que causou a descompensação: superinfecção brônquica, embolia pulmonar, pneumopatia, cirurgia torácica ou insuficiência cardíaca esquerda também podem ser responsáveis pelo desconforto respiratório. A intoxicação por opiáceos ou outras substâncias com efeito depressor respiratório também pode estar envolvida.
Causas
O desconforto respiratório é induzido pela falta de surfactante pulmonar (surfactante cujas proteínas do surfactante não só facilitam a troca de oxigênio e CO2, mas protegem contra vírus como o influenza A ). Essa deficiência de surfactante pode ter múltiplas causas, às vezes exacerbadas em homens porque a produção de surfactante pulmonar está ligada ao sistema hormonal e controlada principalmente pelo cromossomo X (humanos têm apenas um). É, por exemplo, inibido pela diidrotestosterona no feto masculino e feminino. Por outro lado, um antiandrogênio (por exemplo, flutamida ) suprime o dimorfismo sexual na produção de surfactantes.
Em adultos
Em adultos, devido a estudos muito heterogêneos, faltam dados sobre a distribuição global das várias causas de dificuldade respiratória.
Um estudo de 1995 em uma coorte alemã encontrou infecções pulmonares (15%, incluindo pneumonia por aspiração ) como a etiologia mais comum, seguida por causas cardíacas com choque cardiogênico (13%) e insuficiência cardíaca esquerda (7,6%).
Uma coorte escandinava estudada em 1999 encontrou infecções pulmonares (23%) como a causa primária, seguidas por atelectasia (15%) e descompensações de doença pulmonar obstrutiva crônica (13%) e, em seguida, insuficiência cardíaca esquerda (9%); choque cardiogênico estando envolvido em apenas 5% dos casos.
A análise de uma coorte brasileira em 2011 realizada em unidades médicas e cirúrgicas intensivos encontrado, como a principal causa médica de angústia respiratória, síndrome de angústia respiratória aguda (SDRA) (10%) seguido por pneumonia (8%).), Não- sepse pulmonar (7%), insuficiência cardíaca (6%) e trauma torácico (6%). No entanto, a maioria dos pacientes (38%) desenvolveu insuficiência respiratória aguda imediatamente após a cirurgia.
A pneumonia bacteriana adquirida na comunidade envolve hospitalização em apenas 20% dos casos; apenas 10% dos quais apresentarão dificuldade respiratória. Já em pacientes imunocomprometidos , o desconforto respiratório é o primeiro motivo de internação em terapia intensiva e terapia intensiva, principalmente por causa de infecções pulmonares; pode ser tanto clássica comunidade - suportados pneumonia, bem como infecções oportunistas , em particular infecções fúngicas. Mais raramente, pode ser um efeito colateral de alguns tratamentos de câncer, particularmente quimioterapia e certas terapias direcionadas podem ser responsáveis por pneumonite por hipersensibilidade como pneumonite intersticial . Em pacientes com câncer ativo, entretanto, a pneumonite bacteriana é a causa mais comum (47%), seguida por infecções oportunistas (31%), e em 22% dos casos por causas não infecciosas.
A SDRA preocupa entre 1,7 e 19,5% de todos os pacientes internados em unidades de terapia intensiva para adultos, com números mais frequentemente relatados em torno de 7%.
Na doença pulmonar intersticial , como fibrose pulmonar idiopática , a dificuldade respiratória pode ocorrer em dois casos principais. Em pacientes já diagnosticados, a exacerbação aguda corresponde à deterioração, por menos de um mês, do estado respiratório e das lesões observadas nos exames de imagem, sem patologia pulmonar associada. O desconforto respiratório pode, entretanto, ser o modo de descoberta de doença intersticial, em particular para fibrose pulmonar idiopática, conectivite e vasculite com envolvimento pulmonar e fibrose induzida por drogas.
Em crianças
A principal causa de dificuldade respiratória em recém-nascidos ( geralmente bebês prematuros ) é a deficiência de surfactante pulmonar . Essa angústia pode ser evitada com corticoterapia pré-natal (que, no entanto, é mais eficaz em meninas do que em meninos); essa diferença na produção de surfactante pulmonar fetal de acordo com o sexo também é observada no modelo animal , a priori influenciada pelo receptor de andrógeno (AR).
Esse tratamento reduziu significativamente o número de doenças da membrana hialina e contribuiu para a redução da mortalidade infantil (menor morbidade e mortalidade de bebês prematuros).
Em neonatos de curto prazo, a causa mais comum de insuficiência respiratória é SDRA, em 43% dos pacientes, seguida por inalação de mecônio (9,7%) e pneumonia ou sepse (8,3%). A taquipneia transitória do recém - nascido está envolvida em 4% dos casos, mas é particularmente comum em crianças nascidas por cesariana, mesmo em crianças nascidas a termo. Na ausência da passagem do feto no canal do parto contraído, os pulmões não são enxaguados do fluido pulmonar fetal que contêm.
Mais raramente, algumas doenças cardíacas congênitas também podem causar dificuldade respiratória.
Em crianças pequenas, a bronquiolite é responsável por 26,7% do desconforto respiratório e a pneumonia bacteriana 15,8%. Os edemas pulmonares lesionais são responsáveis por cerca de 10% dos casos, sendo a SDRA causando pouco mais da metade deles.
A criança asmática é menos responsável pelo desconforto respiratório devido ao surgimento de novos DMARDs.
Suportado
Esta é uma emergência médica . O desconforto respiratório requer atendimento hospitalar, com transporte médico. Dependendo da condição do paciente, pode haver internação direta em terapia intensiva. O paciente deve ser colocado em repouso, se possível em uma posição semissentada. Uma infusão intravenosa é configurada.
Em caso de inalação de corpo estranho , e se o paciente estiver asfixiante ou não apresentar tosse efetiva, a manobra de Heimlich deve ser realizada com urgência.
Terapia de oxigênio
Devido à urgência vital do desconforto respiratório, o tratamento é iniciado na fase pré-hospitalar. Depois de garantir a liberdade das vias aéreas superiores, o primeiro tratamento de emergência é a oxigenoterapia . Isso pode ser feito de várias maneiras, dependendo da gravidade: óculos, máscara facial de alta concentração, sistema de alto fluxo nasal.
O principal fator limitante na terapia de oxigênio por máscara de alta concentração é o fluxo de oxigênio. Se pode chegar a 15 l / min , sua eficácia clínica é limitada pelos fluxos ventilatórios que o paciente consegue mobilizar. Na verdade, quando o pico de fluxo inspiratório é maior do que o fluxo de oxigênio fornecido, o volume de ar inspirado é suplementado pelo ar da sala.
Os sistemas de terapia de oxigênio nasal de alto fluxo , até 60 l / min , superam essa limitação específica, permitindo que o paciente inale apenas a mistura de gás fornecida. Eles são complementados por um umidificador e um aquecedor permitindo uma melhor tolerância do gás fornecido. Suas cânulas nasais também são mais bem toleradas pelos pacientes do que as máscaras faciais de alta concentração. Esses sistemas foram usados pela primeira vez em pediatria, mas agora são estendidos para adultos. Reservados para pacientes com atividade ventilatória espontânea suficiente, eles podem impedir a mudança para assistência ventilatória genuína. No entanto, os inúmeros vieses dos estudos realizados em adultos não permitem avaliar a eficácia do tratamento em relação à oxigenoterapia convencional.
Assistência ventilatória
A assistência de ventilação é necessária quando a gravidade da dificuldade respiratória é fatal e um ou mais sinais de falha são observados. Também pode ser iniciada pelos critérios gasométricos de hipoxemia resistente à oxigenoterapia ou acidose respiratória por hipercapnia acrescida.
A assistência ventilatória pode ser fornecida de duas formas: ventilação não invasiva e intubação traqueal. A ventilação não invasiva pode ser feita na sala de emergência ou em uma unidade de terapia intensiva. A ventilação invasiva após a intubação é realizada na unidade de terapia intensiva.
Ventilação não invasivaA ventilação não invasiva (VNI) possui todos os métodos de ventilação mecânica que não utilizam o primeiro endotraqueal onde a máscara nasobucal traz o ar sob pressão positiva. Ao aliviar a carga de trabalho dos músculos peitorais, evita a exaustão respiratória. A pressão expiratória positiva que fornece também permite o recrutamento de alvéolos pulmonares.
A VNI é reservada para insuficiência respiratória isolada em pacientes cooperativos e deve ser iniciada precocemente, sem esperar o início da acidose. É contra-indicado em pacientes com traumas na face ou vias aéreas superiores, traumas graves no cérebro e em casos de instabilidade hemodinâmica .
A principal vantagem das técnicas de VNI é evitar as complicações da intubação e ajudar a restaurar a mecânica ventilatória fisiológica. A taxa de falha, definida pela necessidade de intubação traqueal, é baixa. O sucesso de um tratamento de VNI é medido pela diminuição da frequência respiratória, o aumento dos volumes de ar inspirado, a melhora da vigilância, um menor uso dos músculos inspiratórios acessórios, e em termos de medição de gás por uma correção de hipoxemia e hipercapnia.
O desenvolvimento de técnicas de VNI desde a década de 1990 tornou possível reduzir o número de intubações. Na SDRA, o uso de VNI evita cerca de 50% das intubações. A VNI é recomendada como tratamento de primeira linha para descompensações da DPOC, onde reduz o número de intubações em 65% e reduz a mortalidade em 46%. No edema agudo de pulmão, a VNI reduz o risco relativo de mortalidade hospitalar, a taxa de intubação e o tempo de internação. Também é de grande utilidade no tratamento de traumas contusos no tórax, com redução significativa da mortalidade (3% vs. 22%). Em relação às patologias neuromusculares, a VNI é frequentemente utilizada, mas a falta de estudos randomizados limita a possibilidade de recomendações. Seu uso na asma é controverso, e é recomendado não usá-lo como tratamento de primeira linha em patologias pulmonares intersticiais, devido à piora frequentemente rápida dos pacientes. No entanto, a VNI tem função preventiva pós-operatória após cirurgia abdominal supra-mesocólica, onde possibilita a redução do número de intubações. Seu uso preventivo em cirurgia torácica é pouco comprovado.
O uso de uma sedação leve para melhorar a tolerância à VNI, em particular no recém-nascido, é delicado devido ao caráter depressor respiratório dos medicamentos utilizados. A ausência da necessidade de sedação, ao contrário da intubação, também é considerada uma das vantagens da técnica. Quando a sedação leve é usada, o monitoramento deve ser mais frequente. Vários fatores de risco para falha da VNI foram identificados: assincronia entre o paciente e a máquina, claustrofobia, presença de depressores respiratórios e a habitual falta de equipes de atendimento.
Quando a ventilação não invasiva não é possível, ou não melhora o paciente, a intubação traqueal é necessária. A reavaliação da VNI deve ser precoce, 30 minutos a 2 horas após seu início, para não atrasar uma intubação que se torne necessária.
Ventilação invasivaA ventilação invasiva combina intubação traqueal e traqueostomia , duas técnicas cujo objetivo é levar a mistura gasosa diretamente para a traqueia do paciente. Um paciente com vigilância prejudicada ou outra contra-indicação para VNI pode se beneficiar da intubação durante o tratamento. Além disso, em caso de obstrução das vias aéreas superiores, como por estenose laríngea ou traquéia , a ventilação invasiva elimina a barreira para ventilar efetivamente o paciente. No contexto particular das patologias intersticiais, cujas lesões são consideradas irreversíveis, a necessidade de ventilação invasiva está associada a tal gravidade da doença que alguns recomendam intubar apenas os pacientes que poderiam se beneficiar de um transplante de pulmão. Nesses pacientes, é recomendado evitar a ventilação invasiva potencialmente irracional, tanto quanto possível.
Vários modos de ventilação mecânica podem ser usados, dependendo da presença ou não de sedação, mas também dependendo da doença de base. Os dois modos principais usados são ventilação controlada e ventilação assistida. Na assistência ventilatória, é a inspiração espontânea do paciente que aciona o ciclo da máquina. Um limite de frequência é geralmente definido: quando o paciente leva muito tempo para inspirar, a máquina inicia seu ciclo. Ao contrário, na ventilação controlada, o respirador fornece um volume ou pressão fixa em uma determinada frequência; isso requer sedação do paciente para evitar problemas com o ventilador . Nesse caso, a sedação deve ser interrompida periodicamente para avaliar a capacidade do paciente de ventilar espontaneamente. Em caso de atelectasia , as manobras de recrutamento pulmonar, que consistem no aumento da pressão por um longo período de tempo, são ora recomendadas (com baixo nível de evidência), ou mesmo consideradas como medida preventiva.
Se a intubação for prolongada, uma traqueostomia pode ser realizada. Cerca de 12% dos pacientes com dificuldade respiratória precisarão de uma traqueostomia. O tempo médio durante o qual a traqueostomia é mantida no local é de seis dias.
A ventilação endotraqueal ajuda a proteger as vias aéreas da inalação de saliva ou fluido gástrico. A aspiração das secreções brônquicas também é facilitada.
Devido à sua natureza invasiva, tanto a intubação quanto a traqueostomia podem ser fontes de complicações, principalmente pneumonias adquiridas em ventilação mecânica . Essas são as infecções nosocomiais mais frequentes na terapia intensiva.
De 7 a 28% das crianças com bronquiolite precisam de intubação. Para asma infantil, 5 a 17% dos ataques de asma aguda grave requerem intubação.
Oxigenação por membrana extracorpórea (ECMO)
Se apesar de tudo, a assistência ventilatória não garante oxigenação e descarboxilação corretas, a oxigenação por membrana extracorpórea (ECMO) pode ser iniciada no ambiente de terapia intensiva. Um circuito de ECMO é composto de cânulas para drenar e, em seguida, reinjetar o sangue do paciente, uma bomba e uma membrana que permite a troca gasosa. Nas falhas respiratórias, a chamada ECMO venoso-venosa é preferencialmente usada. O sangue é então drenado da veia cava ou do átrio direito do coração e reinjetado no átrio direito após oxigenação e descarboxilação. Duas cânulas diferentes podem ser colocadas, mas também há cânulas de duplo fluxo, permitindo que o sangue seja coletado na entrada do átrio direito e reinjetado próximo à válvula tricúspide . Em seguida, ele se mistura com o fluxo sanguíneo que não foi integrado ao circuito da bomba.
Alguns sistemas permitem apenas a descarboxilação, sendo a troca de CO 2 através da membrana mais fácil do que a de oxigênio. Isso é especialmente usado em descompensações de DPOC e asma grave, onde a hipercapnia pode ser maior e mais prejudicial do que a hipoxemia. Mais excepcionalmente, a ECMO pode ser usada para permitir a espera por um transplante de pulmão nos casos em que isso for indicado.
Em crianças, o uso de ECMO em populações pediátricas é debatido em certas indicações, notadamente na SDRA, onde parece não melhorar a sobrevida. Por outro lado, em recém-nascidos, seu uso continua recomendado.
A duração do uso de uma ECMO é geralmente inferior a 28 dias (84-88% dos pacientes), com uma duração média de sete a oito dias. As patologias respiratórias intersticiais geralmente requerem tempos de assistência mais longos. O motivo mais comum para a retirada da ECMO é a recuperação da função respiratória em 54% dos pacientes. No entanto, a ocorrência de complicações pode exigir a descontinuação da ECMO.
Embora as complicações neurológicas sejam menos frequentes na ECMO venoso-venosa do que em outras formas de assistência circulatória, ainda afetam 8,5% dos pacientes adultos e até 20% dos recém-nascidos. Essas complicações neurológicas são dominadas por hemorragias intracranianas (42%), acidente vascular cerebral (20%) e morte encefálica (23,5%). Na verdade, para evitar a coagulação do sangue no circuito da ECMO, é necessária uma anticoagulação em dose curativa. Podem ocorrer complicações tanto trombóticas quanto hemorrágicas.
A taxa de sobrevida geral dos pacientes que necessitaram de ECMO para insuficiência respiratória é muito heterogênea de acordo com os estudos. Em adultos, é entre 32 e 90%. Em recém-nascidos, a sobrevida é de 18 a 50%, enquanto em crianças é de 22 a 66%.
Desmame ventilatório
Após o episódio agudo ter passado, o suporte ventilatório deve ser suspenso o mais rápido possível.
Quando um paciente é intubado, essa fase de desmame ventilatório pode ser complexa. Às vezes, uma traqueostomia pode ser realizada; ao reduzir o trabalho ventilatório, torna-se mais fácil para o paciente. Não há recomendação sobre quanto tempo para colocar uma traqueostomia; a análise deve ser feita caso a caso.
Antes da retirada da ventilação invasiva, um ou mais testes de retirada são realizados. A assistência mecânica é então reduzida ao mínimo e a ventilação espontânea do paciente é monitorada. Medição de gás, estabilidade hemodinâmica e conforto do paciente também são monitorados. Se o teste de desmame falhar, o suporte ventilatório deve ser retomado por pelo menos 24 horas.
Depois que o teste de desmame for bem-sucedido, várias etapas devem ser executadas antes da extubação. O paciente deve ser capaz de tossir eficazmente por conta própria, estar bem acordado e ter pouca secreção brônquica.
Após a extubação, o suporte por VNI pode ser realizado. Isso ajuda a reduzir o risco de reintubação. Isso é particularmente adequado em pacientes com fatores de risco para falha de extubação, como hipercapnia, insuficiência cardíaca e tosse ineficaz, e até mesmo recomendado em pacientes com DPOC. A VNI é então interrompida quando não há mais sinais clínicos ou gasométricos de insuficiência respiratória.
Também é possível usar oxigenoterapia nasal de alto fluxo em vez de VNI após a extubação, especialmente em crianças e bebês prematuros.
Outros tratamentos
Dependendo da causa do desconforto respiratório, outros tratamentos mais específicos serão introduzidos: antibioticoterapia para pneumonite bacteriana, corticoterapia, etc. Um derrame pleural abundante deve ser drenado . A embolia pulmonar requer anticoagulação e, às vezes, fibrinólise . A asma aguda grave será tratada com broncodilatadores . Pacientes com trauma torácico também se beneficiam de analgesia peridural . Nas descompensações de miastenia gravis, é necessária plasmaférese ou tratamento com imunoglobulinas. Quando é observada desnutrição , ela deve ser tratada da maneira usual.
A fisioterapia respiratória diária é uma parte importante do manejo. Em pacientes conscientes, facilita a drenagem brônquica e melhora a capacidade respiratória, reduzindo a atelectasia. Em um nível mais geral, a fisioterapia também permite lutar contra a neuropatia da terapia intensiva , perda de autonomia e complicações de decúbito, como escaras .
Ficar de pé e levantar na cadeira (ou pelo menos levantar a cabeceira da cama em pacientes sob ventilação invasiva) são comumente praticados.
Monitoramento e acompanhamento
Desde a década de 1980, a oximetria de pulso tornou possível monitorar de forma não invasiva a saturação periférica de oxigênio. No entanto, sua confiabilidade é enfraquecida no caso de má perfusão do tecido (por exemplo, durante um estado de choque circulatório), uso de tratamentos vasoconstritores como norepinefrina ou mesmo hipotermia . As decisões terapêuticas em relação à assistência ventilatória devem, portanto, ser tomadas com base na medida direta de PaO 2 , pH e PaCO 2, por meio da medida do gás arterial, que continua sendo o exame de referência. Embora o sangue capilar possa ser usado para estimar esses valores, as amostras de sangue venoso periférico são inadequadas para essas medições.
A relação P / F é calculada dividindo a PaO 2 pela fração de oxigênio no ar inspirado. Permite acompanhar a evolução dos edemas pulmonares lesionais, em especial a SDRA .
Em caso de assistência ventilatória, em particular intubação, é possível monitorar indiretamente a capnia por meio da capnografia . Trata-se da análise dos gases exalados, possibilitando a quantificação do CO 2 expirado.
O acompanhamento diário da radiografia de tórax é debatido no paciente em ventilação mecânica, devido à má qualidade das imagens obtidas na posição deitada. No entanto, é necessário fazer uma radiografia após a colocação de uma sonda de intubação ou de um cateter venoso central para verificar sua posição, e mantém um valor de exame de limpeza durante o acompanhamento.
Prognóstico
Mortalidade
O prognóstico da insuficiência respiratória aguda é muito dependente da causa, bem como da gravidade inicial.
A mortalidade geral de adultos com dificuldade respiratória é de 31%. Os fatores gerais de mau prognóstico são a presença de comorbidades significativas e desnutrição. Nas patologias pulmonares intersticiais, o prognóstico é extremamente ruim, com mortalidade intra-hospitalar geral de 50%, que pode chegar a 96%, e expectativa de vida raramente superior a seis meses. Dos pacientes que conseguem deixar o hospital, 42% morrem em um ano. A mortalidade de adultos com SDRA é de 35-45%.
Em crianças, a mortalidade geral é altamente variável dependendo da série, variando de 24 a 34%. Em 2012, as infecções pulmonares foram responsáveis por 2% da mortalidade entre crianças menores de cinco anos nos Estados Unidos, em comparação com 18% em todo o mundo. A mortalidade geral das crianças que apresentam edema pulmonar lesional é, porém, maior, próxima à dos adultos (27%). Os fatores de mau prognóstico são a idade extrema da vida e a presença de comorbidades, principalmente as doenças respiratórias crônicas e a imunossupressão. Por exemplo, a mortalidade pode chegar a 90% em pacientes jovens com leucemia.
Na população pediátrica, a sobrevida global dos pacientes que requerem ECMO é de 57%, com grandes variações dependendo da causa do desconforto respiratório: os pacientes com coqueluche sobrevivem apenas em 39% dos casos, em comparação com 83% dos pacientes.
Sequelas
Pacientes, adultos ou crianças, que experimentaram um episódio de dificuldade respiratória têm maior risco de desenvolver doença pulmonar crônica, seja obstrutiva (como asma , DPOC , enfisema pulmonar ) ou restritiva .
A recuperação da função pulmonar é lenta, até um ano após a alta hospitalar. O dano observado inicialmente pode ser uma síndrome obstrutiva, restritiva ou mista, com ou sem redução da difusão alvéolo-capilar. Na maioria das vezes, é moderado e poucos pacientes se queixam de dispneia.
Nutricionalmente, os pacientes perderam em média 18% do peso corporal na alta da unidade de monitoramento contínuo , mas 71% recuperaram o peso saudável em um ano. Se a qualidade de vida é prejudicada na alta da internação, tende a melhorar durante o ano seguinte. Cinco anos após a SDRA, os pacientes adultos apresentam função pulmonar subnormal. No entanto, eles ainda apresentam uma limitação ao exercício e uma qualidade de vida prejudicada.
Em crianças, faltam dados sobre as sequelas cognitivas de longo prazo.
Referências
- Klaus Lewandowski , “ Contribuições para a epidemiologia da insuficiência respiratória aguda ”, Critical Care , vol. 7, n o 4,2003, p. 288–290 ( ISSN 1364-8535 , PMID 12930552 , ler online , acessado em 27 de dezembro de 2019 ).
- (en) O grupo de estudo FINNALI , Rita Linko , Marjatta Okkonen e Ville Pettilä , “ Insuficiência respiratória aguda em unidades de terapia intensiva. FINNALI: um estudo de coorte prospectivo ” , Intensive Care Medicine , vol. 35, n o 8,agosto de 2009, p. 1352–1361 ( ISSN 0342-4642 e 1432-1238 , DOI 10.1007 / s00134-009-1519-z , ler online , acessado em 20 de janeiro de 2020 ).
- (en) Jean-Louis Vincent , Serdar Akça , Arnaldo de Mendonça e Philip Haji-Michael , “ A Epidemiologia da Insuficiência Respiratória Aguda em pacientes criticamente doentes ” , Peito , vol. 121, n o 5,Maio de 2002, p. 1602–1609 ( DOI 10.1378 / chest.121.5.1602 , ler online , acessado em 19 de dezembro de 2019 ).
- Schneider et al 2012 ..
- (en) Poongundran Namachivayam , Frank Shann , Lara Shekerdemian e Anna Taylor , " Três décadas de terapia intensiva pediátrica: quem foi internado, o que aconteceu na terapia intensiva e o que aconteceu depois *: " , Pediatric Critical Care Medicine , voar. 11, n o 5,setembro de 2010, p. 549–555 ( ISSN 1529-7535 , DOI 10.1097 / PCC.0b013e3181ce7427 , ler online , acessado em 13 de janeiro de 2020 ).
- Faculdade de Professores de Pneumologia, " Aflição respiratória em adultos " (acessado em 9 de fevereiro de 2020 ) .
- Roussos et al 2003 ..
- Michael E. Hanley e Roger C. osso “ insuficiência respiratória aguda ”, Postgraduate Medicine , vol. 79, n o 1,1 r janeiro 1986, p. 166-176 ( ISSN 0032-5481 , DOI 10,1080 / 00325481.1986.11699244 , lido on-line , acessado 14 de janeiro, 2020 ).
- Friedman et ai 2018 .
- Rajnish K. Gupta e David A. Ewards, “ Monitoring Respiratory Depression Due to Opiates, ” on Anesthesia Patient Safety Foundation ,junho de 2018(acessado em 7 de janeiro de 2020 ) .
- Markou et al 2004 .
- (em) Bishwajit Bhattacharya e Kimberly Davis , "Avaliação e Gerenciamento de Angústia Respiratória Aguda na UTI" em Terapia de Cuidados Críticos Cirúrgicos , Springer International Publishing,2018( ISBN 978-3-319-71711-1 , DOI 10.1007 / 978-319-71712-8_15 , ler online ) , p. 161-169.
- (pt) Jean-Yves Fagon , " Insuficiência respiratória aguda em idosos " , Critical Care , vol. 10, n o 4,2006, p. 151 ( PMID 16887005 , PMCID PMC1751014 , DOI 10.1186 / cc4982 , ler online , acessado em 27 de dezembro de 2019 ).
- (in) Hiroshi Sekiguchi , Louis A. Schenck , Ryohei Horie e Jun Suzuki , " Ultrassonografia em cuidados críticos diferencia ARDS, edema pulmonar e outras causas no início do curso de hipoxemia por insuficiência respiratória aguda " , Chest , Vol. 148, n o 4,outubro de 2015, p. 912-918 ( DOI 10.1378 / chest.15-0341 , ler online , acessado em 14 de janeiro de 2020 ).
- (en) Jonathan Dakin e Mark Griffiths , “ O médico pulmonar em cuidados intensivos 1: Investigações pulmonares para insuficiência respiratória aguda ” , Thorax , vol. 57, n o 1,1 ° de janeiro de 2002, p. 79-85 ( PMID 11809996 , PMCID PMC1746170 , DOI 10.1136 / tórax.57.1.79 , ler online , acessado em 20 de janeiro de 2020 ).
- (en) David Schnell , Julien Mayaux , Jérôme Lambert e Antoine Roux , “ Avaliação clínica para identificar causas de insuficiência respiratória aguda em pacientes com câncer ” , European Respiratory Journal , vol. 42, n o 2agosto de 2013, p. 435-443 ( ISSN 0903-1936 e 1399-3003 , DOI 10.1183 / 09031936.00122512 , lido online , acessado em 14 de janeiro de 2020 ).
- (en) Paola Faverio , MIRA De Giacomi , Luca Sardella e Giuseppe Fiorentino , “ Gestão de insuficiência respiratória aguda em doenças pulmonares intersticiais: visão geral e insights clínicos ” , BMC Pulmonary Medicine , vol. 18, n o 1,dezembro de 2018, p. 70 ( ISSN 1471-2466 , PMID 29764401 , PMCID PMC5952859 , DOI 10.1186 / s12890-018-0643-3 , ler online , acessado em 16 de janeiro de 2020 ).
- (em) Albert Dahan , Leon Aarts e Terry W. Smith , " Impact, Reversal, and Prevention of Opioid-Induced Respiratory Depression: " , Anesthesiology , vol. 112, n o 1,janeiro de 2010, p. 226-238 ( ISSN 0003-3022 , DOI 10.1097 / ALN.0b013e3181c38c25 , ler online , acessado em 7 de janeiro de 2020 ).
- (in) KL Hartshorn , EC Crouch , R. White e P Eggleton , " Evidence for a função protetora da proteína D surfactante pulmonar (SP-D) contra vírus influenza A. ” , Journal of Clinical Investigation , vol. 94, n o 1,1 r jul 1994, p. 311–319 ( ISSN 0021-9738 , PMID 8040272 , PMCID PMC296311 , DOI 10.1172 / JCI117323 , ler online , acessado em 14 de maio de 2020 )
- (em) Heber C. Nielsen , Sr. Howard Zinman e John S. Torday , " Dihydrotestosterone Inhibits Rabbit Fetal Pulmonary Surfactant Production " , Journal of Clinical Investigation , Vol. 69, n o 3,1 st março 1982, p. 611-616 ( ISSN 0021-9738 , PMID 6916770 , PMCID PMC371018 , DOI 10.1172 / JCI110488 , ler online , acessado em 14 de maio de 2020 )
- (em) Kuiama Lewandowski , Jutta Metz , Christel Deutschmann , Heinrich Preiss , Ralf Kuhlen , Antonio Artigas e Konrad J. Falke , " Incidência, gravidade e mortalidade de insuficiência respiratória aguda em Berlim, Alemanha. ” , American Journal of Respiratory and Critical Care Medicine , vol. 151, n o 4,Abril de 1995, p. 1121-1125 ( ISSN 1073-449X e 1535-4970 , DOI 10.1164 / ajrccm.151.4.7697241 , ler online , acessado em 20 de janeiro de 2020 ).
- (in) Owe R. Luhr , Kristian Antonsen , Magnus Karlsson e Sidsel Aardal , " Incidence and Mortality after-Acute Respiratory Failure and Acute Respiratory Distress Syndrome in Sweden, Denmark, and Iceland " , American Journal of Respiratory and Critical Care Medicine , vôo. 159, n o 6,Junho de 1999, p. 1849–1861 ( ISSN 1073-449X e 1535-4970 , DOI 10.1164 / ajrccm.159.6.9808136 , ler online , acessado em 20 de janeiro de 2020 ).
- (in) Suelene Aires Franca Carlos Toufen André Luiz D. Hovnanian e André Luís P. Albuquerque , " A epidemiologia da insuficiência respiratória aguda em pacientes hospitalizados: Um estudo de coorte prospectivo brasileiro ' , Journal of Critical Care , vol. 26, n o 3,junho de 2011, p. 330.e1–330.e8 ( DOI 10.1016 / j.jcrc.2010.10.010 , ler online , acessado em 20 de janeiro de 2020 ).
- (em) Simon V. Baldwin , " O médico pulmonar em cuidados intensivos 3: Gerenciamento de cuidados intensivos da pneumonia adquirida da comunidade " , Thorax , vol. 57, n o 3,1 st março 2002, p. 267-271 ( PMID 11867834 , PMCID PMC1746268 , DOI 10.1136 / tórax.57.3.267 , ler online , acessado em 20 de janeiro de 2020 ).
- (en) Bruno L. Ferreyro e Laveena Munshi , “ Causes of Aguda Respiration Failure in the immunocompromised host: ” , Current Opinion in Critical Care , vol. 25, n o 1,fevereiro de 2019, p. 21-28 ( ISSN 1070-5295 , DOI 10.1097 / MCC.0000000000000569 , ler online , acessado em 14 de janeiro de 2020 ).
- (en) Jean-Louis Vincent , Yasser Sakr e Marco Ranieri , " Epidemiologia e resultado da insuficiência respiratória aguda em pacientes de unidade de terapia intensiva: " , Critical Care Medicine , Vol. 31, n o Suplemento,Abril de 2003, S296 - S299 ( ISSN 0090-3493 , DOI 10.1097 / 01.CCM.0000057906.89552.8F , ler online , acessado em 20 de janeiro de 2020 ).
- .
- (em) Jeevarathi Gnanaratnem e Neil N. Finer , " Neonatal Aguda Respiratória Insuficiência: " , Current Opinion in Pediatrics , vol. 12, n o 3,Junho de 2000, p. 227-232 ( ISSN 1040-8703 , DOI 10.1097 / 00008480-200006000-00009 , ler online , acessado em 4 de fevereiro de 2020 ).
- (em) Heber C. Nielsen , Sr. Howard Zinman e John S. Torday , " Dihydrotestosterone Inhibits Rabbit Fetal Pulmonary Surfactant Production " , Journal of Clinical Investigation , Vol. 69, n o 3,1 st março 1982, p. 611-616 ( ISSN 0021-9738 , PMID 6916770 , PMCID PMC371018 , DOI 10.1172 / JCI110488 , ler online , acessado em 14 de maio de 2020 )
- (en) Reese H. Clark , “ A Epidemiologia da Insuficiência Respiratória em Neonatos Nascidos em uma Idade Gestacional Estimada de 34 Semanas ou Mais ” , Journal of Perinatology , vol. 25, n o 4,Abril de 2005, p. 251–257 ( ISSN 1476-5543 , DOI 10.1038 / sj.jp.7211242 , ler online , acessado em 5 de fevereiro de 2020 ).
- (en) Peter G. Dahlem , Willem MC van Aalderen , Marije E. Hamaker , Marcel GW Dijkgraaf e Albert P. Bos , " Incidência e resultado a curto prazo de lesão pulmonar aguda em crianças ventiladas mecanicamente " , Europeu Respiratory Journal , vol. 22, n o 6,1 ° de dezembro de 2003, p. 980-985 ( ISSN 0903-1936 e 1399-3003 , DOI 10.1183 / 09031936.03.00003303 , ler online , acessado em 13 de janeiro de 2020 ).
- (en) JR Masclans , P. Pérez-Terán e O. Roca , “ O papel da oxigenoterapia de alto fluxo na insuficiência respiratória aguda ” , Medicina Intensiva (Edição em Inglês) , vol. 39, n o 8,novembro de 2015, p. 505-515 ( DOI 10.1016 / j.medine.2015.05.004 , ler online , acessado em 26 de dezembro de 2019 ).
- (en) Jeffrey J. Ward , “ -High Flow administração de oxigênio por cânula nasal para Adultos e perinatais pacientes ” , Respiratory Care , vol. 58, n o 1,1 ° de janeiro de 2013, p. 98-122 ( ISSN 0020-1324 e 1943-3654 , DOI 10.4187 / respcare.01941 , ler online , acessado em 26 de dezembro de 2019 ).
- (en) Dominic Wilkinson , Chad Andersen , Colm PF O'Donnell e Antonio G De Paoli , " Cânula nasal de alto fluxo para suporte respiratório em bebês prematuros " , Cochrane Database of Systematic Reviews ,22 de fevereiro de 2016( DOI 10.1002 / 14651858.CD006405.pub3 , ler online , acessado em 26 de dezembro de 2019 ).
- (in) Sr. Nishimura , " Terapia de oxigênio com cânula nasal de alto fluxo em adultos: benefícios fisiológicos, indicação, benefícios clínicos e efeitos adversos " , Respiratory Care , vol. 61, n o 4,1 ° de abril de 2016, p. 529-541 ( ISSN 0020-1324 e 1943-3654 , DOI 10.4187 / respcare.04577 , ler online , acessado em 26 de dezembro de 2019 ).
- (em) Amanda Corley , Claire M Rickard , Leanne M Aitken e Amy Johnston , " Cânulas nasais de alto fluxo para meios respiratórios em pacientes adultos de terapia intensiva " , Cochrane Database of Systematic Reviews ,30 de maio de 2017( PMID 28555461 , PMCID PMC6481761 , DOI 10.1002 / 14651858.CD010172.pub2 , ler online , acessado em 26 de dezembro de 2019 ).
- (en) Christian R Osadnik , Vanessa S Tee , Kristin V Carson-Chahhoud e Joanna Picot , “ Ventilação não invasiva para o manejo da insuficiência respiratória hipercápnica aguda devido à exacerbação da doença pulmonar obstrutiva crônica ” , Cochrane Banco de dados de revisões sistemáticas ,13 de julho de 2017( PMID 28702957 , PMCID PMC6483555 , DOI 10.1002 / 14651858.CD004104.pub4 , ler online , acessado em 26 de dezembro de 2019 ).
- (en) " Conferências de Consenso Internacionais em Medicina Intensiva: Ventilação de Pressão Positiva Não Invasiva na Insuficiência Respiratória Aguda: Organizada em Conjunto pela American Thoracic Society, a European Respiratory Society, a European Society of Intensive Care Medicine e a Société de Réanimation de Langue Française, e aprovado pelo Conselho de Administração da ATS, dezembro de 2000 ” , American Journal of Respiratory and Critical Care Medicine , vol. 163, n o 1,Janeiro de 2001, p. 283–291 ( ISSN 1073-449X e 1535-4970 , DOI 10.1164 / ajrccm.163.1.ats1000 , ler online , acessado em 27 de dezembro de 2019 ).
- Giuseppe Bello , Paolo De Santis e Massimo Antonelli , “ ventilação não invasiva em edema pulmonar cardiogénico ”, Annals of Translational Medicine , vol. 6, n o 18,setembro de 2018, p. 355-355 ( PMID 30370282 , PMCID PMC6186545 , DOI 10.21037 / atm.2018.04.39 , ler online , acessado em 26 de dezembro de 2019 ).
- (em) Dean R. Hess , " Noninvasive Ventilation for Acute Respiratory Failure " , Respiratory Care , vol. 58, n o 6,1 ° de junho de 2013, p. 950-972 ( ISSN 0020-1324 e 1943-3654 , DOI 10.4187 / respcare.02319 , ler online , acessado em 26 de dezembro de 2019 ).
- Barbas et al 2013 .
- (in) Aylin Ozsancak Ugurlu e Mehmet Ali Habesoglu , " Epidemiology of VIN for Acute Respiratory Failure in COPD Patients: Results from the International Surveys vs. the “Real World” ” , DPOC: Journal of Chronic Obstructive Pulmonary Disease , vol. 14, n o 4,4 de julho de 2017, p. 429-438 ( ISSN 1541-2555 e 1541-2563 , DOI 10.1080 / 15412555.2017.1336527 , ler online , acessado em 7 de janeiro de 2020 ).
- (en) Josep Masip e Arantxa Mas , " Ventilação não invasiva em insuficiência respiratória aguda " , International Journal of Chronic Obstructive Pulmonary Disease ,agosto de 2014, p. 837 ( ISSN 1178-2005 , PMID 25143721 , PMCID PMC4136955 , DOI 10.2147 / COPD.S42664 , ler online , acessado em 26 de dezembro de 2019 ).
- Davidson et al 2016 .
- Rochwerg et al 2017 .
- (in) Nicolas Berbenetz , Yongjun Wang , James Brown e Charlotte Godfrey , " ventilação com pressão positiva não invasiva (CPAP ou NPPV de dois níveis) para edema pulmonar cardiogênico " , Cochrane Database of Systematic Reviews ,5 de abril de 2019( PMID 30950507 , PMCID PMC6449889 , DOI 10.1002 / 14651858.CD005351.pub4 , ler online , acessado em 26 de dezembro de 2019 ).
- (in) Fang Luo , Djillali Annane David Orlikowski e Li He , " ventilação invasiva versus não invasiva para insuficiência respiratória aguda em doença neuromuscular e distúrbios da parede torácica " , Cochrane Database of Systematic Reviews ,4 de dezembro de 2017( PMID 29199768 , PMCID PMC6486162 , DOI 10.1002 / 14651858.CD008380.pub2 , ler online , acessado em 26 de dezembro de 2019 ).
- (in) Wei Jie Lim , Redhuan Mohammed Akram , Kristin V Carson e Satya Mysore , " Ventilação de pressão positiva não invasiva para o tratamento da insuficiência respiratória devido a exacerbações agudas graves de asma " , Cochrane Database of Systematic Reviews ,12 de dezembro de 2012( DOI 10.1002 / 14651858.CD004360.pub4 , ler online , acessado em 26 de dezembro de 2019 ).
- (em) Ganesh Raghu , Bram Rochwerg , Yuan Zhang e Carlos Cuello A. Garcia , " An Official ATS / ERS / JRS / ALT Practice Guideline: Treatment of Idiopathic Pulmonary Fibrosis. Uma atualização do Guia de Prática Clínica de 2011 ” , American Journal of Respiratory and Critical Care Medicine , vol. 192, n o 215 de julho de 2015, e3 - e19 ( ISSN 1073-449X e 1535-4970 , DOI 10.1164 / rccm.201506-1063ST , ler online , acessado em 16 de janeiro de 2020 ).
- (in) Debora AS Faria , Edina MK da Silva Álvaro N Atallah e Flávia MR Vital , " ventilação não invasiva de pressão positiva para insuficiência respiratória aguda após cirurgia abdominal superior " , Cochrane Database of Systematic Reviews ,5 de outubro de 2015( DOI 10.1002 / 14651858.CD009134.pub2 , ler online , acessado em 26 de dezembro de 2019 ).
- (in) Maria FS Torres , Gustavo JM Porfirio Alan PV Carvalho e Rachel Riera , " Ventilação não invasiva com pressão positiva para prevenção de complicações pós-ressecção pulmonar em pacientes com câncer de pulmão " , Cochrane Database of Systematic Reviews ,6 de março de 2019( PMID 30840317 , PMCID PMC6402531 , DOI 10.1002 / 14651858.CD010355.pub3 , ler online , acessado em 26 de dezembro de 2019 ).
- (in) Roberto Bellù , Koert A de Waal e Rinaldo Zanini , " Opióides para neonatos recebendo ventilação mecânica " , Cochrane Database of Systematic Reviews ,23 de janeiro de 2008( DOI 10.1002 / 14651858.CD004212.pub3 , ler online , acessado em 26 de dezembro de 2019 ).
- (em) Fahad M Al-hameed e Sat Sharma , " Resultado de Pacientes Admitidos em Unidade de Terapia Intensiva para Exacerbação Aguda de Fibrose Pulmonar Idiopática " , Canadian Respiratory Journal , vol. 11, n o 22004, p. 117-122 ( ISSN 1198-2241 , DOI 10.1155 / 2004/379723 , lido online , acessado em 16 de janeiro de 2020 ).
- (em) John P. Kress , Anne S. Pohlman , Michael F. O'Connor e Jesse B. Hall , " Daily Interruption of Sedative infusions in Critically Ill Patients Undergoing Mechanical Ventilation " , New England Journal of Medicine , vol. 342, n o 20,18 de maio de 2000, p. 1471-1477 ( ISSN 0028-4793 e 1533-4406 , DOI 10.1056 / NEJM200005183422002 , ler online , acessado em 16 de janeiro de 2020 ).
- Alhazzani, W. Møller, MH Arabi, M. Loeb et al. , Surviving sepsis campaign: guidelines on the management of Coronavirus Disease 2019 (COVID-19) - Prova não editada aceite , European Society of Intensive Care Medicine e the Society of Critical Care Medicine,2020( DOI 10.1007 / s00134-020-06022-5 , leia online )
- Thomas Godet, Audrey Johanny e Emmanuel Futier, “ Quando e como faço uma manobra de recrutamento alveolar na sala de cirurgia? » , MAPAR ,2016
- (em) Nora H. Cheung e Lena M. Napolitano , " Traqueostomia: Epidemiologia, Indicações, Tempo, Técnica e Resultados " , Respiratory Care , vol. 59, n o 6,1 ° de junho de 2014, p. 895–919 ( ISSN 0020-1324 e 1943-3654 , DOI 10.4187 / respcare.02971 , ler online , acessado em 27 de dezembro de 2019 ).
- JL Trouillet, " Pneumopatias adquiridas sob ventilação mecânica " , na Sociedade Francesa de Anestesia-Reanimação ,3 de março de 2009(acessado em 16 de janeiro de 2020 ) .
- P. Seguin e K. Hervé, " Prevenção da pneumonia adquirida sob ventilação mecânica " , em sofia.medicalistes.fr ,2012.
- .
- .
- (in) Viviane G. Nasr , Lakshmi Raman , Ryan P. Barbaro e Yigit Guner , " Destaques do Apoio Organização Registry vida extracorpórea: 2006-2017 " , ASAIO Journal , vol. 65, n o 6,agosto de 2019, p. 537-544 ( ISSN 1058-2916 , DOI 10.1097 / MAT.0000000000000863 , ler online , acessado em 14 de janeiro de 2020 ).
- Simon Erickson , “ extra-corpórea membrana de oxigenação no pediátrica aguda síndrome do desconforto respiratório: superestimada ou subutilizados? ”, Annals of Translational Medicine , vol. 7, N o 19,outubro de 2019, p. 512-512 ( PMID 31728365 , PMCID PMC6828785 , DOI 10.21037 / atm.2019.09.27 , ler online , acessado em 14 de janeiro de 2020 ).
- (em) Ryan P. Barbaro , Yuejia Xu , Santiago Borasino e Edward J. Truemper , " A Oxigenação da Membrana Extracorpórea Melhora a Sobrevivência na Insuficiência Respiratória Aguda Pediátrica? ” , American Journal of Respiratory and Critical Care Medicine , vol. 197, n o 9,Maio de 2018, p. 1177–1186 ( ISSN 1073-449X e 1535-4970 , PMID 29373797 , PMCID PMC6019927 , DOI 10.1164 / rccm.201709-1893OC , ler online , acessado em 14 de janeiro de 2020 ).
- (en) Soo Jin Na , Jae-Seung Jung , Sang-Bum Hong e Woo Hyun Cho , “ Resultados clínicos de pacientes recebendo oxigenação por membrana extracorpórea prolongada para suporte respiratório ” , Therapeutic Advances in Respiratory Disease , vol. 13,janeiro de 2019, p. 175346661984894 ( ISSN 1753-4666 e 1753-4666 , PMID 31090503 , PMCID PMC6535699 , DOI 10.1177 / 1753466619848941 , ler online , acessado em 14 de janeiro de 2020 ).
- (em) Matthew L. Paden , Steven A. Conrad , Peter T. Rycus e Ravi R. Thiagarajan , " Extracorporeal Life Support Organization Registry Report 2012: " , ASAIO Journal , vol. 59, n o 3,2013, p. 202-210 ( ISSN 1058-2916 , DOI 10.1097 / MAT.0b013e3182904a52 , ler online , acessado em 14 de janeiro de 2020 ).
- (em) Nikkole Sr. Haines , Peter T. Rycus , Joseph B. Zwischenberger e Robert H. Bartlett , " Extracorporeal Life Support Registry Report 2008: Neonatal and Pediatric Cardiac Cases: " , ASAIO Journal , vol. 55, n o 1,janeiro de 2009, p. 111–116 ( ISSN 1058-2916 , DOI 10.1097 / MAT.0b013e318190b6f7 , lido online , acessado em 14 de janeiro de 2020 ).
- (in) Roberto Lorusso Fabio Barili , Michele Di Mauro e Sandro Gelsomino , " Complicações Neurológicas In-Hospitalares em Pacientes Adultos Submetidos à Oxigenação de Membrana Extracorpórea Venoarterial: Resultados do Registro de Organização de Suporte de Vida Extracorpórea " , Critical Care Medicine , Vol. 44, n o 10,outubro 2016, e964 - e972 ( ISSN 0090-3493 , DOI 10.1097 / CCM.0000000000001865 , ler online , acessado em 14 de janeiro de 2020 ).
- (em) Yue-Nan Ni Jian Luo , He Yu e Dan Liu , "A cânula nasal de alto fluxo pode reduzir a taxa de reintubação em pacientes adultos após a extubação? Uma meta-análise ” , BMC Pulmonary Medicine , vol. 17, n o 1,dezembro de 2017, p. 142 ( ISSN 1471-2466 , PMID 29149868 , PMCID PMC5693546 , DOI 10.1186 / s12890-017-0491-6 , ler online , acessado em 26 de dezembro de 2019 ).
- (em) William D Schweickert , Mark C. Pohlman , Anne S Pohlman e Celerina Nigos , " Early física e terapia ocupacional em mecanicamente ventilados, pacientes criticamente enfermos: um ensaio clínico randomizado " , The Lancet , vol. 373, n o 9678,Maio de 2009, p. 1874–1882 ( DOI 10.1016 / S0140-6736 (09) 60658-9 , ler online , acessado em 13 de janeiro de 2020 ).
- (en) Gerald S. Zavorsky , Jiguo Cao , Nancy E. Mayo e Rina Gabbay , “ arterial contra gases sanguíneos capilares: Uma meta-análise ” , Respiratory Physiology & Neurobiology , vol. 155, n o 3,Março de 2007, p. 268-279 ( DOI 10.1016 / j.resp.2006.07.002 , lido online , acessado em 7 de janeiro de 2020 ).
- (en) Michael W. Quasney , Yolanda M. López-Fernández , Miriam Santschi e R. Scott Watson , “ The Outcomes of Children With Pediatric Acute Respiratory Distress Syndrome: Proceedings from the Pediatric Agute Lung Injury Consensus Conference ” , Pediatric Critical Care Medicine , vol. 16,junho de 2015, S118 - S131 ( ISSN 1529-7535 , DOI 10.1097 / PCC.0000000000000438 , ler online , acessado em 13 de janeiro de 2020 ).
- (em) Maki Kobayashi Yoko Shibata , Sumitomo Inoue e Akira Igarashi , " Preditores para mortalidade por insuficiência respiratória em uma população geral " , Scientific Reports , Vol. 6,16 de maio de 2016( ISSN 2045-2322 , PMID 27180927 , PMCID 4867438 , DOI 10.1038 / srep26053 , ler online , acessado em 21 de janeiro de 2020 ).
- (in) Whitney D. Gannon , David J. Lederer , Mauer Biscotti e Azka Javaid , " Modelo Resultados e predição de mortalidade de adultos críticos com insuficiência respiratória aguda e doença intersticial pulmonar " , Peito , Vol. 153, n o 6,junho de 2018, p. 1387–1395 ( PMID 29353024 , PMCID PMC6026289 , DOI 10.1016 / j.chest.2018.01.006 , ler online , acessado em 16 de janeiro de 2020 ).
- (em) Demosthenes Bouros , Andrew G. Nicholson , Vlasis Polychronopoulos e Roland M. du Bois , " Acute interstitial pneumonia " , European Respiratory Journal , vol. 15, n o 2Fevereiro de 2000, p. 412 ( DOI 10.1034 / j.1399-3003.2000.15b31.x , ler online , acessado em 16 de janeiro de 2020 ).
- (em) Jason Phua , Joan R. Badia , Neill KJ Adhikari e Jan O. Friedrich , " Has Mortality from Acute Respiratory Distress Syndrome Decreased over Time?: A Systematic Review " , American Journal of Respiratory and Critical Care Medicine , Vol. 179, n o 3,Fevereiro de 2009, p. 220-227 ( ISSN 1073-449X e 1535-4970 , DOI 10.1164 / rccm.200805-722OC , ler online , acessado em 13 de janeiro de 2020 ).
- (en) Margaret S. Herridge , Angela M. Cheung , Catherine M. Tansey e Andrea Matte-Martyn , " One-Year Outcomes in Survivors of the Acute Respiratory Distress Syndrome " , New England Journal of Medicine , voar. 348, n o 8,20 de fevereiro de 2003, p. 683-693 ( ISSN 0028-4793 e 1533-4406 , DOI 10.1056 / NEJMoa022450 , ler online , acessado em 13 de janeiro de 2020 ).
- .
- (in) Margaret S. Herridge , Catherine M. Tansey , Andrea Matté e George Tomlinson , " Functional Disability 5 anos após Síndrome de aflição respiratória aguda " , The New England Journal of Medicine , vol. 364, n o 14,7 de abril de 2011, p. 1293-1304 ( ISSN 0028-4793 e 1533-4406 , DOI 10.1056 / NEJMoa1011802 , ler online , acessado em 14 de janeiro de 2020 ).
Veja também
Bibliografia
Fisiopatologia- (pt) Charis Roussos e Antonia Koutsoukou , “ Respiratory failure ” , European Respiratory Journal , vol. 22, n o Suplemento 47,16 de novembro de 2003, p. 3s - 14s ( ISSN 0903-1936 e 1399-3003 , DOI 10.1183 / 09031936.03.00038503 , lido online , acessado em 26 de dezembro de 2019 ).
- (en) Nicolaos K. Markou , Pavlos M. Myrianthefs e George J. Baltopoulos , " Respiratory Failure: An Overview " , Critical Care Nursing Quarterly , vol. 27, n o 4,outubro de 2004, p. 353-379 ( ISSN 0887-9303 , DOI 10.1097 / 00002727-200410000-00006 , ler online , acessado em 16 de janeiro de 2020 ).
- (em) James Schneider e Todd Sweberg , " Acute Respiratory Failure " , Critical Care Clinics , Vol. 29, n o 2Abril de 2013, p. 167-183 ( DOI 10.1016 / j.ccc.2012.12.004 , lido online , acessado em 7 de janeiro de 2020 ).
- (em) Matthew L. Friedman e Mara E. Nitu , " Acute Respiratory Failure in Children " , Pediatric Annals , vol. 47, n o 7,1 ° de julho de 2018, e268 - e273 ( ISSN 1938-2359 , DOI 10.3928 / 19382359-20180625-01 , ler online , acessado em 26 de dezembro de 2019 ).
- (en) Carmen Sílvia Valente Barbas , Alexandre Marini Ísola , Augusto Manoel de Carvalho Farias e Alexandre Biasi Cavalcanti , “ recomendações brasileiras de ventilação mecânica 2013. Parte 2 ” , Revista Brasileira de Terapia Intensiva , vol. 26, n o 3,2014( ISSN 0103-507X , PMID 25295817 , PMCID PMC4188459 , DOI 10.5935 / 0103-507X.20140034 , ler online , acessado em 16 de janeiro de 2020 ).
- (pt) Bram Rochwerg , Laurent Brochard , Mark W. Elliott e Dean Hess , “ Diretrizes oficiais de prática clínica ERS / ATS: ventilação não invasiva para insuficiência respiratória aguda ” , European Respiratory Journal , vol. 50, n o 2agosto de 2017, p. 1602426 ( ISSN 0903-1936 e 1399-3003 , DOI 10.1183 / 13993003.02426-2016 , ler online , consultado em 4 de fevereiro de 2020 ).
- (pt) Para Craig Davidson , Stephen Banham , Mark Elliott e Daniel Kennedy , “ Diretriz BTS / ICS para o manejo ventilatório da insuficiência respiratória hipercápnica aguda em adultos ” , Thorax , vol. 71, n o Suppl 2,abril de 2016, ii1 - ii35 ( ISSN 0040-6376 e 1468-3296 , DOI 10.1136 / thoraxjnl-2015-208209 , lido online , acessado em 4 de fevereiro de 2020 ).
Artigos relacionados
Causas comuns de dificuldade respiratória- Pneumopatia
- Insuficiência cardíaca e edema agudo de pulmão
- Exacerbação da DPOC
- Síndrome da insuficiência respiratória aguda
- Oxigenoterapia nasal de alto fluxo
- Ventilação não invasiva
- Ventilação invasiva: intubação e traqueostomia
- Oxigenação por membrana extracorpórea
- Respirador artificial
links externos
- Desconforto respiratório: informações para os pacientes , Claudia Steurer-Stey, Revue Médicale Suisse (2015; volume 11, páginas 1965-1966).
- O que fazer com insuficiência respiratória aguda , faculdade nacional de professores de ressuscitação médica.
- Revisão geral da ventilação artificial , Bhakti K. Patel, Manuel Merck , abril de 2018.
- Ventilação insuficiente , Bhakti K. Patel, Manuel Merck , abril de 2018.