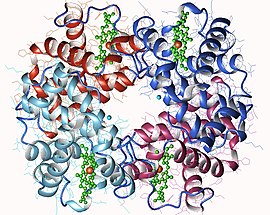
Hemoglobina
A hemoglobina , comumente simbolizado Hb , por vezes Hgb é um pigmento respiratório (família molecular de metaloproteínas , aqui contendo ferro ) presentes principalmente no sangue do vertebrado , nas suas células vermelhas do sangue e nos tecidos alguns dos invertebrados . Sua função é transportar oxigênio O 2do sistema respiratório ( pulmões , guelras ) para o resto do corpo . A quantidade de hemoglobina é um parâmetro medido durante um hemograma .
Função
A hemoglobina libera oxigênio nos tecidos para a respiração celular aeróbia , que, por meio do metabolismo , fornece energia para os processos biológicos essenciais à vida.
No ser humano , a hemoglobina é uma proteína hetero - tetramérica formado a partir de cadeias de péptidos são idênticas duas a duas. A hemoglobina A (HbA) representa aproximadamente 95% das moléculas de hemoglobina em adultos, consistindo em duas cadeias α e duas cadeias β; há também uma hemoglobina A 2 (HbA 2 ) de fórmula α 2 δ 2, e uma hemoglobina F (HbF, fetal) de fórmula α 2 γ 2. Cada um dos quatro canais está associado a um grupo protético denominado heme e consiste em um cátion de ferro complexado com uma porfirina . A hemoglobina é, portanto, uma hemoproteína .
Em mamíferos , a hemoglobina constitui quase 96% da massa de matéria seca dos glóbulos vermelhos e cerca de 35% de seu conteúdo total, incluindo água. Cada molécula de hemoglobina pode ligar até quatro moléculas de oxigênio O 2, e a hemoglobina no sangue pode transportar 1,34 mL de O 2por grama de proteína, o que permite transportar 70 vezes mais oxigênio do que a quantidade de O 2dissolvido em sangue. A hemoglobina também está envolvida no transporte de outros gases além do oxigênio. Em particular, garante o transporte de parte do dióxido de carbono CO 2produzido pela respiração celular, e também transporta óxido nítrico NO, que desempenha um papel significativo na sinalização celular de certos processos fisiológicos , e que é liberado junto com o oxigênio após ser transportado em um grupo tiol da apoproteína .
a maior parte da hemoglobina é encontrada nos glóbulos vermelhos, que são produzidos pela medula óssea. No entanto, nem toda a hemoglobina está concentrada nos glóbulos vermelhos. É assim encontrado, por exemplo, em neurônios dopaminérgicos do grupo A9 da substância negra , em macrófagos , em células alveolares e, nos rins , em células de mesângio . Nestes tecidos, a hemoglobina desempenha um papel antioxidante e regulador do metabolismo do ferro .
A hemoglobina e várias moléculas relacionadas também estão presentes em um grande número de invertebrados, fungos e plantas . Nestes organismos, a função da hemoglobina é transportar oxigênio O 2, mas também pode atuar como um transportador e regulador de outras espécies químicas , como o dióxido de carbono CO 2, monóxido de nitrogênio NO, sulfeto de hidrogênio HS e ânion sulfeto S 2– . Uma variante da hemoglobina, chamada leghemoglobina , remove o oxigênio dos sistemas anaeróbicos , por exemplo, nódulos de Rhizobium em fabaceae , antes de inativá -los.
Estrutura e operação
Subunidades
A hemoglobina tem uma estrutura quaternária característica de muitas proteínas com subunidades globulares . A maioria de seus resíduos de aminoácidos está envolvida em hélices α unidas por segmentos não helicoidais. As seções helicoidais são estabilizadas por ligações de hidrogênio que dão à proteína sua estrutura tridimensional característica, chamada de dobramento de globina , pois também é encontrada em outras globinas com um grupo heme protético , como a mioglobina . Este dobramento característico possui uma cavidade na qual está firmemente inserida uma molécula heme que constitui o grupo protético da proteína. A hemoglobina, portanto, contém uma molécula heme por subunidade.
-
Representação genérica de uma molécula de hemoglobina, mostrando as quatro subunidades, idênticas em pares, cada uma com uma molécula heme inserida em cavidades dentro das subunidades.
Na maioria dos vertebrados, a molécula de hemoglobina é um conjunto de quatro subunidades globulares em um arranjo quase tetraédrico . Essas subunidades são mantidas juntas por ligações de hidrogênio, por ligações iônicas e por efeito hidrofóbico . Em humanos adultos, o tipo mais comum de hemoglobina é a hemoglobina A, que consiste em duas subunidades α e duas subunidades β, cada uma composta por 141 e 146 resíduos de aminoácidos, respectivamente. Esta estrutura é simbolizada por α 2 β 2. Essas subunidades são estruturalmente muito semelhantes e têm aproximadamente o mesmo tamanho. Cada um tem um peso molecular de cerca de 16 kDa , ou 64 kDa ( 64 458 g · mol -1 ) para a proteína de comprimento total. Em crianças, a principal hemoglobina é chamada hemoglobina F (fetal), de fórmula α 2 γ 2, as cadeias γ sendo gradualmente substituídas por cadeias β durante o crescimento.
Heme
O heme é composto de um cátion de ferro ( II ) coordenado a quatro átomos de nitrogênio de uma porfirina , um tetrapirrol, a molécula é plana. Este cátion Fe 2+ também está covalentemente ligado ao resíduo de histidina F8 da globina na qual o heme está inserido; esse resíduo, denominado histidina proximal , está localizado abaixo do plano do heme. Fe 2+ também pode se ligar reversivelmente por meio de uma ligação covalente coordenada a uma molécula de oxigênio O 2acima do plano heme, oposto à histidina proximal, completando a geometria de coordenação octaédrica de seis ligantes do cátion ferro ( II ) na oxihemoglobina; na ausência de oxigênio, na desoxihemoglobina, esse sexto local é ocupado por uma molécula de água de ligação muito fraca.
O ferro ferroso da desoxihemoglobina encontra-se em estado de spin alto , ou seja, seus cinco orbitais d são ocupados, principalmente por elétrons individuais, daí um raio iônico da ordem de 92 pm , enquanto que, na oxiemoglobina, o ferro ferroso está estado de spin baixo , ou seja, seus orbitais d são ocupados por seis pares de elétrons que são limitados aos três orbitais de energia mais baixa, portanto, um raio iônico de apenas 75 pm . Por esta razão, o íon Fe 2+ é deslocado cerca de 40 µm do plano do heme na desoxihemoglobina, mas apenas 10 µm na oxiemoglobina. Essa variação está na base da alternância entre a forma tensa e a forma relaxada da hemoglobina.
- Estrutura do heme b , grupo protético da hemoglobina.
-
(pt) Diagrama esquemático da ligação de uma molécula de oxigênio O 2no heme , simbolizado aqui por uma linha grossa. Superóxido íon O 2• - resultante está ligado em um lado ao cátion de ferro ( III ) por uma ligação covalente coordenada e o outro lado à histidina distal. O cátion Fe ( II ) da desoxihemoglobina está no estado de spin alto e deslocado do plano heme em direção à histidina proximal, mas é trazido de volta a este plano passando para o estado de spin baixo pela ligação ao oxigênio 1., que muda a histidina proximal ao heme e promove a mudança do resto da proteína da forma tensionada (T) para a forma relaxada (R).
O cátion ferro pode estar no estado de oxidação +2 ou +3: neste último caso, estamos lidando com a metemoglobina , que se liga ao oxigênio de forma menos reversível do que a hemoglobina, e com menor afinidade. Na verdade, quando se liga ao heme ferroso, a molécula de oxigênio O 2tende a ser reduzido a íon superóxido O 2• - enquanto o cátion Fe 2+ tende a ser oxidado a Fe 3+ , um mecanismo que é revertido durante a liberação de oxigênio; em contraste, a ligação do oxigênio ao heme férrico é essencialmente irreversível e tende a bloquear a proteína forma R, que impede a liberação de oxigênio e inibe sua funcionalidade de transportador de oxigênio. O citocromo b 5 redutase , ou metemoglobina redutase, é a enzima que garante a redução da hemoglobina funcional da metemoglobina por redução do cátion Fe 3+ a Fe 2+ , tornando-se uma enzima essencial na manutenção das propriedades do sangue.
Forma tensa (T) e forma relaxada (R)
A hemoglobina desoxigenada (desoxiemoglobina) tem a chamada conformação T, ou tensa , enquanto a hemoglobina oxigenada (oxihemoglobina) tem a chamada R, ou conformação relaxada . A forma T tem baixa afinidade pelo oxigênio e, portanto, tende a liberá-lo, enquanto a forma R tem alta afinidade pelo oxigênio e tende a ligá-lo. Vários fatores favorecem uma ou outra dessas conformações. Assim, a forma T é favorecida por um baixo pH ( ácido ), uma alta concentração de CO 2e um alto nível de 2,3-bisfosfoglicerato (2,3-BPG), que promove a liberação de oxigênio conforme o sangue circula pelos tecidos , enquanto a forma R é favorecida por um pH alto, uma pressão parcial baixa de CO 2e baixo nível de 2,3-BPG, que promove a captação de oxigênio quando o sangue circula no nível dos alvéolos pulmonares .
-
Representação esquemática da troca da hemoglobina entre as formas T (desoxi) e R (oxi). Os movimentos do heme e da histidina proximal são claramente visíveis nas subunidades α 1 e β 2 .
-
Taxa de saturação de O 2hemoglobina em função da pressão parcial de O 2 ; às vezes chamada de curva de Barcroft , é sigmóide devido ao efeito cooperativo que acompanha a ligação do oxigênio à hemoglobina.
A troca entre a forma T e a forma R da hemoglobina é um mecanismo denominado mecanismo cooperativo , ou seja , alostérico , porque a ligação de uma molécula de oxigênio à forma T induz uma mudança conformacional que se propaga parcialmente para as subunidades adjacentes , cuja afinidade pelo oxigênio aumenta gradualmente à medida que outras moléculas de oxigênio se ligam à hemoglobina, até que toda a proteína assuma a conformação R; inversamente, a liberação de uma molécula de oxigênio da forma R induz uma mudança conformacional que se propaga parcialmente para as subunidades adjacentes, cuja afinidade pelo oxigênio diminui gradualmente à medida que a hemoglobina libera oxigênio, até que toda a proteína adote a conformação T. Esta é a razão pela qual o A curva de ligação do oxigênio à hemoglobina em função da pressão parcial de oxigênio tem a forma sigmóide , ao passo que seria hiperbólica na ausência de alosteria.
Curva de saturação de oxigênio da hemoglobina
É comum representar graficamente a taxa de saturação da hemoglobina no oxigênio O 2representado no eixo y em função da pressão parcial de oxigênio O 2, dado na abcissa . Nessa representação, a curva é sigmóide e tende a deslizar para a esquerda quando a afinidade da hemoglobina pelo oxigênio aumenta e para a direita quando ela diminui. A pressão parcial de oxigênio na qual a hemoglobina está 50% saturada com oxigênio é chamada de p 50 : quanto menor seu valor, maior a afinidade da hemoglobina pelo oxigênio. A título de orientação, o p50 da hemoglobina de um adulto saudável é tipicamente 3,5 kPa , frequentemente representado por 26,6 mmHg , enquanto o da mioglobina é tipicamente 130 Pa .
Vários fatores aumentam o p 50 e, portanto, deslizam esta curva para a direita:
- uma queda no pH , que se torna ácido : este é o efeito Bohr ;
- um aumento no nível de dióxido de carbono CO 2 : este é o efeito Haldane ;
- um aumento no nível de 2,3-bisfosfoglicerato (2,3-BPG);
- um aumento na temperatura, porém com um efeito relativamente pequeno.
Esses efeitos são reversíveis e a reversão da direção da variação desses fatores faz com que a curva deslize para a esquerda.
Outros ligantes transportados pela hemoglobina
Além de oxigênio O 2, que se liga à hemoglobina em um chamado mecanismo cooperativo , essa proteína também transporta outros ligantes , alguns dos quais são inibidores competitivos , como o monóxido de carbono CO, e outros são ligantes alostéricos , como o dióxido de carbono CO 2e monóxido de nitrogênio NO. CO 2se liga reversivelmente a grupos amina na apoproteína para formar carbaminohemoglobina , que se acredita fornecer cerca de 10% do transporte de CO 2em mamíferos , o resto sendo transportado principalmente na forma de íons de bicarbonato de HCO 3- . O óxido nítrico se liga reversivelmente aos grupos tiol da apoproteína para formar um S- nitrosotiol . O transporte de óxido nítrico pode mediar indiretamente o transporte de oxigênio pela hemoglobina, agindo como um vasodilatador em tecidos onde a pressão parcial de oxigênio é baixa.
Inibidores por competição com oxigênioA ligação do oxigênio à hemoglobina é efetivamente bloqueada pelo monóxido de carbono CO, por exemplo, da fumaça do cigarro , escapamentos ou combustão incompleta por uma caldeira . O monóxido de carbono compete com o oxigênio no local de ligação deste último no heme. A afinidade da hemoglobina pelo monóxido de carbono é cerca de 230 vezes a da hemoglobina pelo oxigênio, então pequenas quantidades de monóxido de carbono são suficientes para reduzir significativamente a oxigenação da hemoglobina durante a hematose e, portanto, a capacidade do sangue de oxigenar o corpo. A hipóxia que resulta da exposição contínua a 0,16% de CO no ar causa tontura , náusea , cefaléia e taquicardia em 20 minutos e leva à morte em duas horas; 1,28% de CO no ar causa inconsciência após apenas duas a três respirações e morte em menos de três minutos. Quando combinada com o monóxido de carbono, a hemoglobina é uma proteína chamada carboxihemoglobina cuja cor vermelha muito brilhante tende a colorir a pele de rosa de vítimas que morreram de envenenamento por monóxido de carbono , que de outra forma teriam a pele pálida ou azulada.
Da mesma forma, as exibições de hemoglobina, no seu local de ligação de oxigénio, um de afinidade competitivo para o cianeto de iões CN - , monóxido de enxofre SO, e sulfureto de iões S 2- , como com o sulfureto de hidrogénio H 2 S. Estes se ligam ao cátion de ferro do heme sem modificar seu estado de oxidação, mas, no entanto, inibem a ligação do oxigênio ao heme, daí sua alta toxicidade.
Ligantes de hemoglobina alostéricaO dióxido de carbono CO 2liga-se mais facilmente à desoxihemoglobina, o que facilita sua eliminação do corpo. Isso é chamado de efeito Haldane .
Além disso, CO 2dissolvido no sangue é convertido em ânion bicarbonato HCO 3- por anidrase carbônica , dependendo da reação:
CO 2+ H 2 S→ H 2 CO 3→ HCO 3- + H + .Conclui-se que o sangue rico em CO 2também é mais ácido , ou seja, seu pH é reduzido pelo efeito do ácido carbônico . A ligação de prótons H + e moléculas de CO 2a hemoglobina induz uma mudança conformacional que favorece a forma T e, portanto, a liberação de oxigênio. Os prótons se ligam a diferentes locais na hemoglobina, enquanto o dióxido de carbono se liga aos grupos α- amino para formar a carbaminohemoglobina . A diminuição da afinidade da hemoglobina pelo oxigênio na presença de CO 2e o pH ácido é chamado de efeito Bohr .
Pessoas aclimatadas a grandes altitudes têm um nível sanguíneo aumentado de 2,3-bisfosfoglicerato (2,3-BPG). Este último é um efetor heteroalostérico que tem o efeito de reduzir a afinidade da hemoglobina pelo oxigênio ao estabilizar a forma T: sob uma pressão parcial de oxigênio mais baixa do que no nível do mar, uma queda na afinidade da hemoglobina pelo oxigênio tem o efeito de aumentar o eficiência geral do transporte de oxigênio pela hemoglobina. Mais geralmente, um aumento no nível de 2,3-BPG é observado quando a pressão parcial de oxigênio diminui nos tecidos periféricos, por exemplo, no caso de hipoxemia , doença respiratória crônica, anemia ou mesmo insuficiência cardíaca . Por outro lado , o nível de 2,3-BPG diminui no caso de choque séptico e hipofosfatemia (in) .
Biossíntese e degradação
A biossíntese da hemoglobina envolve um conjunto complexo de etapas. O heme é proveniente de uma série de reações que se iniciam na mitocôndria e continuam no citosol dos eritrócitos imaturos, enquanto a apoproteína é produzida no citosol dos ribossomos . A produção de hemoglobina ocorre nos estágios iniciais da eritropoiese , desde o estágio de pró - eritroblasto até o estágio de reticulócitos na medula óssea . É aqui que os eritrócitos de mamíferos perdem seu núcleo , enquanto o núcleo permanece nos eritrócitos de pássaros e de muitas outras espécies . A biossíntese da apoproteína, entretanto, continua após a perda do núcleo, pois resta do RNA mensageiro na célula, que pode ser traduzido pelos ribossomos do citosol até a ativação do eritrócito no aparelho cardiovascular .
Em vertebrados , os eritrócitos que atingiram o fim de sua vida devido à senescência ou deterioração são removidos do sangue por fagocitose por macrófagos no baço e no fígado . No caso de hemólise na corrente sanguínea , a hemoglobina liga-se à haptoglobina , enquanto o heme livre é ligado à hemopexina , o que limita o efeito oxidativo. A hemoglobina não completamente degradada ou liberada em grandes quantidades pelos glóbulos vermelhos danificados pode obstruir os vasos sanguíneos , como os capilares dos rins , o que pode causar doença renal . A hemoglobina liberada é eliminada do sangue pela proteína CD163 , que é expressa exclusivamente em monócitos e macrófagos. A hemoglobina é quebrada nessas células e o ferro heme é reciclado, enquanto uma molécula de monóxido de carbono é liberada por molécula heme degradada: a quebra do heme é um dos poucos processos naturais. Produzindo monóxido de carbono no corpo humano e é responsável pela presença de CO no sangue de pessoas que respiram até o ar mais puro. Esse processo forma a biliverdina e depois a bilirrubina , que é de cor amarela. Insolúvel, é liberado pelos macrófagos no plasma sanguíneo , onde se liga à albumina sérica , que a transporta para os hepatócitos . Este último o solubiliza por conjugação com ácido glucurônico e o secretam nos intestinos com a bile . Os intestinos metabolizam a bilirrubina em urobilinogênio , que é excretado nas fezes como estercobilina e também na urina . Quando a bilirrubina não pode ser excretada, sua concentração no sangue aumenta e é eliminada principalmente pela urina, que escurece enquanto as fezes perdem a cor.
O ferro produzido pela degradação do heme é armazenado nas ferritinas dos tecidos e transportado no plasma sanguíneo por β-globulinas como as transferrinas .
Genético
As moléculas de hemoglobina consistem em subunidades do tipo globina, cuja sequência difere dependendo da espécie . Existem também variantes de hemoglobinas dentro da mesma espécie, embora uma dessas variantes seja geralmente predominante sobre as outras. Em humanos , a forma predominante de hemoglobina é chamada de hemoglobina A; é codificado pelos genes HBA1 , HBA2 e HBB localizados no cromossomo 16 para os dois primeiros e no cromossomo 11 para o último.
Evolução
É geralmente aceito que a diferença entre hemoglobina e mioglobina é subsequente à separação dos gnatostomos ( vertebrados até a mandíbula ) da lampreia . A mioglobina tem sido direcionada para o armazenamento de oxigênio, enquanto a hemoglobina é especializada no transporte de oxigênio. As subunidades da proteína são codificadas por genes do tipo α e β globina . Os predecessores desses genes surgiram durante uma duplicação ocorrida após o surgimento dos gnatóstomos, há cerca de 450 a 500 milhões de anos. O surgimento dos genes α e β abriu caminho para a polimerização dessas globinas e, portanto, para a formação de uma proteína maior composta por subunidades distintas. O fato de a hemoglobina ser uma proteína polimérica é a base do mecanismo alostérico que está, notadamente, na base da natureza cooperativa da ligação do oxigênio à hemoglobina. O gene α foi subsequentemente submetido a uma segunda duplicação que conduz à formação dos hba1 e HbA2 genes . Essas múltiplas duplicações e divergências criaram todo um conjunto de genes relacionados às globinas α e β, cuja regulação leva a que se expressem em diferentes estágios de desenvolvimento.
-
Alinhamento das sequências das cadeias α, β e δ da hemoglobina humana (fonte UniProt ).
Mutações
As mutações dos genes da hemoglobina podem levar a variantes da hemoglobina. A maioria dessas variantes é funcional e não tem efeito sobre a saúde. Algumas mutações na hemoglobina, por outro lado, podem causar doenças genéticas chamadas hemoglobinopatias . A mais conhecida dessas condições é a anemia falciforme , que foi a primeira doença humana cujo mecanismo foi elucidado em nível molecular. As talassemias são outro grupo de hemoglobinopatias envolvendo uma alteração da regulação gênica do componente globina da hemoglobina. Todas essas doenças resultam em anemia .
Alterar a sequência de aminoácidos da hemoglobina pode ser adaptativo. Foi assim possível mostrar que a hemoglobina se adapta à queda da pressão parcial de oxigênio observada em grandes altitudes. A hemoglobina deve então ser capaz de se ligar ao oxigênio a uma pressão mais baixa, o que pode ser manifestado por uma mudança na sequência no nível de aminoácidos envolvidos na afinidade da hemoglobina pelo oxigênio., Como foi observado, por exemplo, em beija-flores de Cordilheira dos Andes : assim, em espécies do gênero Oreotrochilus , no colibri Castelneau , no inca violifera ou mesmo no colibri gigante , essas mutações reduzem a afinidade da hemoglobina pelo ácido fítico , que nessas aves desempenha o mesmo papel que 2, 3-bisfospoglicerato em humanos; esta diminuição da afinidade tem o efeito de aumentar a eficiência do transporte de oxigênio quando a pressão parcial deste é reduzida.
A adaptação da hemoglobina a grandes altitudes também afeta os humanos. Assim, identificamos um grupo de mulheres tibetanas cujo genótipo codifica uma hemoglobina cuja afinidade pelo oxigênio aumenta com pressão parcial baixa. Isso tem o efeito de reduzir a mortalidade infantil sob essas condições extremas, o que oferece uma vantagem seletiva favorecendo os indivíduos portadores dessas mutações de hemoglobina.
Variantes humanas de hemoglobina
Em adultos, a principal variante da hemoglobina é a hemoglobina A , ou HbA , de fórmula α 2 β 2, que é responsável por mais de 97% da hemoglobina total de um adulto saudável. A outra variante da hemoglobina adulta é a hemoglobina A 2 , ou HbA 2 , com a fórmula α 2 δ 2, que representa entre 1,5% e 3,1% da hemoglobina total de um adulto saudável, mas cuja proporção aumenta em pacientes com anemia falciforme . Além dessas variantes adultas saudáveis, há uma dúzia de outras variantes da hemoglobina humana, que são encontradas em embriões , fetos ou pacientes com uma ou mais formas de hemoglobinopatia .
Hemoglobinas embrionárias
Quatro tipos de hemoglobina embrionária são conhecidos em humanos :
- Hb Gower-1 , de fórmula ζ 2 ε 2, é relativamente instável e se decompõe facilmente;
- Hb Gower-2 , de fórmula α 2 ε 2, mais estável do que a variante Gower-1, existe em pequenas quantidades durante a vida embrionária e fetal; foi proposto como um tratamento por reativação do gene em pacientes que sofrem de hemoglobinopatias , como β-talassemia, nos quais a reativação da hemoglobina F é contra-indicada por razões de toxicidade;
- Hb Portland-1 , de fórmula ζ 2 γ 2, está presente em pequenas quantidades durante a vida embrionária e fetal;
- Hb Portland-2 , de fórmula ζ 2 β 2, é ainda mais instável do que a variante de Gower-1, mas foi proposto como um tratamento por reativação do gene em pacientes com talassemia α .
A hemoglobina embrionária às vezes é simbolizada por Hbε, que não deve ser confundida com hemoglobina E, denotada por HbE, que é uma variante patológica de HbA apresentando uma mutação deletéria nas subunidades β, denotadas β E (o "E" neste caso se refere a o resíduo de glutamato modificado por mutação ).
Hemoglobina fetal
A hemoglobina fetal HbF de fórmula α 2 γ 2, substitui a hemoglobina embrionária após 10 a 12 semanas de desenvolvimento. Constitui até 95% do sangue do recém - nascido e é gradualmente substituído pela hemoglobina HbA adulta a partir do sexto mês após o nascimento; no entanto, permanece presente em vestígios em adultos, onde não excede 1% de todas as variantes de hemoglobina detectáveis. Ela permanece em crianças produzidas durante certa talassemia particular, às vezes até os cinco anos de idade, e uma condição rara chamada persistência hereditária do distúrbio da hemoglobina fetal (en) ( HPFH ) resulta na produção de HbF em vez de HbA além do período normal. Além disso, a produção de HbF pode ser reativada em adultos em um ambiente terapêutico para tratar a anemia falciforme .
A hemoglobina fetal é caracterizada por uma maior afinidade pelo oxigênio do que a hemoglobina adulta, o que permite ao feto se oxigenar do sangue da mãe: na verdade, o p 50 de HbF é de aproximadamente 19 mmHg ( 2,6 kPa ), em comparação com 26,8 mmHg ( 3,6 kPa ) para HbA. Essa diferença na afinidade pelo oxigênio resulta de uma diferença na afinidade por um dos efetores alostéricos da hemoglobina: 2,3-bisfosfoglicerato (2,3-BPG), cuja ligação com a hemoglobina tem o efeito de estabilizar a forma T desta proteína, que corresponde à desoxihemoglobina, que reduz a afinidade da hemoglobina pelo oxigênio. No caso da hemoglobina fetal, a subunidade γ tem um resíduo de serina na posição 143, onde uma subunidade β HbA tem um resíduo de histidina : esta posição está localizada no local de ligação 2,3-BPG, e a substituição de um A histidina, cuja cadeia lateral carrega uma carga elétrica positiva, por uma serina eletricamente neutra, enfraquece a interação do 2,3-BPG com a hemoglobina, porque o 2,3-BPG é uma pequena molécula que carrega cinco cargas elétricas negativas.
Hemoglobinopatias
As talassemias são caracterizadas pela produção insuficiente de um dos dois tipos de subunidades da hemoglobina adulta. Assim, é feita uma distinção entre a talassemia α , que é bastante rara, na qual as subunidades α são insuficientemente produzidas, e a talassemia β , a mais comum, na qual são as subunidades β que são insuficientemente produzidas. O primeiro leva à formação de tetrâmeros de β-globina chamados hemoglobina H , de fórmula β 4, que são bastante instáveis. Os homozigotos α 0 geralmente não sobrevivem por muito tempo após o nascimento devido a uma profunda alteração da hemoglobina fetal HbF, dando nessas condições hemoglobina de Barts , da fórmula γ 4.
As principais mutações na hemoglobina são:
- a hemoglobina C , de fórmula α 2 β C 2, que corresponde a uma substituição E6K, substituição do resíduo de glutamato na posição 6 por um resíduo de lisina . O primeiro tem uma cadeia lateral curta e carregada negativamente, enquanto o último tem uma cadeia lateral longa e carregada positivamente, que afeta a plasticidade geral dos eritrócitos . Os heterozigotos têm uma hemoglobina C de 28% a 44%, que permanece assintomática, enquanto os homozigotos têm 100% de hemoglobina C, o que causa uma anemia hemolítica leve . O gene da hemoglobina C está presente principalmente na África Ocidental , onde se pode ter uma vantagem preventiva contra a malária como outras hemoglobinopatias, bem como no sul da Europa , América Latina e as regiões. Caribbean ;
- a hemoglobina E ' da fórmula α 2 β E 2, que corresponde a uma substituição E26K, substituição do resíduo de glutamato na posição 26 por um resíduo de lisina. Essa mutação afeta cerca de 1 milhão de pessoas em todo o mundo, principalmente no sudeste da Ásia . Afeta a expressão de β-globina induzindo um splicing alternativo do RNA mensageiro nos códons 25-27, portanto, um déficit na produção de β-globina normal, o que leva à β-talassemia . Além disso, as subunidades β E interagem menos fortemente com as subunidades α, o que torna as moléculas de hemoglobina E menos estáveis na presença de oxidantes ;
- a hemoglobina S , de fórmula α 2 β S 2, que corresponde a uma substituição E6V, substituição do resíduo de glutamato na posição 6 por um resíduo de valina . Essa substituição, que coloca um resíduo de aminoácido hidrofóbico na superfície da proteína, cria uma zona de adesão que promove a precipitação da hemoglobina S em longos filamentos que estendem os eritrócitos dando-lhes uma foice ( foice em inglês, daí o "S" dessa variante), daí o nome de anemia falciforme também atribuída a essa doença, também chamada de anemia falciforme . O gene S está presente principalmente na África Subsaariana , Oriente Médio e Índia Central: em 2013, estimou-se que 3,2 milhões de homozigotos sofrem de doença falciforme e 43 milhões de heterozigotos têm traço falciforme. Sua anemia os protege da malária , daí uma vantagem seletiva que favorece a prevalência do gene da célula falciforme nas regiões maláricas.
Moléculas analógicas
Existe uma grande variedade de proteínas em plantas e animais que se ligam ao oxigênio para armazenamento ou transporte. As bactérias , os protozoários e os fungos também têm proteínas relacionadas com a hemoglobina que, por sua função conhecida ou prevista, se ligam a ligantes gasosos de forma reversível. Além do transporte e detecção de oxigênio, essas proteínas podem intervir para remover o oxigênio do meio que se acredita permanecer anaeróbico , como também é o caso da leghemoglobina .
Uma vez que muitas dessas proteínas são feitas de globinas e heme , elas são freqüentemente chamadas de "hemoglobina", embora sua estrutura geral seja muito diferente da hemoglobina de vertebrados . Em particular, a distinção entre mioglobina e hemoglobina é freqüentemente impossível nos animais mais simples na ausência de músculos nestes últimos, enquanto o sistema circulatório da maioria dos insetos não está envolvido na difusão de oxigênio através do corpo. Vários artrópodes ( aranhas , escorpiões , alguns crustáceos ) usam o buraco da fechadura , que é um heme livre contendo cobre, mas usando cátions de cobre diretamente coordenados com resíduos de histidina , mas esta proteína não é homóloga à hemoglobina.
A estrutura das hemoglobinas é muito variável dependendo da espécie considerada. Freqüentemente, é mono-globina em bactérias, protozoários, algas e plantas , enquanto muitos nematóides , moluscos e crustáceos têm proteínas muito grandes contendo um número muito maior de subunidades do que nos vertebrados. Os fungos e anelídeos, em particular, possuem hemoglobinas quiméricas contendo globinas e outros tipos de proteínas. Assim, o sem-fim tubo gigante das fontes hidrotermais contém uma variedade de hemoglobina compreendendo não menos do que 144 subunidades de globina, cada um associado com um grupo heme, cujo papel é o de captura de oxigénio ó 2e sulfeto de hidrogênio H 2 Snecessário para bactérias que vivem em simbiose com ele, bem como dióxido de carbono CO 2necessário para o anabolismo do verme. Essas estruturas são notáveis por poderem transportar oxigênio na presença de íons sulfeto e transportar esses íons sem serem envenenados por eles, como o são as hemoglobinas de outras espécies.
Entre as proteínas além da hemoglobina capazes de se ligar ao oxigênio, as seguintes moléculas podem ser retidas:
- Mioglobina - encontrada nos músculos da maioria dos vertebrados , incluindo humanos , dá a esses tecidos uma tonalidade vermelha ou cinza escuro. Sua estrutura é muito semelhante às subunidades da globina da hemoglobina, mas é monomérica e, portanto, não exibe um efeito cooperativo ao se ligar ao oxigênio. Está mais envolvido no armazenamento de oxigênio do que no seu transporte.
- Hemocianina - o segundo carreador de oxigênio mais comum na natureza, depois da hemoglobina, é encontrada em muitos artrópodes e moluscos . Ele usa um grupo protético que consiste em cobre, não ferro heme , e exibe uma cor azul quando oxigenado.
- Hemeritrina - alguns invertebrados marinhos e algumas espécies de anelídeos usam esta proteína de ferro não heme para transportar oxigênio. Apresenta coloração rosa ou roxa quando oxigenado e é límpido quando não oxigenado.
- Clorocruorina - encontrada em muitos anelídeos, é muito semelhante à eritrocruorina, mas seu grupo heme tem uma estrutura marcadamente diferente. É vermelho quando oxigenado e verde quando é desoxigenado (daí o seu nome).
- Eritrocruorina - encontrada em muitos anelídeos, incluindo minhocas , é uma proteína muito grande que pode conter mais de cem subunidades de proteínas e unidades heme, todas com massa molecular de até 3.600 kDa .
- Leghemoglobina - presente nas vagens , como alfafa e soja , que tem a função de proteger as bactérias fixadoras de azoto oxigénio para permitir que o nitrogenase para reduzir o azoto , o qual pode fazer na presença de oxigénio.
Uso clínico
Na medicina, vários termos se referem à hemoglobina:
- O nível de hemoglobina é expresso em g / 100 mL . Os valores normais de hemoglobina dependem do sexo e da idade do sujeito. Um nível de hemoglobina abaixo do normal define anemia . Os valores de referência são maiores para homens do que para mulheres. Um estudo questiona benchmarks de hemoglobina, argumentando que não se justifica ter diferentes benchmarks de hemoglobina para homens e mulheres.
- A saturação SaO 2definido como% é calculado pela quantidade de oxihemoglobina dividida pela quantidade total de hemoglobina no sangue. A saturação SaO 2pode ser medido no sangue venoso ou arterial. Um dos parâmetros de um teste chamado gasometria é a saturação de oxigênio do sangue . O valor de saturação é considerado perigoso se for inferior a 90% para o sangue arterial. O valor normal é cerca de 96-100% para condições atmosféricas normais. Nesse valor, falamos de capacidade de O 2sangue .
- A cianose é um sinal clínico. Esta é a coloração azulada dos tegumentos. Aparece quando a concentração de hemoglobina reduzida excede 5 g / 100 ml de sangue capilar. Pode ser mascarado pela anemia.
Doenças genéticas da hemoglobina
Como muitas proteínas, as cadeias de hemoglobina apresentam várias mutações que na maioria das vezes não têm impacto clínico. Mais de 500 hemoglobinas anormais foram identificadas. Certas mutações (Hb Köln, Indianapolis, etc.) causam instabilidade do tetrâmero precipitante no corpo de Heinz , ou metemoglobinemia (hemoglobina M).
Às vezes, essa mutação causa uma afinidade anormal por oxigênio, ou seja, como Hb Hope, uma diminuição na afinidade com um P50 alto dando uma anemia bem tolerada e cianose em repouso, o esforço e a altitude sendo mal suportados., Ou, como Hb Chesapeake, Malmö ou Olympia, um aumento da afinidade com um P50 reduzido e uma policitemia compensatória levando a manifestações clínicas a partir de uma certa idade.
Outros podem ser responsáveis pela hemólise crônica, HbS (por mutação da glutamina em valina que causará a polimerização da Hb), HbC ou piorar no estado heterozigoto outra hemoglobinopatia, HbO Arab, HbD Punjab ou Hb Lepore, ou β-talassemia, HbE.
Finalmente, o dano genético pode estar relacionado não à estrutura primária da proteína, mas a um defeito quantitativo em sua síntese ou a uma persistência anormalmente alta de hemoglobina HbF fetal.
Defeitos de síntese ou anomalia molecular são descritos sob os nomes de:
Histórico
Os primeiros estudos de hemoglobina foram levados para o XIX th século na Alemanha . Descoberta em 1840 por Hünefeld, a hemoglobina foi cristalizada em 1851 por Otto Funke (en) , e foi Felix Hoppe-Seyler quem demonstrou a fixação reversível de oxigênio nesta proteína em 1866. A natureza tetramérica e o peso molecular da hemoglobina foram estabelecidos por Gilbert Smithson Adair (en) em 1925 medindo a pressão osmótica das soluções de hemoglobina, que também identificou as bases do efeito cooperativo da ligação do oxigênio a essa proteína pela alosteria .
A estrutura tridimensional da hemoglobina foi estabelecida por Max Perutz em 1959 por cristalografia de raios X , o que o levou a compartilhar o Prêmio Nobel de Química de 1962 com John Kendrew , que realizou um trabalho semelhante sobre a mioglobina .
Hemoglobina nas artes
Em 2005, o artista Julian Voss-Andreae criou a escultura Coração de Aço (Hemoglobina) , modelada na espinha dorsal da proteína. A escultura é feita de vidro e aço Corten . A aparência enferrujada da obra é intencional e evoca a reação química fundamental da ligação do oxigênio ao ferro contido na hemoglobina.
O artista de Montreal Nicolas Baier criou a escultura Luster (hemoglobina) , uma escultura de aço inoxidável polido que mostra a estrutura da molécula de hemoglobina. A escultura está localizada no átrio do centro de pesquisa do Centro de Saúde da Universidade McGill em Montreal. O tamanho da escultura é de aproximadamente 10 metros por 10 metros por 10 metros.
Notas e referências
- (em) G. Fermi, MF Perutz e B. Shaanan , " The crystal structure of human desoxyhaemoglobin at 1.74 A resolution " , Journal of Molecular Biology , vol. 175, n o 2 15 de maio de 1984, p. 159-174 ( PMID 6726807 , DOI 10.1016 / 0022-2836 (84) 90472-8 , leia online )
- Os valores da massa e do número de resíduos indicados aqui são aqueles do precursor da proteína resultante da tradução do gene , antes das modificações pós-tradução , e podem diferem significativamente dos valores correspondentes aos valores da proteína funcional.
- (em) Robert I. Weed, Claude F. Reed e George Berg , " Is Hemoglobin Structural year Essential Component of Human Erythrocyte Membranes? ” , Journal of Clinical Investigation , vol. 42,Abril de 1963, p. 581-588 ( PMID 13999462 , PMCID 289.318 , DOI 10,1172 / JCI104747 , lido online )
- (in) E. Domínguez de Villota, MT García Carmona, JJ Rubio e S. Andrés Ruiz , " Igualdade da capacidade de ligação ao oxigênio in vivo e in vitro da hemoglobina em pacientes com doença respiratória grave " , British Journal of Anesthesia , vol. 53, n o 12,Dezembro de 1981, p. 1325-1328 ( PMID 7317251 , PMCID 289.318 , DOI 10.1093 / BJA / 53.12.1325 , lido online )
- (em) Connie CW Hsia , " Respiratory Function of Hemoglobin " , The New England Journal of Medicine , vol. 338, n o 4, 22 de janeiro de 1998, p. 239-247 ( PMID 9435331 , DOI 10.1056 / NEJM199801223380407 , leia online )
- (em) Sr. Biagioli, Sr. Pinto, D. et al Cesselli. , “ Expressão inesperada de α- e β-globina em neurônios dopaminérgicos mesencefálicos e células gliais ” , Proceedings of the National Academy of Sciences dos Estados Unidos da América , vol. 106, n o 36, 8 de setembro de 2009, p. 15454-15459 ( PMID 19717439 , PMCID 2732704 , DOI 10.1073 / pnas.0813216106 , ler online [PDF] )
- (en) Roy E. Weber e Serge N. Winogradow, “ hemoglobinas não Vertebrados: funções e adaptações moleculares ” , Physiological avaliação , vol. 81 n o 2, Abril de 2001, p. 569-628 ( PMID 11274340 , leia online )
- (em) Ross C. Hardison , " Uma breve história das hemoglobinas: planta, animal, protista e bactérias " , Proceedings of the National Academy of Sciences dos Estados Unidos da América , vol. 93, n o 12, 11 de junho de 1996, p. 5675-5679 ( PMID 8650150 , PMCID 39118 , DOI 10.1073 / pnas.93.12.5675 , JSTOR 39604 , Bibcode 1996PNAS ... 93.5675H , leia online )
- (em) Mireille Van CP Beekvelt Willy NJM Colier, Ron A. Wevers e Van Engelen Baziel GM , " Desempenho da espectroscopia infravermelha próxima no consumo local de O2 e medição do fluxo sanguíneo no músculo esquelético " , Journal of Applied Physiology , vol. 90, n o 2 Fevereiro de 2001, p. 511-519 ( PMID 11160049 )
- (en) RD Shannon , " Efetivos iônicos radii Revised and sistemic studies of interatomic distance in halogenides and Chalcogenides " , Acta Crystallographica Seção A: Crystal Physics, Diffraction, Theoretical and General Crystallography , Vol. 32, n o 5 de setembro, p. 1976 ( DOI 10.1107 / S0567739476001551 , Bibcode 1976AcCrA..32..751S , leia online )
- (em) Wray H. Huestis e Michael A. Raftery , " Conformation and cooperativity in hemoglobin " , Biochemistry , vol. 14, n o 9,6 de maio de 1975, p. 1886-1892 ( PMID 235969 , DOI 10.1021 / bi00680a013 , leia online )
- (em) Frank B. Jensen , " Os papéis duplos dos glóbulos vermelhos no fornecimento de oxigênio aos tecidos: transportadores de oxigênio e reguladores do fluxo sanguíneo local " , Journal of Experimental Biology , vol. 212, n o Pt 21,novembro de 2009, p. 3387-3393 ( PMID 19837879 , DOI 10.1242 / jeb.023697 , ler online )
- (em) D. Nicholas Bateman , " Carbon Monoxide " , Medicine , vol. 31, n o 10, Outubro de 2003, p. 41-42 ( DOI 10.1383 / medc.31.10.41.27810 , ler online )
- (em) CL e RL Townsend Maynard , " Effects on health of prolonged exposição to low carbon monoxide " , Occupational & Environmental Medicine , Vol. 59, n o 10, Outubro de 2002, p. 708-711 ( PMID 12356933 , PMCID 1740215 , DOI 10.1136 / oem.59.10.708 , JSTOR 27731796 , ler online )
- (em) John Haldane , " The Action of Carbonic Oxide on Man " , The Journal of Physiology , Vol. 18, n osso 5-6, 16 de novembro de 1895, p. 430-462 ( PMID 16992272 , PMCID 1514663 , DOI 10.1113 / jphysiol.1895.sp000578 , leia online )
- (em) Mark Goldstein , " Carbon Monoxide Poisoning " , Journal of Emergency Nursing , Vol. 34, n o 6, dezembro de 2006, p. 538-542 ( PMID 19022078 , DOI 10.1016 / j.jen.2007.11.014 , leia online )
- (em) Tim Struttmann Amy Scheerer, T. Scott Prince e Linda A. Goldstein , " Intoxicação por monóxido de carbono não intencional de uma fonte improvável " , Journal of the American Board of Family Medicine , vol. 11, n o 6, Novembro a dezembro de 1998, p. 481-484 ( PMID 9876005 , DOI 10.3122 / jabfm.11.6.481 , leia online )
- (em) Edward R. Burka , " Characteristics of RNA degradation in the erythroid cell " , Journal of Clinical Investigation , Vol. 48, n o 7, Julho de 1969, p. 1266-1272 ( PMID 5794250 , PMCID 322349 , DOI 10.1172 / JCI106092 , ler online )
- (em) Goro Kikuchi, Tadashi Yoshida Masato Noguchi , " Heme oxygenase and heme degradation " , Biochemical and Biophysical Research Communications , Vol. 338, n o 1, 9 de dezembro de 2005, p. 558-567 ( PMID 16115609 , DOI 10.1016 / j.bbrc.2005.08.020 , ler online )
- (em) Ross C. Hardison , " Evolução de hemoglobina e seus genes " , Cold Spring Harbor Perspectives in Medicine , vol. 2, n o 12, dezembro 2012, a011627 ( PMID 23209182 , PMCID 3543078 , DOI 10.1101 / cshperspect.a011627 , ler online )
- (in) Morris Goodman, William G. Moore e Genji Matsuda , " Evolução Darwiniana na genealogia da hemoglobina " , Nature , vol. 253, n o 5493, 20 de fevereiro de 1975, p. 603-608 ( PMID 1089897 , DOI 10.1038 / 253603a0 , Bibcode 1975Natur.253..603G , ler online )
- (en) Jay F. Storz, Juan C. Opazo e Federico G. Hoffmann , “ duplicação de genes, a duplicação do genoma, e a diversificação funcional de vertebrados globinas ” , Molecular Phylogenetics and Evolution , vol. 66, n o 2 Fevereiro de 2013, p. 469-478 ( PMID 22846683 , PMCID 4306229 , DOI 10.1016 / j.ympev.2012.07.013 , leia online )
- (em) EA Zimmer, SL Martin, Beverley SM, YW Kan e AC Wilson , " Rapid duplicação e perda de codificação de genes para as cadeias alfa da hemoglobina " , Proceedings of the National Academy of Sciences dos Estados Unidos , vol. 77, n o 4, Abril de 1980, p. 2158-2162 ( PMID 6929543 , PMCID 348671 , DOI 10.1073 / pnas.77.4.2158 , ler online )
- (em) Cynthia M. Beall, Kijoung Song, Robert C. Elston e Melvyn C. Goldstein , " Higher Tibetan offpring survival Entre mulheres com genótipos de alta saturação de oxigênio Residing at 4.000 m " , Proceedings of the National Academy of Sciences of the United Estados da América , vol. 101, n o 39, 28 de setembro de 2004, p. 14300–14304 ( PMID 15353580 , PMCID 521103 , DOI 10.1073 / pnas.0405949101 , leia online )
- (en) Zhenning He e J. Eric Russell , " Expressão, purificação e caracterização de hemoglobinas humanas Gower-1 (ζ 2 ε 2 ), Gower-2 (α 2 ε 2), e Portland-2 (ζ 2 β 2) montados em camundongos transgênicos complexos ” , Blood , vol. 97, n o 4,15 de fevereiro de 2001, p. 1099-1105 ( PMID 11159543 , leia online )
- (em) J. Eric Russell e Stephen A. Liebhaber , " Reversal of Lethal α- and β-thalassemias in Mice by Expression of Human Embryonic globins " , Blood , Vol. 92, n o 9, Novembro de 1998, p. 3057-3063 ( PMID 9787139 , ler online )
- (in) Sophie Lanzkron John J. Strouse, Renee Wilson, Mary Catherine Beach, Carlton Haywood Park Haesong Catherine Witkop, Eric B. Bass e Jodi B. Segal , " Systematic Review: Hydroxyurea for the Treatment of Adults with Sickle Cell Disease " , Annals of Internal Medicine , vol. 148, n o 12, 17 de junho de 2008, p. 939-955 ( PMID 18458272 , PMCID 3256736 , DOI 10.7326 / 0003-4819-148-12-200806170-00221 , ler online )
- (em) Amoz I. Chernoff Virginia Minnich, Supa Na Nakorn, Soodsarkorn Tuchinda, Channivat Kashemsant e Renate R. Chernoff , " Studies on hemoglobin S - I. As características clínicas, hematológicas e genéticas das síndromes da hemoglobina E " , Jornal of Laboratory and Clinical Medicine , vol. 47, n o 3, Março de 1956, p. 455-489 ( PMID 13353880 , leia online )
- (em) " Incidência global, regional e nacional, prevalência e anos de vida com deficiência para 301 doenças agudas e crônicas e lesões em 188 países, 1990-2013: uma análise sistemática para o Global Burden of Disease Study 2013 " , Lancet , vol. 386, n o 9995, 22 de agosto de 2015, p. 743-800 ( PMID 26063472 , DOI 10.1016 / S0140-6736 (15) 60692-4 , leia online )
- (em) William E. Royer Jr., Hitesh Sharma, Kristen Strand, James E. Knapp e Balaji Bhyravbhatla , " Lumbricus Erythrocruorin at 3.5 Å Resolução: Architecture of a megadalton Respiratory Complex " , Structure , vol. 14, n o 7, julho de 2006, p. 1167-1177 ( PMID 16843898 , DOI 10.1016 / j.str.2006.05.011 , leia online )
- (em) Luc Int Panis, Boudewijn Goddeeris e Rudolf Verheyen , " The hemoglobin concentração de Chironomus cf. Plumosus l. (Diptera: Chironomidae) larvas de dois habitats lênticos ” , Netherland Journal of Aquatic Ecology , vol. 29, n o 1, Abril de 1995, p. 1-4 ( DOI 10.1007 / BF02061785 , leia online )
- (em) Franck Zal, Francis H. Lallier, Brian N. Green, Serge N. Vinogradov e Andre Toulmond , " The multi-hemoglobin system of the hydrothermal vent tube worm gigantesco tubo worm. II. Composição da cadeia polipeptídica completa investigada por análise de entropia máxima de espectros de massa ” , Journal of Biological Chemistry , vol. 271, n o 15, 12 de abril de 1996, p. 8875-8881 ( PMID 8621529 , DOI 10.1074 / jbc.271.15.8875 , ler online )
- (em) Zoran Minic e Guy Hervé , " aspectos químicos e enzimológicos da simbiose entre les deep-sea tubeworm gigante tubeworm and Its bacterial endosymbiont " , The FEBS Journal , vol. 271, n o 15, Agosto de 2004, p. 3093-3102 ( PMID 15265029 , DOI 10.1111 / j.1432-1033.2004.04248.x , leia online )
- “ Quais são as evidências das diferenças de gênero na ferritina e na hemoglobina? » (Acessado em 2 de novembro de 2019 )
- Bernard Dreyfus 'Hematology, Médecine-Sciences- Flammarion 1992
- (de) Felix Hoppe-Seyler , " Über die oxidation in lebendem blute " , Med-chem Untersuch Lab , 1866, p. 133-140
- (em) Gilbert S. Adair , " The Osmotic Pressure of Hemoglobin in the Absence of Salts " , Proceedings of the Royal Society of London. Série B, Containing Papers of a Biological Character , vol. 98, n o 692, Outubro de 1925, p. 524 ( DOI 10.1098 / rspa.1925.0126 , JSTOR 94515 , Bibcode 1925RSPSB..98..524A , ler online )
- (en) MF Perutz, Rossmann MG, Ann F. Cullis, Hilary MUIRHEAD, GEORG WILL & ACT NORTH , " Structure of Hemoglobin: A Three-Dimensional Fourier Synthesis at 5.5-Å. Resolução, obtida por X-Ray Analysis ” , Nature , vol. 185, n o 4711 13 de fevereiro de 1960, p. 416-422 ( PMID 18990801 , DOI 10.1038 / 185416a0 , ler online )
- (en) Max Perutz F. , " Structure of hemoglobin " , Brookhaven Symposia in Biology , vol. 13, 1960, p. 165-183 ( PMID 13734651 )
-
(em) " O Prêmio Nobel de Química em 1962 " (acessado em 6 de novembro de 2016 ) :
" O Prêmio Nobel de Química de 1962 foi concedido em conjunto a Max Ferdinand Perutz e John Cowdery Kendrew" por seus estudos das estruturas das proteínas globulares " . "
- (em) Constance Holden , " Blood and Steel " , Science , vol. 309, n o 5744,30 de setembro de 2005, p. 2160 ( DOI 10.1126 / science.309.5744.2160d , ler online [PDF] )
- (em) Moran L Horton RA Scrimgeour G, Perry M, Principles of Biochemistry , Boston, MA, Pearson ,2011, 786 p. ( ISBN 978-0-321-70733-8 e 0-321-70733-8 ) , p. 127
- (em) Sean Henry, " Dê uma espiada na coleção de arte do MUHC " no CBC News ,7 de agosto de 2014(acedida em 1 r fev 2016 )
- " Luster (hemoglobina) 2014 " na Arte Pública Montreal (acessado em 1 st fevereiro 2016 )
- " Nicolas Baier " na McGill University Health Centre (acessado em 1 st fevereiro 2016 )
Veja também
Bibliografia
- Banerjee, R. & Sagaert, L. (1967). Dissociação da hemoglobina humana em meio ácido . Biochimica and Biophysica Acta (BBA) -Protein Structure, 140 (2), 266-273 ( resumo ).
- Blum, N., Maleknia, M., & Schapira, G. (1970). Α- e β-globinas livres e biossíntese de hemoglobina. Biochimica et Biophysica Acta (BBA) -Nucleic Acids and Protein Synthesis, 199 (1), 236-247.
- Breton-Gorius, J. (1970). Uso de diaminobenzidina para demonstração ao microscópio eletrônico da hemoglobina intracelular . Novo Rev. Fr. Hematology, 10, 243-256.
- Caffin, JP, Chauvet, JP, & Acher, R. (1969). Hemoglobinas anfíbias: Separação e caracterização preliminar das cadeias de hemoglobina do sapo Bufo bufo . FEBS letters, 5 (3), 196-198 ( abstract ).
- Bardakdjian-Michau, J., Dhondt, JL, Ducrocq, R., Galactéros, F., Guyard, A., Huchet, FX, ... & Wajcman, H. (julho de 2003). Boas práticas no estudo da hemoglobina . Em Annals of Clinical Biology (Vol. 61, No. 4, pp. 401-409).
- Bernard, M., Bordas-Fonfrède, M., Grimaldi, A., Guillemin, C., Stahl, A., Leutenegger, M., & Gillery, P. (1995). Interesses respectivos de ensaios de hemoglobina glicada e frutosamina no monitoramento de diabetes mellitus . Em Annals of Clinical Biology (Vol. 53, No. 6, pp. 321-327). John Libbey Eurotext.
- Bert, P. (1882). Sobre a riqueza de hemoglobina do sangue de animais que vivem em lugares altos. CR Acad Sei Paris, 94, 805-807.
- Bloch-Raphaël, C. (1939). Localização, formação e destruição da hemoglobina em anelídeos poliquetas (dissertação de doutorado).
- Eaton, WA e Hofrichter, J. (1990). Polimerização da hemoglobina falciforme . Avanços na química de proteínas, 40, 263-279.
- Foettinger, A. (1880). Sobre a existência de hemoglobina em equinodermos . Arco. Biol. Paris, 1, 405-415.
- Kruh, J., Dreyfus, JC, & Schapira, G. (1964). Ativação da síntese livre de células de hemoglobina pelo ácido ribonucléico: III. Ação do ácido ribonucléico total do fígado . Biochimica et Biophysica Acta (BBA) - Seção Especializada em Ácidos Nucleicos e Assuntos Relacionados, 91 (3), 494-505 ( resumo ).
- Kruh, J., Dreyfus, JC, Rosa, J., & Schapira, G. (1962). Síntese de hemoglobina por sistemas reticulócitos livres de células . Biochimica et Biophysica Acta (BBA) - Seção Especializada em Ácidos Nucleicos e Assuntos Relacionados, 55 (5), 690-703.
- Lambert, PP, Grégoire, F., & Royers, E. (1955). Hemodinâmica glomerular e excreção de hemoglobina . Archives Of Physiology And Biochemistry, 63 (1), 7-34 ( resumo ).
- Lena-Russo, D., North, ML, & Girot, R. (1992). Epidemiologia das doenças genéticas da hemoglobina na França metropolitana . The Practitioner Review, 42 (15), 1867-1872.
- Robert, M. (1975). Afinidade da hemoglobina pelo oxigênio . Hospital cantonal, departamento médico, clínica médica terapêutica.
- Uriel, J. (1958). Detecção das atividades da catalase e peroxidase da hemoglobina após eletroforese em ágar . Bulletin of the Society of Biological Chemistry, 40, 277-280.
- White, CT, Murray, AJ, Smith, DJ, Greene, JR e Bolin, RB (1986). Toxicidade sinérgica de endotoxina e hemoglobina. J Lab Clin Med, 108 (2), 132-137.