Alcalóide
Os alcalóides são moléculas com bases nitrogenadas, geralmente heterocíclicas , sendo a grande maioria de origem vegetal . Eles podem estar na forma de moléculas orgânicas heterocíclicas de nitrogênio básicas . Associado com o desenvolvimento da indústria farmacêutica, eles abriram o campo de "drogas químicas" a partir do final do XIX ° século .
Como muitos produtos naturais, quase todos os nomes de alcalóides comuns têm uma terminação "-ina", como nicotina , cafeína , atropina , ibogaína , emetina , ergina ou morfina . Normalmente, na química biológica, os alcalóides são derivados dos aminoácidos . Eles são encontrados na forma de misturas complexas, muitas vezes baseadas em várias ou mesmo dezenas de diferentes moléculas de alcalóides, com seus precursores, como metabólitos secundários , principalmente em plantas , fungos e alguns pequenos grupos de animais. Existe um tipo de alcalóide que contém dois átomos de nitrogênio no anel aromático e que não é de origem natural, é o grupo dos pirazóis .
Na forma purificada, essas moléculas muitas vezes revelam toxicidade aguda , bem como, em doses menores, uma atividade farmacológica calmante, não sem efeitos aditivos ou toxicidade crônica de longo prazo. Mas as proporções diminutas de cafeína no café , cocaína na folha seca de coca , nicotina no tabaco mascado ou mascado foram aceitas em várias culturas humanas, muitas vezes muito antigas: às vezes é difícil dizer se é apesar ou devido a seus vários psicotrópicos , ações psicoativas , estimulantes , dopantes , tônicas , eméticas , calmantes , latentes e analgésicas .
Na verdade, as moléculas de alcalóides no estado puro, as mais conhecidas, são frequentemente altamente tóxicas como estricnina , aconitina , atropina , cocaína ... mas algumas, por causa de sua poderosa ação fisiológica, são efetivamente empregadas em dosagens medidas e controladas nos modernos medicamento ou terapia. Estas são, por exemplo, propriedades analgésicas com morfina ou codeína , no contexto de protocolos de sedação ( anestesia ) frequentemente acompanhados por hipnóticos , ou então para uso como um agente antimalárico ( quinina , cloroquina ) ou agente. Drogas anticâncer ( vinblastina , vincristina ) e até sedação opióide com ibogaína .
Liberado de laboratórios químicos entre 1819 e 1827, a palavra alcalóide originalmente se referia a "comportamento químico semelhante a um alcalóide , ou seja, a qualquer corpo básico em meio aquoso" durante a operação de extração em meio líquido de base forte, solubilizando o soluto (s) básico (s) chamados alcalóides. Foi usado no século seguinte para descrever qualquer base de Lewis contendo um heterociclo nitrogenado ou, inadequadamente, uma função amina . Por causa do dupleto de elétrons não vinculativo do nitrogênio , os alcalóides são considerados bases de Lewis.
Histórico
O termo 'alcalóide', atestado em francês em 1827, pode ser decomposto pela raiz alcalóide * que significa "base ou alcalino ou caractere básico" e o sufixo -oïde * que significa "semelhante a, da mesma forma, do mesmo comportamento " O sufixo de origem greco-romana deriva do grego είδος "forma". A raiz vem do latim álcali medieval , ele próprio emprestado do árabe al-qétiyi por sua forma comum al qate, al qaly القالي "soda", uma planta do gênero Salsola da qual um carbonato de sódio mais ou menos foi extraído por muito tempo . menos puro, chamado "refrigerante", a partir do qual a soda cáustica pode ser feita . O termo al qali também designava, como a palavra refrigerante em francês com duplo uso para a salina e o refrigerante químico, a cinza calcinada com propriedades básicas.
Conhecimento e uso de alcalóides de plantas, tais como a papoula do ópio ou acônito , são muito antigos, mas o conhecimento de suas datas de substâncias activas apenas a partir do início do XIX ° século . Em 1803, Charles Derosne , farmacêutico e industrial francês, foi o primeiro a isolar um álcali vegetal extraindo do ópio uma mistura de narcotina e morfina , mas atribuiu a natureza alcalina de seu extrato aos resíduos da preparação. No ano seguinte, em 1804, Armand Seguin relata ter encontrado um processo para a preparação da morfina, mas não publica seus resultados até 1814. Finalmente, em 1805, na Vestfália, um assistente de farmácia, Friedrich Sertürner , reconhece a natureza alcalina do adormecido princípio do ópio. Dez anos depois, ele o chamou de morphium em referência a Morfeu , a divindade dos sonhos na Grécia antiga. Passando despercebidas na época, essas descobertas feitas na França e na Alemanha não foram reconhecidas até 1817, com a prova fornecida por Sertürner de que a morfina reage com o ácido para formar um sal.
A rivalidade franco-alemã continuou a ser frutífera desde que, entre 1817 e 1820, dois farmacêuticos franceses, Pelletier e Caventou , descobriram uma série impressionante de compostos ativos: cafeína , emetina (da ipeca), estricnina (da noz-vômito), quinina e cinchonina (da casca de cinchona).
O termo "alcalóide" foi cunhado em 1819 por um farmacêutico de Halle, Wilhelm Meissner (de) (1792-1853).
A elucidação das estruturas químicas de alcalóides começa em 1870 com a do mais simples, conina por Schiff, e alguns não revelar a sua estrutura no final do XX ° século , durante o qual Maurice-Marie Janot e seus alunos terão isolado, analisou e sintetizou mais de uma centena, estabelecendo, em 1953, a estrutura da corinanteína, um grande passo no progresso da química dos alcalóides.
Detecção de alcalóide
Alcalóides têm a propriedade de formar sais e ter um sabor amargo .
A caracterização da presença de alcalóide pode ser feita por precipitação usando:
- reagente silicotúngstico: reagente de Bertrand ;
- reagente fosfotúngstico: reagente de Scheibler ;
- reagente fosfomolíbdico: reagente Try-Sonenschein ;
- reagente fosfoantimônico: reagente de Schulze ;
- iodeto de potássio: reagente de Bouchardat ;
- tetraiodomercurato de potássio: reagente de Valser-Mayer ;
- iodobismutato de potássio: reagente de Dragendorff ;
- iodoplatinato de potássio;
- ácido pícrico ;
- taninos .
Muitos outros métodos, como cromatografia, também são usados para identificar e testar a molécula.
Extração de alcalóides
Como os alcalóides são mais freqüentemente encontrados na forma de sais de ácidos minerais ou orgânicos, e às vezes em sua combinação (incluindo taninos em particular), as plantas são pulverizadas com um álcali. Seu método de extração é muito variável dependendo da natureza do alcalóide, mas existem tipicamente dois esquemas de extração: por um solvente apolar em meio alcalino ou por um solvente polar em meio ácido (de Brönsted).
Solvente não polar em meio alcalino
- A planta seca é borrifada e umedecida com uma solução aquosa alcalina (cal, amônia NH4 + OH-, soda para deslocar bases fortes)
- Extração com um solvente orgânico não polar
- O bagaço é eliminado
- A solução orgânica (alcalóides, lipídios, pigmentos) é mantida
- Nós nos concentramos por aquecimento suave ou por um evaporador rotativo
- O concentrado é exaurido com um ácido diluído (geralmente é utilizado ácido sulfúrico 0,5 N) e, em seguida, é realizada uma extração (líquido - líquido).
- A solução aquosa ácida é alcalinizada
- Uma nova exaustão é realizada com um solvente orgânico imiscível (éter, clorofórmio, xileno)
- Obtém-se uma solução de alcalóide orgânico que deve ser concentrada por evaporação.
- Isso dá um resíduo de alcalóides brutos
Álcool ácido
- A planta seca é pulverizada na presença de álcool ácido
- Nós procedemos a uma lixiviação
- O bagaço é rejeitado
- A solução extraída (alcalóides, aminas, resinas, pigmentos) é evaporada
- Esta solução é retomada com ácido diluído (a solução aquosa ácida obtida contém sais de alcalóides impuros)
- A solução aquosa ácida é então alcalinizada para saponificar os sais alcalóides
- A exaustão é então realizada com um solvente imiscível (éter, xileno, clorofórmio)
- A solução de alcalóide orgânico é separada
- Esta solução é evaporada para obter um resíduo alcalóide bruto
Finalmente, as reações de precipitação do alcalóide são realizadas para verificação.
Classificações
Atualmente, estima-se que mais de 8.000 compostos de ocorrência natural foram identificados como alcalóides. Todos os anos, cerca de 100 novas moléculas são adicionadas por cientistas de todo o mundo. Para melhor compreender esta grande lista, três tipos de classificação de alcalóides foram propostos como segue:
- Suas atividades biológicas e ecológicas;
- Suas estruturas químicas;
- Suas vias biossintéticas.
Classificação estrutural
Há muito que são categorizados e nomeados de acordo com a planta, fungo ou animal do qual foram isolados.
A partir do XXI th século, eles são categorizados de acordo com sua estrutura química:
- grupo azolidines (pirrolidinas) : aniracetam (br) , anisomicina , CX614 (em) , dextromoramida , difenil prolinol (en) , ácido domoic , histapyrrodine (br) , caínico ácido , metdilazina , oxaceprol , prolintano , pyrrobutamine , higrina , cuscohygrine ;
- grupo de azinas : piperidina , conicine , trigonelina , arecaidine (br) , guvacine (br) , pilocarpina , citisina , nicotina , esparteína , pelletierine ;
- grupo tropano : atropina , hiosciamina , cocaína , ecgonina , escopolamina ;
-
quinolina grupo : acridina , ácido bicinconínico , broxyquinoline (br) , chlorquinaldol (br) , cinchophene (br) , clioquinol (br) , dequalínio (br) , dihydroquinine (br) , dihydroquinidine (br) , hidroxicloroquina , 8-hidroxiquinolina , o iodoquinol (en) , ido quinurico , mefloquina , nitroxoline (br) , oxycinchophene (br) , primaquina , quinino , quinidina , TSQ (br) , topotecano , ácido xanturénico (br) , estricnina , brucina , veratrina , cevadine , echinopsin
- aminoquinolinas : cloroquina , hidroxicloroquina , primaquina ,
- 8-aminoquinolina (in) s: primaquina , tafenoquina , rodoquina , pamaquina ;
-
grupo de isoquinolinas : dimethisoquine , quinapril , quinapirilate , debrisoquina , 2,2'-hexadecamethylenediisoquinolinium dicloreto , N-laurylisoquinolinium brometo , narceina , hidrastina , berberina
- alcalóides do ópio :
- natural: morfina , codeína , thebaine , papaverina , narcotine , noscapine ,
- semi-sintético: hidromorfona , hidrocodona , heroína ,
- sintético: fentanil , petidina , metadona , propoxifeno ;
- alcalóides do ópio :
- grupo de feniletilaminas (estes não são literalmente alcalóides, embora regularmente classificados como tal): MDMA , metanfetamina , mescalina , efedrina , catina e catinona ;
-
grupo de indóis :
- triptaminas : DMT , NMT (monometiltriptamina), psilocibina , serotonina , pseudoframina ,
- ergolins : da cravagem alcalóides de centeio ( ergometrina , ergotamina , ergosina , ergovalina , ergokryptine , ergocornina , ergocristina , ácido lisérgico , etc), ergina , LSD , etc.
- beta-carbolinas : harmina , ioimbina , reserpina , emetina ;
-
grupo purina :
- xantinas : cafeína , teobromina , teofilina ;
-
grupo terpenóide :
- os alcalóides do acônito napel : aconitina ,
- solanidina , solasodine , batrachotoxine , delphinine ,
- esteróides : solanina , samandarina ;
- grupo de betaínas ( compostos de amônio quaternário, não são alcalóides no sentido próprio, mesmo que regularmente classificados como tais): muscarina , colina , neurina ;
- grupos pirazol .
Classificação biogenética
Alcalóides podem ser classificados de acordo com seu precursor antes de serem sintetizados em uma via biológica. Três classes principais são então distinguidas dependendo se têm ou não um aminoácido como precursor direto e se contêm ou não um átomo de nitrogênio em um heterociclo.
| Derivado de aminoácido | Heterociclo nitrogênio | |
|---|---|---|
| Alcalóides verdadeiros | sim | sim |
| Protoalcalóides | sim | não |
| Pseudo-alcalóides | não |
Alcalóides verdadeiros são derivados de aminoácidos e possuem um átomo de nitrogênio em um sistema heterocíclico. São substâncias dotadas de grande atividade biológica, mesmo em baixas doses. Eles aparecem nas plantas, seja na forma livre, seja como um sal ou como N-óxido.
Os protoalcalóides são aminas simples, cujo nitrogênio não está incluído em um heterociclo. Eles também são derivados de aminoácidos.
Os pseudoalcalóides não são derivados de aminoácidos. No entanto, eles podem estar indiretamente ligados à via dos aminoácidos por meio de um de seus precursores ou de um de seus pós-cursores (derivados). Eles também podem resultar de aminação , ou de uma reação de transaminação em uma via conectada com os precursores ou pós-cursores de aminoácidos.
Tadeusz Aniszewski propõe a seguinte classificação, com base nos precursores da via biológica sintética.
| Precursor | Grupo de alcalóides | Núcleo característico | Exemplos |
|---|---|---|---|
L- ornitina 
|
Alcalóides pirrolidina |
Pirrolidina |
Cuscohygrine , Hygrine |
| Alcalóides tropânicos |
Tropane |
Atropina , cocaína , hiosciamina , escopolamina | |
| Alcalóides pirrolizidínicos |
Pirrolizidina |
Acetil-licopsamina , Europina , Homospermidina , Ilamina , Meteloidina , Retronecina |
|
L- lisina 
|
Alcalóides piperidínicos |
Piperidina |
Anaferina , Conine , Lobélanine , Lobelina , Pelletierine , piperidina , piperina , Sedamine |
| Alcalóides quinolizidina |
Quinolizidina |
Cytisine , lupinina , Esparteína | |
| Alcalóides indolizidínicos |
Indolizidina |
Castanospermina , Swainsonina | |
L- tirosina 
|
Alcalóides tetrahidroisoquinolínicos simples |
Benzyltetrahidroisoquinolina |
Codeína , Morfina , Norcoclaurina , Papaverina , Tetrandina , Tebaína , Tubocurarina |
| L- tirosina ou L- fenilalanina | Alcalóides de feniletilisoquinolina | Alcalóides de Amaryllidaceae | Crinin , Floramultine , Galantamine , Lycorine |
L- triptofano
|
Alcalóides indólicos |
Indole
|
- Arundacine , Psilocina , serotonina , Tryptamine , Zolmitriptan - Elaeagnine , Harmine - Ajmalicine , Catharantine , Tabersonine |
| Alcalóides quinolina |
Quinolina |
Cloroquinina , Cinchonidina , Quinina , Quinidina | |
| Alcalóides pirroloindólicos | Indole | A- ioimbina , quimonantheína , corinanteidina | |
| Alcalóides da cravagem do centeio |
Ergoline 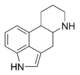
|
Ergotamina , Ergokryptine | |
L- histidina 
|
Alcalóides imidazol |
Imidazol |
Histamina , Pilocarpina , Pilosina |
| Alcalóides de manzamina | Xestomanzamina | Xestomanzamina A e B | |
| L- arginina |
Alcalóides marinhos |
β-carbolina 
|
Saxitoxina , tetrodotoxina |
Ácido antranílico 
|
Alcalóides quinazolínicos |
Quinazoline |
Peganin |
| Alcalóides quinolina |
Quinolina |
Acutin , Bucharine , Dictamine , Foliodine , Perforine , Skimmianine |
|
| Alcalóides acridônicos |
Acridina |
Acronicina , Rutacridona | |
Ácido nicotinico 
|
Alcalóides piridínicos |
Piridina Pirrolidina |
Anabasine , Cassinine , Evoline , Nicotine , Wilforine |
Os protoalcalóides são compostos nos quais o átomo de nitrogênio N derivado de um aminoácido não faz parte de um heterociclo.
| Precursor | Grupo de alcalóides | Núcleo característico | Exemplos |
|---|---|---|---|
L- tirosina
|
Alcalóides de feniletilamina |
Feniletilamina |
Adrenalina , Anhalamine , Dopamine , Noradrenaline , Hordenine , Mescaline : |
L- triptofano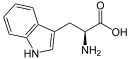
|
Alcalóides indoloterpênicos |
Indole
|
Ioimbina |
L- ornitina
|
Alcalóides pirrolizidínicos |
Pirrolizidina |
4-hidroxi-estaquidrina , estaquidrina |
Pseudo-alcalóides são compostos cujo esqueleto de carbono básico não deriva de aminoácidos.
| Precursor | Grupo de alcalóides | Núcleo característico | Exemplos |
|---|---|---|---|
acetato 
|
Alcalóides piperidínicos |
Piperidina |
Coniine , Conicein , Pinidine |
| Alcalóides sesquiterpênicos | Sesquiterpeno |
Cassinine , Évonine , Maymyrsine , Wilforine |
|
Ácido pirúvico
|
Alcalóides da efedrina | Fenil C | Catina, catinona, efedrina , norefedrina |
ácido ferúlico 
|
Alcalóides aromáticos |
Henyl 
|
Capsaicina |
|
geraniol |
Alcalóides terpênicos | Terpenóides |
Aconina , Aconitina , Metillicaconitina , Actinidina , Atisina , Gentianina |
| saponinas | Alcalóides esteróides |
Colestano , Conessine , Jervine, Etioline, pregnenolona , solanidina |
Interesse atual em alcalóides
Devido às suas funções fisiológicas ou às suas atividades biológicas específicas, as moléculas alcalóides continuam a ser reagentes biológicos importantes. Eles ainda são de interesse atual na terapia. Se a busca por princípios ativos continua ativamente em relação às plantas medicinais e / ou tóxicas, os alcalóides conhecidos são os produtos básicos da farmácia. Em 1995, representavam em valor na indústria farmacêutica cerca de 1,5 bilhão de francos, a mesma classificação dos hormônios, cifra superada pelas vitaminas com 1,8 bilhão de francos, mas excedendo em valor os antibióticos de 1,2 bilhão de francos.
A nicotina é um inseticida vegetal natural. Seus efeitos são multiplicados se o composto tóxico for adicionado a uma emulsão de óleo vegetal, chamada de óleo branco. O todo é rapidamente biodegradável. A rianodina foi usada como inseticida botânico.
Notas e referências
- O químico Maurice-Marie Janot definiu cinco critérios: 1. Pertencer a uma classe de moléculas orgânicas, com estrutura formada por um arranjo de átomos de carbono , hidrogênio e oxigênio 2. Presença de nitrogênio na estrutura molecular 3. formação de sais (com a notável exceção da colchicina, não salificável 4. Atividade fisiológica reconhecida 5. Obter derivados insolúveis com uma variedade de reagentes gerais de alcalóides. Outros químicos descobrem que a definição deste grupo heterogêneo de moléculas é consistente, tamanho grande o suficiente é difícil, se não impossível se não esquecermos os derivados dessas moléculas com propriedades comparáveis. Na verdade, as estruturas moleculares e as propriedades químicas, mas também os efeitos biológicos observados são muito variados. classificações, descobertas e estudos de alcalóides têm sido uma alavanca poderosa e jogado um papel estimulante na química das substâncias naturais.
- O nome original lembra a planta ou organismo de origem ou associado à descoberta: Nicot grass ou tabaco, a bebida de café , a flor da Bela Dama ou Atropa belladona ... Em menor medida, lembra a atividade fisiológica ou a papel farmacológico: emetina para a função emética, morfina para adormecer "nos braços de Morfeu" ...
- O campo de estudo, inicialmente limitado ao reino vegetal, estendeu-se aos animais terrestres e marinhos, bem como a diversos microrganismos.
- É mais fácil decidir pela Datura , espécie de planta causadora de alucinações e transes, procurada em antigas culturas xamânicas.
- Geralmente são iguais. Assim, a estricnina em quantidades muito pequenas por suas propriedades estimulantes, a cafeína ...
- " Tratamento com ibogaína e efeitos colaterais | Centro de desintoxicação de drogas ” , em www.desintoxicationdrogue.fr (consultado em 21 de setembro de 2015 )
- acordo com o Grande Robert
- Bruneton, J. Farmacognosia - Fitoquímica, plantas medicinais, 4 ª edição, revista e ampliada. , Paris, Tec & Doc - International Medical Publishing,2009, 1288 p. ( ISBN 978-2-7430-1188-8 )
- (in) Paul Bernard Foley, feijão, raízes e folhas: uma história da terapia química do parkinsonismo , Tectum Verlag,2003
- (en) Tadeusz Aniszewski, Alcaloides - Segredos da Vida, Química de Alcaloides, Significado biológico, Aplicações e Papel Ecológico , Elsevier, 2007
- Quid 1998
Bibliografia
- Arnold Brossi, The Alkaloids, Chemistry and Pharmacology , Academic Press, 1989.
- RHF Manske (eds.), The Alkaloids: Chemistry and Physiology, Chemistry and Physiology, Vol. 1-20, Academic Press Inc., 1950-1981. [1] . A partir de 1981, a série foi continuada pela edição científica de HL Holmes, então Arnold Brossi. Agora tem cerca de trinta volumes.
- Jacques E. Poisson, artigo de Alcaloïdes , Encyclopædia Universalis , 2011.
- A.-Mathieu Villon e Pierre Guichard , Dicionário de química industrial: contendo as aplicações da química à indústria, metalurgia, agricultura, farmácia, pirotecnia e artes e ofícios , Paris, Librairie científica e industrial (Bernard Tignol e Henri Nolo),1880( reimpressão 1902), não paginado em três volumes p. ( leia online )